【総説】多点相互作用を誘起するイオン液体・オリゴマーイオン液体 ―グラフェンの高効率合成・高キャパシタンス電解質の実現
本記事は、和光純薬時報 Vol.87 No.3(2019年7月号)において、物質・材料研究機構 国際ナノアーキテクトニクス研究拠点 松本 道生様、理化学研究所 創発物性科学研究センター、東京大学大学院 工学系研究科 相田 卓三様に執筆いただいたものです。
はじめに
1992年にWilkesらによって1-エチル-3-メチルイミダゾリウムテトラフルオロボラートは常温で溶融した塩で、空気中でも安定な液体であると報告された1)。この報告は水系溶媒、有機溶媒に加わる、第三の溶媒として「イオン液体」という新しい研究分野を切り拓いた2)。
イオン液体は「室温付近に融点を有する塩であり、イオンのみからなる液体」と定義される。イオン液体の特徴は(1)蒸気圧が低く不揮発性であること、(2)熱安定性が高くかつ難燃性であること、(3)極めて高いイオン雰囲気を作り、またイオン導電性であることなどがあげられる。
それに加えて、特に有機化学者の注目を集めたのは、イオン液体としての性質を示す分子構造が多様で、分子設計の自由度が大きいことであった。イオン液体は溶融塩であるため、カチオンとアニオンの組み合わせで構成される。特に有機カチオンを構造に含むことが多く、カチオン、アニオンともに化学構造が大きく変化を加えられる。
我々はこのイオン液体の化学構造の可変性と超分子化学の相互作用増強法である多点相互作用の考え方を組み合わせることで、オリゴマーイオン液体(OIL)を新たに開発した(図1)。OILの基本構造は有機カチオンのイミダゾリウムを連結させることで、一分子に複数のカチオンを持つ構造である。これは従来のイオン液体の多くが一分子につき、一つのカチオンを持つという点で大きく異なる。
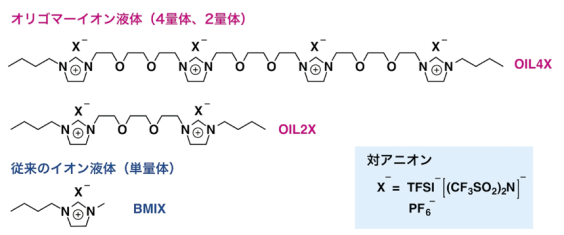
図1.オリゴマーイオン液体(OIL)と従来のイオン液体の化学構造
このOILを用いることで、グラファイトの剥離とイオン液体をゲート材料に用いるトランジスター素子という全く異なるプロセスの高効率化に共に成功した。以下、開発の経緯について紹介する。
グラファイトから単層グラフェンを超高効率に剥がし出す
2003年に、有機カチオンであるイミダゾリウムを分子構造に持つイオン液体がカーボンナノチューブ(CNT)を分散させるのに著しく優れた溶媒であることが相田研究室で見出された3)。市販のCNT粉末中ではCNT表面のπ共役表面同士がπ-π相互作用によって会合するため、CNTが束になってバンドル化している。
π-π相互作用は分子間相互作用の一種であり、一般にはその結合力は弱く、会合体は簡単に壊れる。しかしながら、CNTの束の場合、CNTの筒が同一方向に揃って束となるため、π-π相互作用をする局面同士が接触する距離が長い。その結果、弱い力ながら結合する部位が非常に長く(多く)なるため、全体の結合は著しく強くなる。
この一つずつは弱い力でありながら、相互作用を起こす点の数を増やすことで全体の会合を強める現象を多点相互作用を呼び、生体中などでも多く見つけられる超分子化学の考え方である4)。この多点相互作用による強い会合形成のため、CNTは溶媒和させづらく、液体媒質に高濃度に分散させることが著しく難しかった。
福島らはイオン液体中のイミダゾリウムが、CNTのπ共役表面とカチオン-π相互作用を引き起こすことで、CNT同士のバンドル化を妨げ、さらにほぐし、同イオン液体中でCNTを高濃度に分散できることを見出した3)。この分散液はほぐれたCNTを著しく多く含むため、CNTが分散液中で絡み合い、ゲル化する。イオン液体はイミダゾリウムを溶融塩カチオンとして著しく高密度に含むことができる。これにより、強いCNT同士の結合を量論的に弱めることができ、CNTを高分散させることができた。
このCNTでの発見以降、イミダゾリウムを含む分子をCNT以外の炭素材料の分散にも用いる報告が数多くなされた。特に近年、注目を集める二次元炭素材料、グラフェンを、前述のCNTと同様に、積層体であるグラファイトから剥離させる試みは様々行われていた5)。
しかしながら、前述のCNTを破格に分散させることができた、イミダゾリウムを持つイオン液体は、グラファイトを剥離させるのに十分な溶媒ではなかった。これはCNTではπ-π相互作用が「曲面-曲面」で作用するため、比較的細い、「線」として作用するのに対して、グラファイトの場合は、「平面-平面」での相互作用のため、面積が大きい「面」として相互作用することに起因する。
つまり、グラファイトはCNTよりも、はるかに多い点での相互作用があるため、多点相互作用のより強い寄与があり、会合状態がCNTよりも安定化している。結果、従来のイミダゾリウムを持つイオン液体をもってしても、グラファイトを剥離するのに十分でなかったのだ。
ここで、我々はグラファイトの多点相互作用に対抗するため、「目には目を」の考えで、イオン液体の側にも多点相互作用を引き起こす化学構造を導入し、多点のカチオン - π相互作用をイオン液体 - π共役表面で誘起させれば、グラファイトも剥離できるのではないかと考えた。
多点相互作用を導くイオン液体の構造として、イミダゾリウムを連結させたオリゴマーイオン液体、OILを合成した。イミダゾリウムをエチレングリコール鎖で繋ぐことにより合成した、イミダゾリウムを2つ(OIL2)、もしくは4つ(OIL4)繋いだカチオンに対して、アニオンをヘキサフルオロフォスフェートイオン(PF6-)もしくはビス[(トリフルオロメチル)スルホニル]イミドイオン(TFSI-)を選ぶことで、室温で液体として振る舞うイオン液体を得た(図1)。
余談ではあるが、連結させる鎖の化学構造はイオン液体としての溶融挙動に大きな影響を及ぼす。エチレングリコール鎖の代わりに同様の長さのアルキル鎖で繋いだ構造は融点が著しく高く、特にアルキル鎖で繋いだ二量体カチオンとPF6-アニオンの組み合わせでは室温で固体となった。これはアルキル鎖の結晶性の良さに起因していると考えられる。
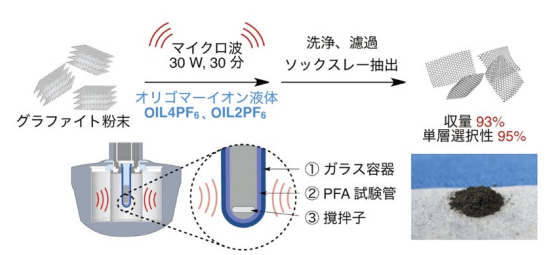
図2.OILを用いたグラファイトの高効率剥離
さて、我々は合成したオリゴマーイオン液体OILを用いて、グラファイト剥離を検討するため、OIL2カチオンとPF6-アニオンを持つOIL2PF6とOIL4カチオンとPF6-アニオンを持つOIL4PF6のそれぞれに、グラファイトを懸濁させ、それぞれにマイクロ波を照射した(図2)。マイクロ波を当てることでグラファイトの積層構造に由来するXRDピーク(グラファイト(002)ピーク)が大きく減少し、グラファイトの剥離が起きていることが示唆された。
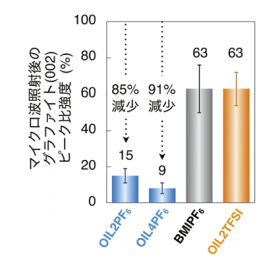
図3.イオン液体構造に依存したグラファイトの剥離効率の違い
この大きなピーク強度の減少はOIL4PF6とOIL2PF6でのみ起こる。CEM社のマイクロ波合成装置Discoveryを用いて、シングルモードのマイクロ波30Wを30分照射したところ、懸濁液中のグラファイト(002)ピーク強度がOIL4PF6とOIL2PF6の懸濁液でそれぞれ85%、91%減少した(図3)。これは従来のモノマーイオン液体である、1-ブチル-3-メチルイミダゾリウムヘキサフルオロフォスフェート(BMIPF6)を懸濁液に用いたサンプルとは大きく異なる結果である。
このマイクロ波照射した懸濁液から剥離片を取り出すため、複数の溶媒をソックスレー抽出の抽出溶媒として用いて、洗浄し固形残渣を回収した。OIL2PF6を懸濁液に用いたサンプルから得られた黒色粉体は、原料のグラファイトに対して高収量(95%)であり、さらに原子力間顕微鏡(AFM)で観察されたシート化合物の93%が、厚さ1.0 nm以下であることがわかった。
液相剥離法で剥離されたグラフェンは一般に1.0 nm以下の厚さのものを単層グラフェンと評価されるため、93%が単層グラフェンであると結論づけた。本剥離グラフェンは不純物、構造的欠陥をほとんど含まないことをラマン分光法とX線光電子分光法を用いて確認している。本手法はマイクロ波を30分当てるだけで、高品質な単層グラフェンを簡便に提供することができる6)(コラム参照)。
また、興味深いことにこの剥離現象は、OILの対アニオンがPF6-であるときのみ観測され、OILの対アニオンがTFSI-では観測されなかった(図3オレンジ)。イオン液体中のPF6-はTFSI-と異なり、マイクロ波照射時にイオン液体中に混入する少量の水と反応し、少量のフッ化水素(HF)が発生する。HFはグラファイトへの層間挿入が過去に報告されており、本系でも剥離初期の層間挿入に関与していると思われる。
OILの電解質としての利用とトランジスタ素子効率の向上
OILによる多点相互作用はグラファイト剥離のみでなく、イオン液体をゲート材料に用いるトランジスタ素子でも効果を発揮した。上述のグラファイト剥離では、多点相互作用の考え方を用いることで、イオン液体中のイミダゾリウムカチオンとグラフェンのπ共役表面とのカチオン - π相互作用を増強させ、単層グラフェンへの選択的なグラファイト剥離を実現した。
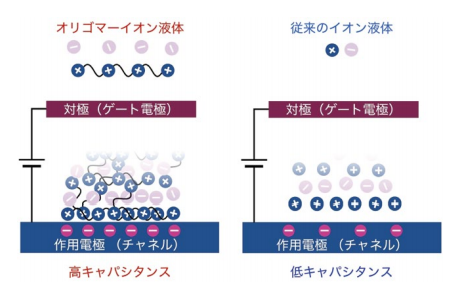
図4.OILを用いた高キャパシタンス電解質
括弧外、括弧内のそれぞれの電極名称は電気化学測定、電気二重層トランジスタの電極呼称に対応する。さらに、我々はイオン液体を電解質として用いる系の、電解質(イオン液体) - 電極の静電相互作用でも、多点相互作用による寄与が観測できるのではないかと考えた。イオン液体を電解質として用いる場合、電極に電圧を印加すると、電極電荷と反対の電荷を持つイオンが最近接し、その上にカチオンとアニオンの層が交互に積み重なる層状の電気二重層を形成すると言われている7)。つまり、電極に負電荷が蓄積されたときは、イオン液体のカチオンが、正電荷が蓄積されたときはアニオンが最近接すると考えられている。
当然、電荷を持つ電極と最近接イオンとは静電相互作用によって相互作用する。我々はこの電極と最近接イオンとの静電相互作用も多点相互作用の概念で増強可能で、その結果、電気二重層としての静電容量向上に寄与するのではないかと考えた(図4)。
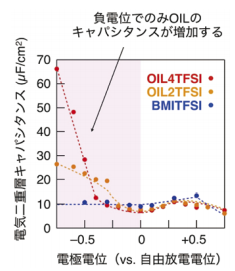
図5.イオン液体の電位に依存したキャパシタンス挙動
電気化学インピーダンス法を用いて、金電極上でのOIL2TFSI、OIL4TFSI(電気化学的な安定性の観点からTFSI-を用いた)の静電容量についての電極電位依存性を調べた。オリゴマー構造を持つカチオンが近接する電極電位が負の時には、モノマーイオン液体に対して最大で6倍の静電容量の上昇がOIL4TFSIで観測されたのに対して、アニオンが近接する電極電位が正の時には静電容量の上昇は観測されなかった(図5)。このことからカチオンのオリゴマー構造が静電容量の上昇に寄与していることが示唆された。
さらに、n型半導体であるSrTiO3上に電気二重層トランジスタ素子を形成し、ゲート材料としてのOILと従来のモノマーイオン液体の違いを検証したところ、OILを用いたトランジスタ素子は、より低い動作電圧でon - off のスイッチングを引き起こし、高い電荷導入率を示すことがわかった8)。このトランジスタ素子構造はFeSeのデバイスにも応用され、従来のイオン液体を用いた素子と比べて、FeSeの超電動転位温度を6K上昇させることができることも確認されている9)。
おわりに
我々はOILを用いることで、グラファイトからグラフェンへの高効率剥離と電気二重層トランジスタの高効率化に成功した。多点相互作用を誘起する本構造は、高品質グラフェンを得る簡便な手法を提供するだけでなく、イオン液体を用いる様々な応用用途での効率の向上をもたらす可能性がある。二次元高分子の合成から物性物理の研究現場、電気二重層キャパシタとしての検討など、広くご利用いただけたら幸いである。
本研究を通して多くの共同研究者の協力を得た。特に、東京工業大学 福島 孝典 教授、横浜国立大学 渡邉 正義 教授、東京大学・理化学研究所 岩佐 義弘 教授、東北大学 塚崎 敦 教授とそれぞれのグループには実際に実験を共同、もしくは OIL を利用しての実験を行なっていただいた。謝意を表す。それぞれの共同研究の詳細に関しては原著論文をご確認いただきたい。また、今回、OILの試薬販売にあたって富士フイルム和光純薬株式会社と株式会社東京大学TLOのそれぞれのご担当者様に多大なご助力をいただいたことに感謝する。
参考文献
- Wilkes, J. S. and Zaworotko, M. J. : J. Chem. Soc. Chem. Commun., 0, 965 (1992). DOI: 10.1039/C39920000965
- 高分子学会編:「イオン液体」,2 巻(共立出版) (2012).
- Fukushima, T. et al . : Science , 300, 2072 (2003). DOI: 10.1126/science.1082289
- Fasting, C. et al. : Angew. Chem. Int. Ed., 51, 10472 (2012). DOI: 10.1002/anie.201201114
- Nicolosi, V. et al. : Science, 340, 1226419 (2013). DOI: 10.1126/science.1226419
- Matsumoto, M. et al. : Nat. Chem., 7, 730 (2015). DOI: 10.1038/nchem.2315
- Fujimoto, T. and Awaga, K. : Phys. Chem. Chem. Phys ., 15, 8983 (2013). DOI: 10.1039/C3CP50755F
- Matsumoto, M. et al . : J. Am. Chem. Soc ., 139, 16072 (2017). DOI: 10.1021/jacs.7b09156
- Miyakawa, T. et al. : Phys. Rev. Mater ., 2, 031801 (2018). DOI: 10.1103/PhysRevMaterials.2.031801
グラファイト(12.5 mg)をOIL2PF6 (0.5 mL)中に懸濁させ、テフロン容器の入ったマイクロ波照射試験管に攪拌子とともに導入する。シングルモードのマイクロ波照射装置で固形化しないようにマイクロ波照射を行う。(CEM社 Discoveryの場合コンプレッサー使用時、30 W, 30分、反応容器の温度が同装置上 170 ℃程度で安定) マイクロ波照射後、5 mLのジメチルスルフォキシド(DMSO)で希釈し、その希釈液をPTFE製のソックスレーフィルターに移し、ソックスレー抽出器を用いて洗浄した。抽出溶媒としてDMSO(減圧:~30 mmHg)、2,2,2-トリフルオロエタノール、ジクロロメタンを順次用い、各溶媒で抽出液が色づかなくなるまで洗浄した。ジクロロメタンでの洗浄後、フィルター上の固体残渣を減圧条件下で乾燥し、黒色粉体を得た。





