【連載】アミノ酸分析~新たな潮流~ 「第 4 回 ペプチド、タンパク質定量のための新技術」
本記事は、和光純薬時報 Vol.87 No.3(2019年7月号)において、第一三共株式会社 研究開発本部 薬物動態研究所 合田 竜弥様に執筆いただいたものです。
はじめに
アミノ酸から構成されるペプチド及びタンパク質は、遺伝子の最終産物であり、細胞の形態や機能を直接制御している。そのため、癌化等により細胞の形態や機能が変化する過程で、個々のペプチド及びタンパク質の発現量、翻訳後修飾等が変化する。これらの変化は、患者の層別化、疾患の早期診断、薬効評価等のためのバイオマーカーとして利用可能であり、病態の原因解明を目指した研究と共に盛んに行われている。これらの研究では、ペプチド及びタンパク質の個体内及び個体間変動を評価できるような、測定変動の極力小さい定量法が重要となる。
また、ペプチド及びタンパク質は、医薬品の新しいモダリティとしても活用されている。その代表例が抗体医薬品である。現在の医薬品開発研究は、低分子化合物を中心とした創薬から抗体医薬品に代表されるバイオ創薬へシフトしており、抗体医薬品の売上高はすでに世界におけるランキング上位を占めている。さらに、低分子医薬品や抗体医薬品では狙えない新しい標的分子を創薬ターゲットとした、分子量の小さいペプチド等を含む中分子創薬も積極的に展開されており、次世代の医薬品として高い期待が寄せられている。ここでも、ガイドラインに準拠した正確な真度及び精度を有するペプチド及びタンパク質の定量法が必要となる。
しかし、アミノ酸が複数つながったペプチド及びタンパク質は、様々な高次構造を形成することが可能であり、低分子化合物であるアミノ酸とは物性が大きく異なる。特に、吸着や凝集等の現象が強く認められ、取り扱いにも注意が必要となる。これらの性質は、通常の LC 分析において、ピーク形状の悪さ、カラム充填剤からの回収率の低さ、高感度化の難しさ等の問題を引き起こすことから、ペプチド及びタンパク質定量のためには、低分子化合物であるアミノ酸分析とは全く異なる工夫が必要である。
ペプチド及びタンパク質定量のための新しい技術として、前処理法、使用容器やカラム等の素材検討をはじめ、分析現場では様々な工夫が行われているが、ここでは、ペプチド吸着制御 LC(Peptide Adsorption-Controlled LC, PAC-LC)を紹介したい。
LC 分析におけるペプチドの吸着の影響
先に述べた通り、ペプチド及びタンパク質の吸着は、正確な取り扱いを困難とし、結果として高感度定量を困難とする。
例えば、アミノ酸残基数 40、分子量 4,696のペプチドであるurocortinを用い、アセトニトリル含量の異なるurocortin溶液(1 nM)100 μLをLC に導入した時に得られるSRMクロマトグラムを図 1A に、カラムに保持された urocortin のピーク面積値を図 1B に示す。この時、水だけに希釈された溶液では urocortinピークは確認できない。これは、添加した酸に関わらず、容器やチップ、ニードル等への吸着によってurocortin が失われていることを示しており、このような操作法では nM レベルでの検出もできないことが分かる。
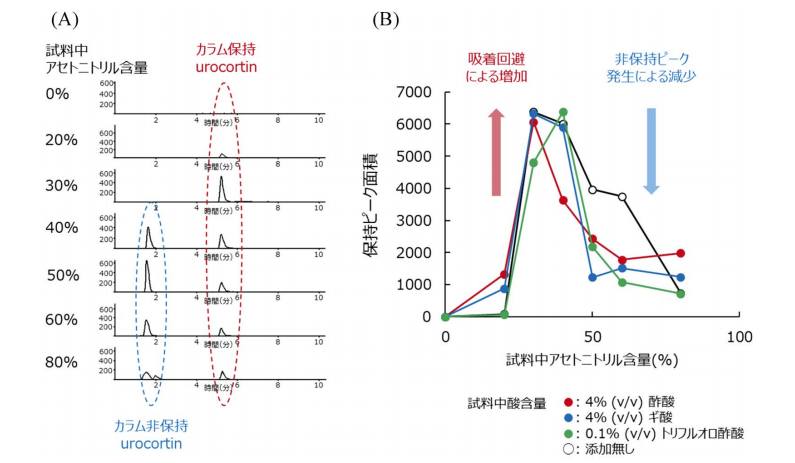
図1.アセトニトリル含量の異なる urocortin 溶液(1 nM)の SRM クロマトグラム(A)及び保持ピーク面積(B)
一方、アセトニトリルを添加することで urocortin のピークが検出されてくるが、カラムに保持した urocortin のピーク(以後、保持ピーク)の面積値は安定しない。これは、アセトニトリル含量が 30%までの場合、urocortin の容器やチップ、ニードル等に対する吸着を完全に回避できていないためである。一方、アセトニトリル含量が 40%以上の場合、urocortin の容器等への吸着を回避できているものの、カラムに全く保持されていない urocortin ピーク(以後、非保持ピーク)が発生し、これが保持ピークの面積値の減少を引き起こす。
従って、urocortin を定量するためには、吸着を完全に回避しつつ、urocortin を1本のピークとして検出可能なアセトニトリル含量が 30% の溶液を用いる必要がある。しかし、urocortin の吸着の程度は、時間の経過によって変化し、また、その他の共存成分によっても影響を受けることから、生体試料のような複雑なマトリックス中の測定においては、アセトニトリルの適切な含量を一義的に 30% と決めることは難しいと考えられる。
ペプチドの吸着能の相転移現象
先に述べた現象は、分子量 1,007 〜 45k の様々なペプチド及びタンパク質において認められ、さらに、この現象を惹起する有機溶媒として、アセトニトリル以外に、メタノール、エタノール、酢酸及びギ酸等が確認されている1)。従って、試料溶液中の有機溶媒含量を増加させることによって、保持ピークに加えて非保持ピークが発生する現象は、ペプチド及びタンパク質にとって普遍的な現象であると考えられる。
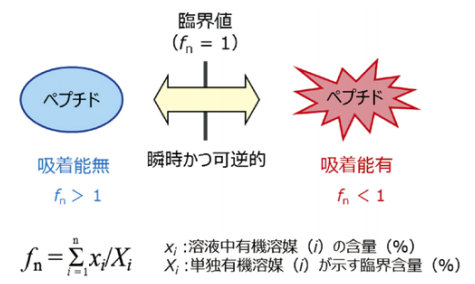
図2.ペプチドの吸着能の相転移理論
この普遍的な現象を説明するためには、ペプチド及びタンパク質のカラム充填剤に対する吸着能が、特定の有機溶媒含量(臨界値)を境に急激かつ可逆的に変化(相転移)する(図 2)と考える必要がある。
つまり、ライン内径及び流速等を考慮すると、LC に導入された 100 μL の urocortin 溶液のほとんどは導入時の溶液組成を保ったままカラムに到達しており、この場合、urocortin はカラム充填剤に対する吸着能を失ったままであるため、カラムを素通りして非保持ピークとして溶出されると考えられる。一方、カラム到達までの間に後ろを流れる移動相と混合してアセトニトリル含量が低下した溶液中の urocortin は、カラム充填剤に対する吸着能を瞬時に回復してカラムに保持された結果、保持ピークとして溶出されると考えられる。
この理論に従う場合、アセトニトリルが urocortin のカラム充填剤に対する吸着能に対して示す臨界値は、図 1A のクロマトグラムから30 〜 40%の間に存在すると推定されるが、これは、アセトニトリルによって惹起されるurocortin の高次構造の変化の臨界値と同じであることが CD スペクトル解析により示されている2)。同時に、この高次構造変化が可逆的であることも示されていることから、urocortin のカラム充填剤に対する吸着能の急激な変化と可逆性は、その高次構造の変化に伴うものであると考えられる。
ペプチド及びタンパク質の吸着能の相転移現象は、従来、タンパク質及びペプチドの逆相分離で説明されてきた、『最初にカラム入口付近の固定相表面に分配保持されたタンパク質及びペプチドは、移動相中の有機溶媒濃度がある特定値に達したときに固定相からはじめて脱離し、一旦脱離したものはそれ以降固定相とは何ら相互作用せずにカラムから溶出される』、という考え方と基本的に同じである。しかし、高次構造の可逆性に伴う吸着能の可逆性を考慮すると、ペプチド及びタンパク質は、臨界値の有機溶媒含量の溶離液付近で固定相表面への保持と脱離を繰り返しながら溶出されているものと考えられる。
ペプチド吸着制御 LC の開発
これまで述べてきた有機溶媒によって惹起されるペプチドのカラム充填剤に対する吸着能の相転移現象を利用することで、より正確に高感度なペプチド定量を可能とする、ペプチド吸着制御 LC(Peptide Adsorption-Controlled LC, PAC-LC)を開発した(図 3)2-4)。
PAC-LC は、標準 LCと比較して、水系移動相用のポンプ位置が異なり、カラム直前で水系移動相を混合するシステムになっている。2 液用としても使用できるが、3 液用の場合、標準 LCとして利用する際にラインのつなぎ換えが必要とならないメリットがある。
この PAC-LC の特徴は、カラム入口前での水系移動相との混合により、導入されたペプチド周りの有機溶媒含量を強制的に変化させることにある。例えば、アセトニトリル含量 50% のペプチド溶液を、水系 100%の移動相 Aと有機溶媒系移動相 B(3 液用の場合 B 及び C)との混合比が 9 対 1 の条件下で導入した場合、カラムに到達するペプチド周りのアセトニトリル含量は 5%となる。これは、アセトニトリルがペプチドの吸着能に対して示す臨界値が 20% である場合、導入時の溶液中でカラム充填剤に対する吸着能を失っていたペプチドが、アセトニトリル含量 5%の溶液中でカラム充填剤に対する吸着能を瞬時に回復してカラムに保持されることを意味する。一方、アセトニトリル含量 50%の溶液中のペプチドは、容器、ニードル、チップ等の固体への吸着能も失っていることから、操作及び LC 導入時の定量性を担保できることを意味する。
実際に、PAC-LCを用いてアセトニトリル含量の異なるurocortin 溶液を測定した場合、urocortin は常に 1 本の保持ピークとして検出され、臨界値(30 〜 40%)より大きいアセトニトリル含量の溶液を用いた場合にほぼ同じピーク面積値が得られている(図 4)。また、アセトニトリル含量 50% の溶液で調製した urocortin 検量線試料のピーク面積は濃度に比例し、10 pM から10 nM の濃度範囲で理論値の±15%以内の良好な真度を有する検量線が得られ 2)、さらに、吸着を回避できるアセトニトリル含量の試料を繰り返し測定した時の測定精度は、アセトニトリル含量に関わらず良好な値(10% 以下)を示している 3)。
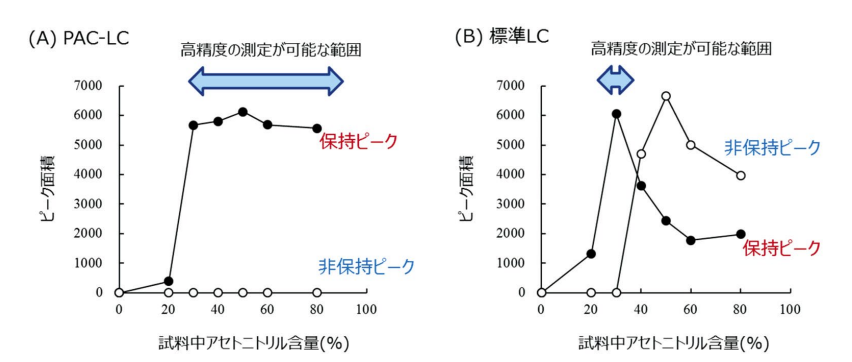
図4.アセトニトリル含量の異なる urocortin 溶液を測定した場合のピーク面積
これらは、臨界値以上のアセトニトリルを用いることで試料調製及び導入時の吸着を回避できること、及びPAC-LCにより1 本のピークとして検出できるために精度の高い測定が可能であることを示している。
一方、標準 LCを用いた場合、標準溶液であるにも関わらず、非保持ピーク及び保持ピークの割合の不規則な変化により測定精度が損なわれることが確認されている 3)。これは、カラム到達までの間に後ろを流れる移動相との混合が均一に起こらないことを示唆している。よって、正確な定量のためには 1 本のピークとして検出できる臨界値近辺の有機溶媒含量の溶液を使用する必要があることを示しており、この事実は、臨界値の大きく異なるペプチド及びタンパク質を高い精度で同時定量することが困難であることを表している。
以上のように、PAC-LC は、標準 LCと比較して、高い測定精度での定量を可能とする試料溶液中の有機溶媒含量範囲が広く、また、臨界値の異なる多成分ペプチドの同時測定を高精度で実施可能な点で大きく優れている。
PAC-LC を用いた生体試料中ペプチド及びタンパク質の定量
抗体医薬品は、ヒトの生体防御に寄与するタンパク質である免疫グロブリン(IgG、IgM、IgD、IgE、IgA)を遺伝子組み換え技術等を応用して作成したものであり、上市されている全ての抗体医薬品は IgG を基としたアミノ酸配列を有している。近年、動物及びヒト血漿中の抗体医薬品をトリプシン消化法 5)にて定量する方法が積極的に検討されているが、内在する IgG や夾雑成分と区別するために、最適なペプチド断片を選択する必要がある。
PAC-LC を用いる場合、トリプシン消化によって得られる様々な特性のペプチド断片の正確な同時測定が可能であるため、消火条件や LC 条件の最適化が容易に実施でき、最適なペプチド断片を効果的に獲得できるメリットがある。また、実試料測定においては、複数ペプチドの同時測定により抗体医薬品の生体内における構造変化(バイオトランスフォーメーション)を評価できる可能性を秘めている。
また、認知症の一種であるアルツハイマー病の主な病理学的特徴の一つである老人斑の主な構成成分であるアミロイドペプチドの定量例では、吸着回避のために酸及び有機溶媒を含む溶液にて CSF を希釈するだけの簡単な前処理を用いて、イヌ CSF 中 4 種アミロイドβペプチドの同時定量が可能となっている 4)。
このように、ペプチド及びタンパク質の吸着能の相転移現象を利用した PAC-LC は、生体試料中のペプチド及びタンパク質定量において有効なツールに成り得ると考えられる。
おわりに
従来、ペプチド及びタンパク質の定量には、標的に特異的に結合する抗体を用いたリガンド結合法が用いられてきた。しかし、抗体作製に時間を要する上に作製できる保証がないこと、交差性等の問題点が存在し、その定量値の解釈が複雑となる場合が存在する。
一方、LC/MS 法は、m/z と保持時間に基づく高い選択性を有しており、標的を正確に定量するという観点では非常に優れた手法である。ペプチド及びタンパク質は、バイオマーカーとしてだけでなく新しい医薬品モダリティとしてますます期待が高まっており、それに伴い様々な測定技術が必要とされてきている。PAC-LC のような新技術の活用が進み、分析化学がこれらの研究の進展に大きく貢献することを期待したい。
参考文献
- Goda, R. et al. : Biomed. Chromatogr., 22, 81 (2008).
- Goda, R, et al. : Biomed. Chromatogr., 21, 1005 (2007).
- Goda, R, et al. : Biomed. Chromatogr., 22, 857 (2008).
- Goda, R, et al. : J Chromatogr. B., 895, 137 (2012).
- Hashii, N. et al . : Chromatography, 39, 7 (2018).








