ELISA/アッセイキット (糖代謝)
食物中の炭水化物から消化吸収されたグルコース (ブドウ糖) は血液に入り、全身へ運ばれ細胞のエネルギーとなります。糖尿病は生活習慣病の1つで、進行すると動脈硬化や網膜症、腎症、神経障害など様々な合併を引き起こします。当社では糖代謝を制御するインスリンやグルカゴンなどを測定するELISA/アッセイキットを取り扱っております。
学術コンテンツ
Ⅰ.グルコース代謝の基礎と調節機構
グルコースは生体の主要なエネルギー源であり、特に脳や赤血球などの一部の組織では唯一のエネルギー源として重要です。細胞内での代謝を通じてATPを産生し、生命活動の維持を可能としています。通常、血中のグルコース濃度は70 ~ 140 mg/dL で保たれています。これはインスリンをはじめとするホルモンや酵素活性の働き、細胞内シグナル伝達によって恒常性が維持されているためです。血糖調節の中心的ホルモンとして知られているのが血糖値を下げるインスリンと血糖値を上昇させるグルカゴンです。それぞれ膵臓のランゲルハンス島のβ細胞とα細胞から分泌されます。他に血糖値を上げるホルモンとしてアドレナリン、コルチゾール、成長ホルモンが知られています。
Ⅱ.インスリンとグルカゴンの役割とシグナル伝達
インスリンは血糖値を下げる唯一のホルモンとして知られています。その作用機序は、まず食事などによって血中のグルコース濃度が上昇しGLUT (glucose transporter) 2を介して膵臓のランゲルハンス島β細胞内にグルコースが流入します。そこで、解糖系やTCA回路によってATPが産生され、結果として細胞膜の脱分極が起こりカルシウムイオンチャネルを介した細胞内Ca2+濃度が上昇します。この刺激を受け、インスリンを含んだ分泌顆粒がCa2+とともに血中へ分泌されます。全身のさまざまな細胞表面にはIR (Insulin Receptor) が存在し、インスリンがIRと結合することでりん酸化され、さらに別のインスリン受容体基質をりん酸化します。種々のシグナル伝達を経て最終的にGLUT4が細胞膜へ移動し、グルコースの取り込みが行われます。
食後の血糖上昇によって、小腸のL 細胞から分泌されるインクレチン (インスリンの分泌を促すホルモン) であるGLP-1 (Glucagon-like peptide-1) も重要な血糖調節因子です。膵β細胞に高発現しているGタンパク質共役受容体を介してインスリン分泌促進作用を発揮します1)。これまで糖尿病治療や肥満の治療としてGLP-1受容体作動薬が多く開発され、現在ではグルカゴン関連療法としてグルカゴン受容体拮抗薬や抗体、アゴニストの模索が行われています2)。
グルカゴンはインスリン拮抗ホルモンの中で最も重要で、血糖値を上げる作用があります。膵α細胞から分泌され、主に肝細胞を標的とします3,4)。グルカゴンがGCGR (Glucagon receptor) に特異的結合をすることで肝グリコーゲン分解を促進し、血糖値を上昇させます5)。GLP-1、GCGR、GIPR (Glucose-dependent insulinotropic polypeptide receptor) は、エネルギー調節の主要な役割を担い、代謝性疾患の治療標的とされています。これらのいずれかに作用する単一分子アゴニストは例えばGLP-1受容体作動薬のようにすでに治療薬として開発されたものもあります。現在特に注目を集めているのは、これら全てに対する作動薬、つまり三重作動薬の開発で高血糖と肥満の両方のリスクを低減できる可能性があります。こちらも臨床試験段階に入っているものもあります6)。
GLUTファミリーは現在GLUT1 ~ 14の14種同定されています7)。これらは3つのクラスに分類されており、その中で最後に同定されたGLUT12はインスリン感受性グルコース輸送体であるGLUT4との相同性から、ヒト乳がん細胞株MCF7から単離されました8)。GLUT12はGLUT4と同じクラスIII のメンバーで、白色脂肪組織、骨格筋、小腸といったインスリン応答性組織で発現しています。やはりGLUT4と同様にインスリンによって細胞膜への移行が誘導され、細胞内へのグルコースの取り込みを促進します。GLUT12を過剰発現させたマウスにおいて耐糖能の向上やインスリン感受性の向上が見られたことから、第二のインスリン応答性グルコース輸送体としての役割を果たすことが報告されています8)。また、肥満やがんとの関連も示唆され、独特の機能特性を持つと考えていますが、生体での生理的役割は未解明の因子の一つです。
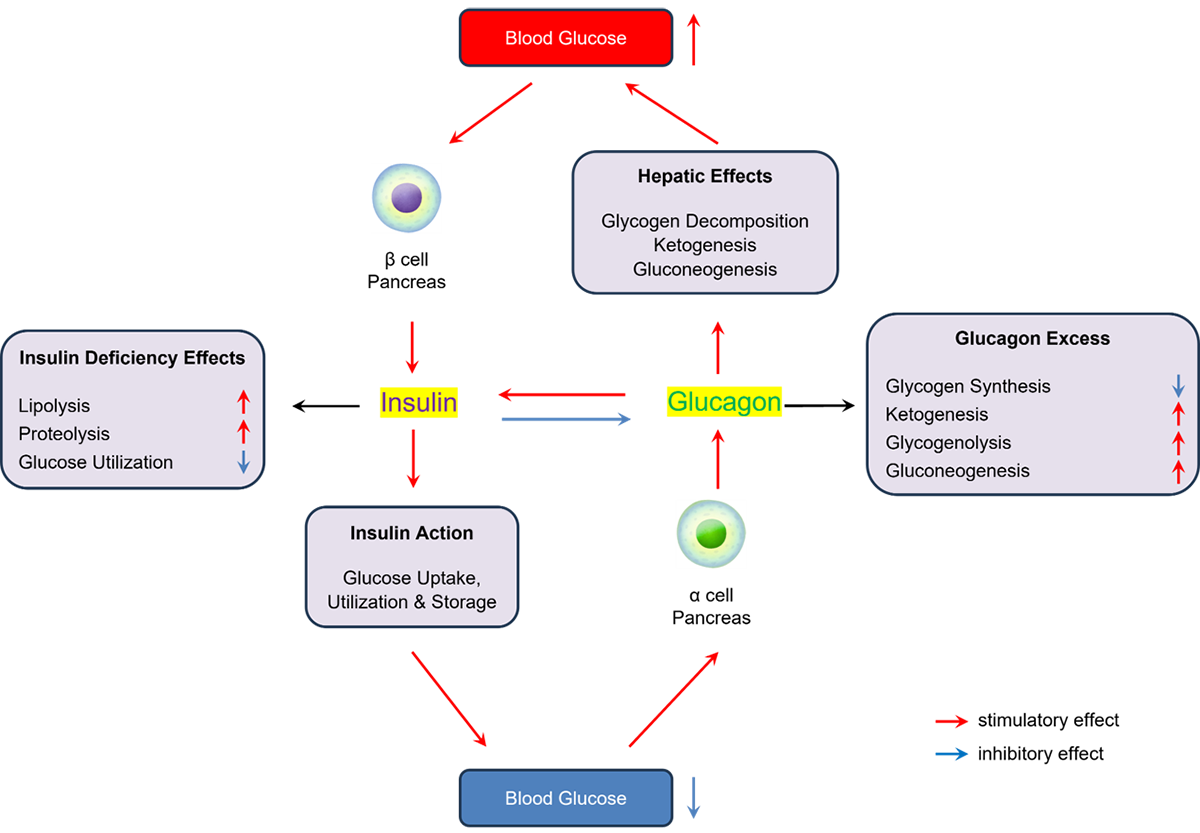
膵島細胞におけるグルコース恒常性のホルモン調節
この概略図はグルカゴンとインスリンの代謝効果を示している。血糖値はインスリンとグルカゴンの分泌に影響を与える。インスリン不足は脂肪分解の亢進、タンパク質分解の増加、グルコース利用の低下を招く一方、過剰なグルカゴンはグリコーゲン合成の低下、ケトン生成の増加、グリコーゲン分解の亢進、糖新生を招く。赤矢印は促進作用、青矢印は抑制作用を示す。
Ⅲ.糖代謝異常がもたらす全身影響 (糖尿病神経障害、糖尿病網膜症、糖尿病腎症)
糖代謝異常、特に慢性的な高血糖状態は、全身の多くの臓器や組織に悪影響を及ぼします。これらの影響は主に糖尿病に関連しており、重大な合併症を引き起こします。三大合併症として糖尿病神経障害、糖尿病網膜症、糖尿病腎症があります。
糖尿病神経障害
高血糖により神経細胞やその支持組織が損傷を受けることで、感覚障害や運動障害、自律神経障害が生じます。血糖による多価アルコール経路の活性化でソルビトールが蓄積し、細胞内浸透圧の異常を引き起こします。酸化ストレスや炎症反応の増加により神経細胞が損傷し、血流障害により神経への酸素・栄養供給が低下することで発症に至ります。臨床症状として手足のしびれ、痛み、感覚鈍麻が知られ、筋力低下や歩行障害を引き起こします。他にも自律神経障害による消化管運動異常や血圧調節障害をもたらします。
糖尿病網膜症
高血糖状態が長期間続くことで網膜の血管に障害が生じ、視力低下や最悪の場合失明に至ることがあります。血管内皮細胞に直接的なダメージを与え、血管の透過性が亢進します。血管壁の肥厚や血液の粘稠度上昇により、網膜の微小血管が閉塞し、酸素不足 (虚血) が生じます。虚血により血管新生因子 (VEGFなど) が過剰に産生され、新生血管が形成されます。これらの新生血管は脆弱で出血しやすく、硝子体出血や網膜剥離を引き起こすことがあります。最終的に血管のバリア機能が破綻し、血漿成分が網膜に漏出することで網膜浮腫を引き起こし、視力障害の原因となります。
糖尿病腎症
糖尿病による腎臓の微小血管障害で、進行すると腎不全に至ることもあります。高血糖が糸球体の基底膜肥厚やメサンギウム細胞の増殖を促進し、糸球体濾過障害や蛋白尿の発生をもたらします。酸化ストレスや炎症、線維化の進行によって発症に至ります。初期症状は無症状ですが、微量アルブミン尿が出現することが知られています。病状が進行すると蛋白尿、腎機能低下、最終的に透析が必要となる疾患です。
Ⅳ.新規糖代謝調節因子と分子標的治療の展望
近年、糖代謝を調節する新規因子の発見が相次ぎ、それらを標的とした分子治療の開発が進展しています。最新の糖代謝調節因子とそれに基づく分子標的治療の展望について解説します。前述したインクレチンの他にSGLT2 (Sodium-glucose transporter 2) 、AMPK (adenosine monophosphate-activated protein kinase) 、ミトコンドリア関連因子などが注目されています。
SGLT2
SGLT2は主にネフロンの近位尿細管に限定され、腎臓のグルコース再吸収能力の約90%に寄与しています9)。SGLT2阻害薬は尿中へのグルコース排出を促進し、血糖値の低下を促しますが、糖尿病治療のみならず心血管死や腎機能悪化を効果的に減少させることが知られており、広い疾患領域での適応が期待されています。
AMPK
AMPKは細胞のエネルギーセンサーとして知られ、細胞内の恒常性調節に不可欠な酵素です。AMPK活性化はGLUT4の細胞膜への移行を促し、グルコース取り込みを促進します10)。また脂肪酸酸化を改善し、インスリン感受性を高めることも知られています11)。
ミトコンドリア関連因子
ミトコンドリア関連因子としてPGC-1α (peroxisome proliferator-activated receptor gamma coactivator 1-alpha) やSIRT1などが知られています。AMPKの活性化によってPGC-1αを直接りん酸化し、ミトコンドリアの合成が促進されます。PGC-1αは長鎖脂肪酸酸化、mtDNA複製、細胞の酸化代謝に関する遺伝子発現の増加させることが知られています12)。一方SIRT1はNAD+依存的脱アセチル化酵素で、PGC-1αとの相互作用が確認されています13)。
参考文献
- Perley, M. J. & Kipnis, D. M. : J Clin Invest ., 46 (12), 1954 (1967).
Plasma Insulin Responses to Oral and Intravenous Glucose: Studies in Normal and Diabetic Subjects* - Jia, Y. et al . : Front Endocrinol (Lausanne) ., 13, 928016 (2022).
Role of Glucagon and Its Receptor in the Pathogenesis of Diabetes - John, H. F. & Willard, O. R. : ENDOCRINOLOGY ., 54 (3), 303 (1954).
THE ACTIVITY OF EXTRACTED PANCREATIC HYPERGLYCEMIC-GLYCOGENOLYTIC FACTOR AFTER COBALTOUS CHLORIDE AND SYNTHALIN A - Vuylsteke, C. A. & de Duve, C. : Archives of Physiology and Biochemistry ., 61 (2), 275 (1953).
[Influence of glucagon on the action of insulin] - Huypens, P. et al . : Diabetologia ., 43 (8), 1012 (2000).
Glucagon receptors on human islet cells contribute to glucose competence of insulin release - Seidelmann, S. B. et al . : Lancet Public Health ., 3 (9), E419 (2018).
Dietary carbohydrate intake and mortality: a prospective cohort study and meta-analysis - Augustin, R. : IUBMB Life ., 62 (5), 315 (2010).
The protein family of glucose transport facilitators: It's not only about glucose after all - Rogers, S. et al . : Am J Physiol Endocrinol Metab ., 282 (3), E733 (2002).
Identification of a novel glucose transporter-like protein—GLUT-12 - Vallon, V. : ANNUAL REVIEW OF MEDICINE , 66, (2015).
The Mechanisms and Therapeutic Potential of SGLT2 Inhibitors in Diabetes Mellitus - Witczak, C. A. et al . : Cell Mol Life Sci ., 65 (23), 3737 (2008).
AMP-activated protein kinase in skeletal muscle: from structure and localization to its role as a master regulator of cellular metabolism - Samuel, V. T. et al . : The Lancet ., 375 (9733), 2267 (2010).
Lipid-induced insulin resistance: unravelling the mechanism - Cheng, CF. et al . : Int J Mol Sci ., 19 (11), 3447 (2018).
PGC-1α as a Pivotal Factor in Lipid and Metabolic Regulation - Ryall, J. G. et al . : Cell Stem Cell ., 17 (6), 651 (2015)
Metabolic Reprogramming of Stem Cell Epigenetics





