エピジェネティクス解析試薬
エピジェネティクスとは、「DNA配列の変化を伴わず、DNAやそれを取り巻くタンパク質の化学修飾により遺伝子発現が制御される生命現象」を指しており、遺伝子発現の多様性やがんなど種々の疾患に深く関与します。DNAメチル化やヒストン修飾(メチル化、アセチル化など)とその機能解析、また創薬研究が盛んに進められています。
当社では、クロマチン免疫沈降(chromatin immunoprecipitation:ChIP)に不可欠な修飾ヒストン抗体(H3K9me、H3K4me等)、ピロールイミダゾールアミドなど、エピジェネティクスの研究試薬を幅広く取り揃えています。
学術コンテンツ
エピジェネティクスとは
ヒトをはじめとする個体は種々の役割を担う多様な細胞集団により構成されています。同一のDNA配列を有する細胞が多様な表現型を示す理由として、遺伝子の発現パターンが細胞種によって大きく異なる点が挙げられます。そしてこの遺伝子発現のパターンはDNAメチル化やヒストン修飾といった化学修飾に基づいて決定されます。このようなDNA配列の変化を伴わない遺伝子発現制御の仕組みをエピジェネティクスといいます。また、このような化学修飾を受けたゲノムを「エピゲノム」といいます。
エピジェネティクスに関連した研究は発生学の領域はもちろん、がん領域のような新たな細胞集団の発生の機構を明らかにする分野においても広く取り組まれています。
エピジェネティックな現象 - 三毛猫の斑模様 -

エピジェネティクスの身近な例として、「三毛猫」が挙げられます。三毛猫は基本的にメスしか存在しません。
哺乳類の性染色体は、オスがXY、メスがXXとなっています。メスの性染色体のうち、片方のX染色体は不活性化されており、どちらが不活性化されるかは細胞によってランダムに決まります。この「X染色体の不活性化」はエピジェネティックな現象です。
猫の毛の色に関する遺伝子は、X染色体上にのみあり、不活性化している部分とそうでない部分があることで斑模様になります。そのため、XX染色体でなければ三毛猫になりません(ただし、XXY染色体を持つオスの三毛猫も例外的に生まれます)。
このように、エピジェネティクスは身近な生命現象に深く関わっています。
DNAメチル化

DNAメチル化は、3’-CG-5’の並びとなる配列(CpG配列)のシトシンにメチル基(-CH3)が付加される現象です。その多くは CpG配列が密に存在する領域(CpGアイランド)のシトシンの5位の炭素(5-メチルシトシン:5-mC)がメチル化されることにより生じます。 DNAのメチル化により、転写因子の染色体上へのリクルートが阻害されます。また、メチル化DNA結合タンパク質(Methyl CpG binding domain(MDB) protein)がリクルートされ、クロマチン構造の凝集を促すことにより、転写が負に制御されます。 このようなDNAメチル化によるエピジェネティックな遺伝子発現制御は、X染色体の不活性化、ゲノムインプリンティング、ゲノム安定性など、生命現象に重要な役割を担っています。
ヒストン修飾
ヒストンとは
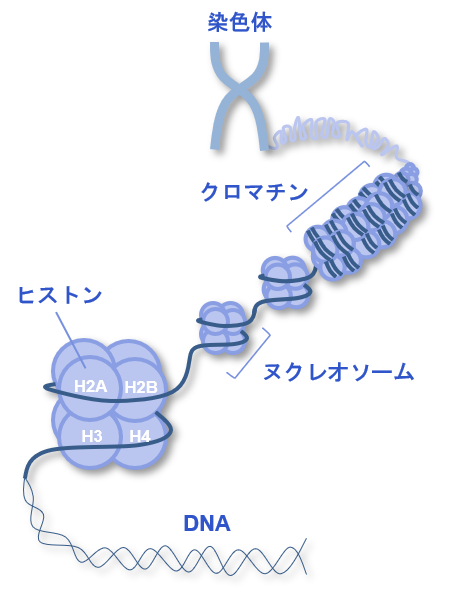
ヒストンは、真核生物の染色体を構成するタンパク質です。塩基性アミノ酸を多く有しており、負に荷電したリン酸基を持つDNAと安定した複合体を形成します。 ヒストンはH1、H2A、H2、H3、H4の5種類が存在します。 H2A、H2、H3、H4を2分子ずつ含む8量体をヒストンコアといい、これにDNAが巻き付いてヌクレオソームが形成されます。このヌクレオソームが数珠状に連なった構造をクロマチンといいます。ヒストンH1は、ヌクレオソーム間のリンカーDNA領域に結合しており、クロマチン高次構造の形成に深く関与していると考えられています。
ヒストンの修飾
ヒストンは、アセチル化やメチル化、リン酸化などの修飾を受け、遺伝子サイレンシング、クロマチン構造変化などを引き起こすことが知られています。ヒストンを修飾する酵素としては、ヒストン脱アセチル化酵素(histonedeacetylase: HDAC)、ヒストンアセチル化酵素(histone acetyl transferase: HAT)、ヒストンメチル化酵素(histonemethyltransferase: HMT)などがあります。その他にも、ユビキチン化、SUMO化など、様々な修飾を受けることが知られています。
ヒストンアセチル化
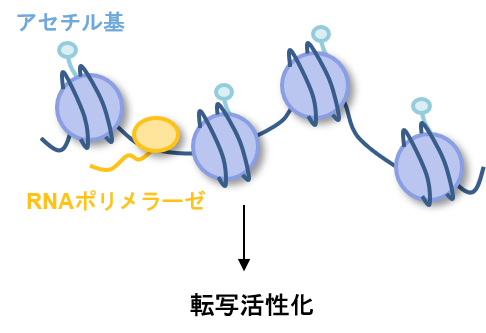
ヒストンのアセチル化は、リジン残基の正電荷を弱めることによって、DNAとヒストンの相互作用を変化させ、クロマチン構造を緩めます。クロマチン構造が緩むことによって、RNAポリメラーゼがアクセスでき、転写が促進されます。 逆に、HDACによりアセチル基が除去されると、DNAとヒストンの相互作用により、転写因子のアクセスが阻害され、転写が抑制されます。
ヒストンメチル化
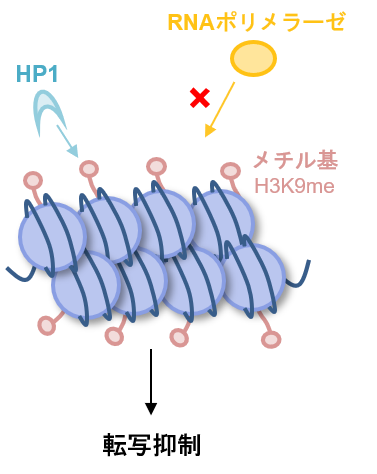
ヒストンのメチル化は、転写の促進、抑制の両方に関与します。ヒストンH3では、4、9、27、36番目のリジン、および2、17、26番目のアルギニン、ヒストンH4では、20番目のリジン、および3番目のアルギニンがメチル化修飾を受けます。
ヒストンH3の9番目のリジンがメチル化(H3K9me)されると、ヘテロクロマチンタンパク質(Heterochromatin Protein1: HP1)が結合し、クロマチン構造が凝縮することによって転写が抑制されます。
一方、ヒストンH3の4番目のリジンがメチル化(H3K4me)されると、転写が促進されます。
このように、ヒストンメチル化は、メチル化状態によって遺伝子発現パターンが変化します。
当社では、クロマチン免疫沈降(chromatin immunoprecipitation:ChIP)に不可欠な修飾ヒストン抗体(H3K9me2、H3K9me3、H3K4me等)、RNAポリメラーゼ抗体(Anti-RNA Polymerase II CTD、Anti-Phospho RNA Polymerase II CTD (Ser2)、Anti-Phospho RNA Polymerase II CTD (Ser5))を各種ラインアップしています。 また、DNA損傷の指標であるγH2AXを二次抗体法で簡便に検出するキットを取り扱っています。
修飾ヒストン抗体一覧(ChIP、ELISA、免疫染色などに使用可能)
ヒストンH3抗体
| ヒストン残基 | 修飾 | clone No. |
|---|---|---|
| H3 | - | MABI0301 |
| H3K4 | me1 | MABI0302 |
| me2 | MABI0303 | |
| me3 | MABI0304 | |
| H3K9 | ac | MABI0305 |
| me1 | MABI0306 | |
| me2 | MABI0307 | |
| MABI0317 | ||
| me3 | MABI0308 | |
| MABI0318 | ||
| H3K9/27 | ac | MABI0310 |
| H3K27 | ac | MABI0309 |
| me1 | MABI0321 | |
| me2 | MABI0324 | |
| me3 | MABI0323 | |
| H3K36 | me1 | MABI0331 |
| me2 | MABI0332 | |
| me3 | MABI0333 | |
| H3S10 | ph | MABI0312 |
| H3S28 | ph | MABI0315 |
ヒストンH2B抗体
| ヒストン残基 | 修飾 | clone No. |
|---|---|---|
| H2BS14 | ph | MABI0251 |
ヒストンH4抗体
| ヒストン残基 | 修飾 | clone No. |
|---|---|---|
| H4 | - | MABI0400 |
| ac(pan-acetyl) | MABI0430 | |
| H4K5 | ac | MABI0405 |
| H4K8 | ac | MABI0408 |
| H4K12 | ac | MABI0412 |
| H4K16 | ac | MABI0416 |
| H4K20 | ac | MABI0420 |
| me1 | MABI0421 | |
| me2 | MABI0422 | |
| me3 | MABI0423 |
RNAポリメラーゼⅡ抗体
| 製品名 | clone No. |
|---|---|
| Anti-RNA Polymerase II CTD | MABI0601 |
| Anti-Phospho RNA Polymerase II CTD (Ser2) | MABI0602 |
| Anti-Phospho RNA Polymerase II CTD (Ser5) | MABI0603 |
エピジェネティクス創薬

上述したように、エピジェネティクスはDNAのメチル化やヒストン修飾など、化学修飾に基づいた遺伝子発現制御に重要であり、生命の恒常性に深く関わっています。 そのため、エピジェネティクスの異常はがんをはじめとする様々な疾患の原因となります。エピジェネティクスの異常に対して行われる創薬アプローチとしては、エピジェネティック制御に関わるタンパク質の阻害薬を創製することになります。
エピジェネティック制御タンパク質は、主にDNAやヒストンのアセチル化・メチル化修飾を行う「書き込み」酵素、これらの修飾を取り除く「消去」酵素、そして遺伝子上に転写因子などを誘導する「読み取り」タンパク質が知られており、これらを制御することによってエピジェネティックな遺伝子発現をコントロールできます。
これまでに、ヒストン脱アセチル化酵素(HDAC)阻害薬やヒストンメチル基転移酵(DNMT)素阻害薬などが、主に血液系のがん(白血病、悪性リンパ腫など)やその他関連疾患の治療薬として承認されています。しかし、エピジェネティクスの異常は、がんだけではなく、HIVや中枢神経系疾患、生活習慣病、炎症性疾患など、様々な疾患に関与しています。そのため、がん以外の疾患を視野に入れたエピジェネティクス創薬が望まれています。
当社では、DNAの塩基配列を認識するピロールイミダゾールポリアミド(PIP)を取り扱っています。PIPにアルキル化剤やHDAC阻害剤をコンジュゲートさせることで、特定領域の遺伝子発現を制御できるため、エピジェネティクス創薬への応用が期待できます。
参考文献
- 杉山 弘:日本白内障学会誌, 29:26〜33(2017).
- GA Holdgate. et al. :Drug Discov Today, 27(4):1088-1098 (2022).
- Shahbazian, M.D. & Grunstein, M, et al.: Annu. Rev. Biochem, 76:75–100 (2007).
- 森信 暁雄: 臨床リウマチ, 20:157-159 (2008)
- 中山潤一: Cell technology 21 (3), 269-273 (2002).
- 有吉 眞理子, 大谷 淳二, 白川 昌宏: YAKUGAKU ZASSHI, 135(1): 3-9 (2015)



