【連載】基礎から応用までよくわかる組織透明化技術 「第3回 CUBIC を用いた組織透明化と3次元観察」
本記事は、和光純薬時報 Vol.87 No.4(2019年10月号)において、東京大学大学院医学系研究科システムズ薬理学教室 洲㟢 悦生様に執筆いただいたものです。

はじめに
今から 100 年以上も前、ドイツの Spalteholz は有機溶剤のベンジルアルコールとサリチル酸メチルを混合した組織透明化試薬を開発し、ヒト組織を3 次元的に観察した例を報告した 1)(これらのサンプルの一部は現在でもドレスデンの公衆衛生博物館で見ることができる)。その後 1980 年代に入るまで、組織透明化技術の目立った発展や応用例は見られなかったが、1989 年に Dent が Murray's clear または BABB 法と呼ばれる改良 Spalteholz 試薬の利用例を報告 2)、さらには 1990 年代以降にロシアの Tuchin ら、台湾の Chiang らが水溶性化合物による組織透明化法を報告し 3, 4)、近代的な組織透明化技術の開発に道を開いた。特に、2007 年の Dodt ら 5)、2011 年の濱ら 6)による蛍光 3 次元イメージングへの適応例が端緒となり、ここ 10 年で数十に及ぶ組織透明化手法が開発されるとともに、主要な組織観察手法の一つとして一般化されつつある。
我々のグループでは 2014 年に CUBIC と名付けた全臓器・全身スケール細胞解析技術のコンセプトを発表し 7, 8)、そのコンセプトを実現する重要な技術要素の一つとして高度な組織透明化手法の開発を継続している。本項ではその詳細とアプリケーション例を紹介したい。
CUBIC 技術のコンセプトと開発経緯
CUBIC (Clear, Unobstructed Brain/Body Imaging Cocktails and Computational Analysis)は、臓器全体、あるいは全身のすべての細胞を観察対象とし、細胞種、細胞機能、細胞同士の接続などの情報をノンバイアスかつ網羅的に収集し解析する技術コンセプトである(図 1)。
細胞解像度の画像データを収集するためには光のモダリティが適切であり、不透明な大型組織サンプルを 3 次元観察するためには組織を光学的に透明にする必要がある。特に、CUBIC が対象とする臓器全体や全身を現実的な時間スケールで光学観察するには、ライトシート顕微鏡と呼ばれる光学切片をサンプル内に作製し 2 次元画像スタックを収集できる特殊な顕微鏡が適している 5)(図 1、「臓器全体の 3D イメージング」部分)。
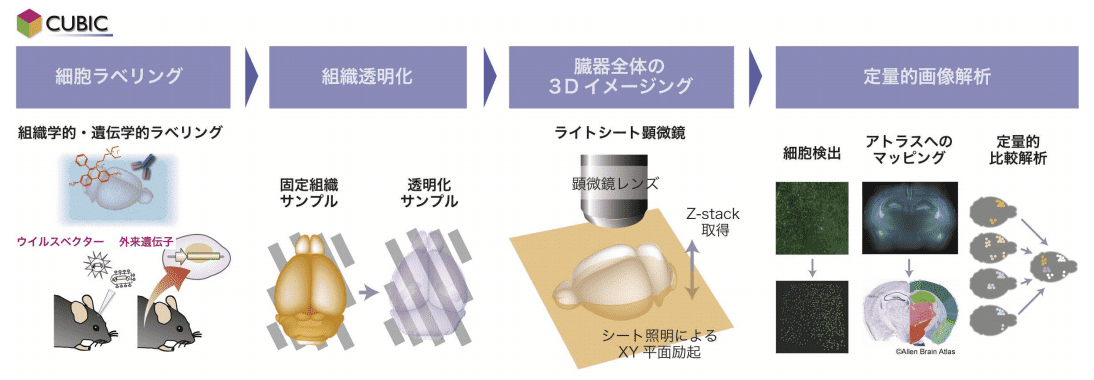
図1.CUBIC の技術コンセプト概略
CUBIC は、臓器全体・全身の網羅的細胞解析を実現する技術コンセプトである。蛍光ラベルを施した組織サンプルを光学的に透明にし、大型サンプル全体を高速に撮像可能なライトシート顕微鏡を用いて細胞解像度の画像取得を行う。取得した画像の定量解析により、細胞種・細胞活動・細胞ネットワーク構造などの情報を抽出する。アトラスの図は Allen Brain Atlas(http://portal.brain-map.org)より使用。しかし、ライトシート顕微鏡は横から励起光を照射し上部から蛍光シグナルを観察するため、サンプル全体が高度に(理想的には文字通り見えないほどに)透明化されている必要がある。当然、観察のための蛍光シグナルは透明化後も残存している必要がある。
これらの仕様要件を満たす組織透明化技術は、筆者らが CUBIC 開発をスタートさせた 2010 年から 2011 年ごろには存在しておらず、新規の技術を開発する必要があった。折しも、理化学研究所の濱・宮脇らのグループが、蛍光タンパク質のシグナル保存に適した水溶性化合物ベースの組織透明化試薬「Scale」を発表したことから 6)、我々は直感に頼らずベストな水溶性化合物を選択するための独自のスクリーニング法を立ち上げ、40 化合物の定量的スクリーニングを行なった。
その結果、最終的に Scale の主要成分である尿素に我々が新規に発見したアミノアルコールを加えた「ScaleCUBIC 試薬」を開発するに至った 7)。さらに我々は、アミノアルコールが組織中の主要な吸光物質であるヘムを除去し、後述する「脱色」の過程で重要な働きをもつことを見出した 8)。これらの特徴により、ScaleCUBIC 試薬はマウス脳、マウス全身、ヒト組織などの高度な透明化と 3 次元観察を可能とした。
その後我々のグループは、マウス全脳全細胞観察のための膨潤透明化法「CUBIC-X」、1600 以上の水溶性化合物をスクリーニングし成分を刷新した「第二世代 CUBIC 試薬(CUBIC-L/R ほか)」、マウス全脳解析基盤としての 1 細胞解像度アトラス「CUBIC-Atlas」などの要素技術を発表した 9-11)(表 1)。
さらに現在では、高度な 3 次元染色プロトコル、マウス全脳 1 細胞解析基盤、高速全細胞観察顕微鏡などの最新の要素技術についても発表準備中である。CUBIC 技術の利用を検討されているユーザーの方々には、これらの最新の開発成果もフォローいただきたい。
表1.CUBIC 試薬一覧
第 2 世代試薬は Scale の主成分である尿素を使用していないため、「CUBIC- 〇〇」の表記に統一した。
| 試薬の世代 | 役割 | 主要な成分 | 文献 | |
|---|---|---|---|---|
| ScaleCUBIC-1 | 第 1 世代 | 脱脂・脱色 | アミノアルコール(クアドロール)、尿素、Triton X-100 | 13) |
| ScaleCUBIC-1A | 第 1 世代 | 脱脂・脱色 | アミノアルコール(クアドロール)、尿素、Triton X-100 | http://cubic.riken.jp/ |
| ScaleCUBIC-2 | 第 1 世代 | 屈折率調整 | アミノアルコール(トリエタノールアミン)、尿素、スクロース | 13) |
| CUBIC-X | 第 1 世代 | 膨潤+屈折率調整 | アンチピリン、イミダゾール | 9) |
| CUBIC-L | 第 2 世代 | 脱脂・脱色 | アミノアルコール(N-ブチルジエタノールアミン)、Triton X-100 | 11) |
| CUBIC-P | 第 2 世代 | 脱色 | 1- メチルイミダゾール、アミノアルコール(N-ブチルジエタノールアミン)、Triton X-100 | 11) |
| CUBIC-B | 第 2 世代 | 骨脱灰 | EDTA、イミダゾール | 11) |
| CUBIC-HL | 第 2 世代 | 脱脂・脱色(一部のヒト組織) | 1,3- ビス(アミノメチル)シクロヘキサン、ドデシルベンゼンスルホン酸ナトリウム | 11) |
| CUBIC-R | 第 2 世代 | 屈折率調整 | アンチピリン、ニコチンアミドまたはN-メチルニコチンアミド | 11) |
CUBIC による組織透明化
物体が光学的に透明であるということは、入射した光が内部で散乱・吸収されずにほぼ直進して射出されるということである。組織が不透明であるのは、組織中のさまざまな成分が光学的に不均一で入射光が強く散乱されるからであり、また血液のヘムのように可視光を強く吸収する色素が含まれているからである。
このため、組織透明化は 1)組織中の光散乱・光吸収物質の除去、2)組織成分と周囲の溶媒成分の光学的特性(特に屈折率)の均一化、の 2 つのステップによって達成される。CUBIC 試薬では界面活性剤(Triton X-100)とアミノアルコールが 1)のステップに重要である。また、2)のステップにおいては、ScaleCUBIC試薬ではスクロースが、第二世代 CUBIC 試薬ではアンチピリンとニコチンアミド誘導体が重要である。
屈折率調整剤はタンパク質などの生体物質の屈折率に近い 1.5 前後の高い屈折率を持っており、「透明化」はこの屈折率調整剤への置換を以て完了する。しかしながら、ScaleCUBIC-1 試薬でもアミノアルコールと尿素の組み合わせにより比較的高い屈折率(1.43)が達成されており、単剤でも比較的明瞭な透明化が達成されるため、全く透明化手法に馴染みのないユーザーや、小型のサンプルを短時間で透明化し、共焦点顕微鏡や 2 光子顕微鏡で観察したいユーザーがはじめにトライする試薬として推奨できる。
より高度な透明化には脱脂・脱色剤+屈折率調整剤の 2 ステップによる透明化を推奨する。また骨組織についてはさらに脱灰も必要である。我々は 1600 以上の大規模化合物スクリーニングを実施するにあたって脱灰化合物も探索対象とし、EDTAにイミダゾールを加えた脱灰試薬(CUBIC-B)を報告している。ヒトを含む霊長類組織はげっ歯類組織より脱脂の難易度が高いため、同じく大規模スクリーニングによりさらに高い脱脂能を達成した試薬(CUBIC-HL)も開発した 11)。
CUBIC 試薬は多くの蛍光タンパク質(GFP バリアント、mCherry、tdTomato、mKate2 など)の保存性に優れるが、発現量が非常に少ない場合は十分なシグナルが得られないこともある。また、一部の蛍光タンパク質とは相性が悪い。このため、実サンプルを用いて蛍光シグナルの残存を評価することを推奨する。
サンプルを最小限のサイズにして処理時間を短くするとともに、脱脂を 37℃ではなく室温で行うと蛍光シグナルの改善が見られる。また、ScaleCUBIC-1 試薬の蛍光シグナル保存性をさらに高めた ScaleCUBIC-1A(Reagent-1A)試薬のレシピも公表している(http://cubic.riken.jp/)。最新の CUBIC-L 試薬と合わせてご検討いただきたい。
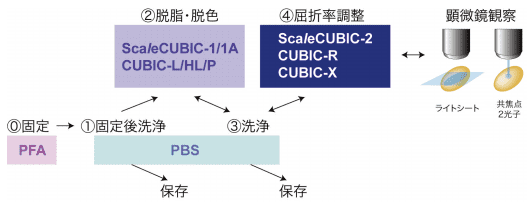
図2.CUBIC を用いた組織透明化・イメージングの流れ
CUBIC 試薬はパラホルムアルデヒド(PFA)固定組織に最適化されている。固定組織は脱脂・脱色をへて屈折率調整により透明化される。間の洗浄過程でサンプルの保存が可能である。試薬の詳細については表1を参照。組織透明化過程の概略を図 2 にまとめた。組織透明化は固定組織サンプルに適応される手法であり、プロトコルに応じた固定法を選択する必要がある。
CUBIC では通常 4% パラホルムアルデヒド固定を推奨する。固定剤の pH は中性を保ち、固定温度、架橋時間は原則的にサンプル間で条件が揃うようにする。脱脂・脱色期間はサンプルによって異なるため、推奨プロトコルに実施例のない組織については条件検討が必要である。
脱脂・脱色後のサンプルはスポンジ状になるため、サンプルのダメージを避ける操作が必要である。筆者らは薬さじにサンプルを乗せてハンドリングしている。また、この段階のサンプルは防腐剤を入れた PBS などで長期保存が可能である。
屈折率調整剤は非常に高濃度の試薬であるため、先に蒸留水で 50% に希釈した試薬で 1 日以上置換したのち、100% の試薬に置換する。希釈した屈折率調整剤の処理時間が不十分だと、内部の透明化が達成されない、組織の変形が起こるなどのトラブルが起こりうる。観察後の組織は PBS で洗浄することで、脱脂・脱色後のサンプルと同等に保存することが可能である。
CUBIC のアプリケーション例
医学生物学研究における組織透明化技術の使用例は年々急速に拡大しており、文献を検索すればさまざまな生物種や組織への適応例を見つけることができる。例えば"CUBIC tissue clearing"で google scholar を検索すると 8000 件余りがヒットし、対象サンプルも幅広い。中にはダンゴムシ・カニなどの甲殻類への適用例 12)など、筆者らが想定していなかったようなアプリケーション例も散見される。
このため、利用を検討しているユーザーには、まず文献などを検索し適用例を探していただくのがスムーズな導入の一助になると思われる。ここでは特に筆者らのグループから報告した CUBIC の適応例について報告する。
上述のように、CUBIC は「臓器全体・全身の網羅的細胞解析」をコンセプトとしており、最初の論文 7, 13)にて、まず光刺激ありなしの 2 個体 2 条件によるマウス全脳神経活動比較解析の例を報告している(図 3A)。その後サンプル数を拡張し、薬物投与下マウスを時系列サンプリングし全脳神経活動を解析した例も報告している 14)。この例では計 8 条件で 20 匹のマウス脳を使用し、最終的にマイクロアレイ 解析などで汎用されるクラスタリング解析を行なって、特定の時間帯・実験条件で特異的に活動している神経細胞群を同定することに成功した。興味のある方は原著論文を参照いただきたい。
さらに、第二世代 CUBIC 試薬を用いて高度にマウス全身を透明化し、がん転移モデルマウスの全身解析を行なった例についても報告している 10)。この例では全身の 3 次元イメージングデータから、臓器中に散見される微小転移巣ももれなく検出できることを示し(図 3B)、CUBIC による全身解析アプローチの有用性を証明した。
CUBIC は核染色や免疫染色などの組織学的手法にもコンパチブルであり、一部の抗体については脳や消化管、腎臓などの臓器を丸ごと染色しイメージングできることを報告している 8, 10, 15)(図 3C)。また、ヒト組織についても透明化や免疫染色、パラフィン包埋法とのコンパチビリティを検討し、3 次元病理学の例として大腸癌リンパ節転移の検出率を 100% まで向上させることができることを報告している 16)。
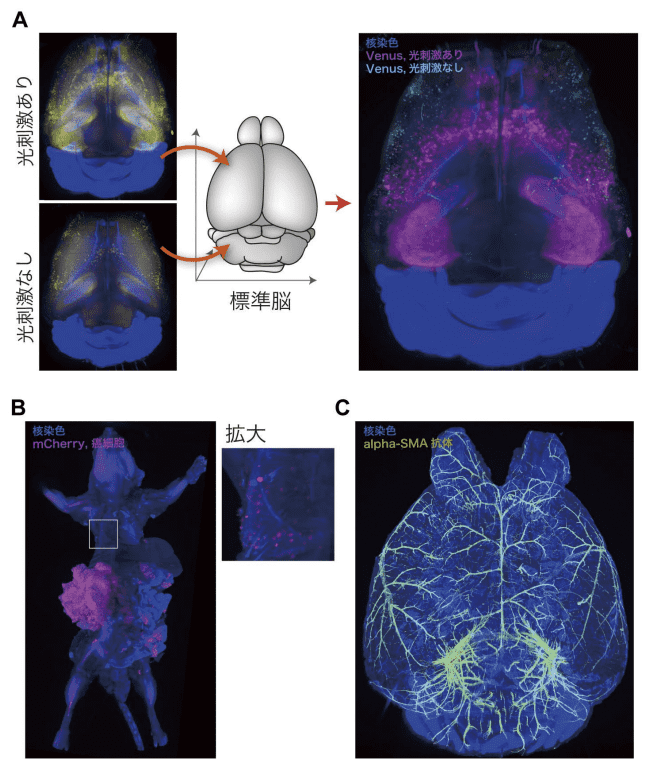
図3.CUBIC を用いたアプリケーション例
A:神経活動を蛍光タンパク質 Venus の発現でラベリングできるトランスジェニックマウス(Arc-dVenus Tg)19)に光刺激を与えたのちサンプリングを行い、光刺激なしのコントロールと比較する実験を行なった。標準脳データに双方のデータをレジストレーションし標準化を行なったのち、重ね合わせ画像を作成して直接比較を行なった。データは文献 13)より改変して使用。B:がん転移モデルマウスの全身を透明化・3D イメージングした例。mCherry でラベルされた癌細胞の微小転移も漏らさず検出可能である。データは文献 10)より改変して使用。
C:マウス全脳免疫染色の例。血管平滑筋をラベリングするα-Smooth Muscle Actin(SMA)抗体で脳全体を染色後、透明化・3D イメージングを行なった。データは文献 10)より改変して使用。
3 次元の抗体染色を実施するにあたっては、抗体のシグナルノイズ比が高く染色性が良好なモノクローナル抗体を使用することが望ましい。筆者らは脱脂・脱色後の組織で凍結切片を作製し、抗体の動作確認を行なっている。
また、3 次元浸透の行程を繰り返さないように、1 次抗体に直接蛍光物質をラベリングした抗体を使用することを推奨する。抗体によっては屈折率調整剤中ではがれるものもあるため、染色後に 1% 程度の PFA で後固定を行うとよい。ただし、固定が強すぎると透明化が阻害されるため、抗体シグナルが残存する必要最小限の条件で実施することが望ましい。
現在まで発表済みのプロトコルでは抗体の深部浸透の問題が完全に解決しておらず、筆者らはこの点を大きく改善させた最新のプロトコルを発表準備中である。興味のあるユーザーは今後の論文発表をフォローいただきたい。
おわりに
より詳しい情報が必要なユーザー向けに、透明化・3 次元イメージングに関する英文総説を発表しているのでご参照いただきたい 17, 18)。組織透明化技術は優れたプロトコルが複数発表されており、ユーザーは目的に応じて最適なプロトコルを選択することができる状況にある。ただし、当研究チームも含め、開発グループの多くはなお技術を向上させており、最初の論文だけでなく最新の文献をフォローすることを推奨する。
CUBIC に関する技術的な質問は筆者(esusaki@m.u-tokyo.ac.jp)までお問い合わせいただければ随時お答えする。本項が組織透明化技術を自身の研究へ活用しようと考えているユーザー各位の参考となれば幸いである。
参考文献
- Spalteholz, W. : "Über das Durchsichtigmachen von menschlichen und tierischen Präparaten.", S. Hirzel, Leipzig (1914).
- Dent, J. A., Polson, A. G. and Klymkowsky, M. W. : "A whole-mount immunocytochemical analysis of the expression of the intermediate filament protein vimentin in Xenopus.", Development, 105, 61 (1989).
- Tuchin, V. V. et al. : Proc. SPIE, 3863, 10 (1999).
- Liu, Y.-C. and Chiang, A.-S. : "High-resolution confocal imaging and three-dimensional rendering.", Methods, 30, 86 (2003). DOI: 10.1016/s1046-2023(03)00010-0
- Dodt, H. U. et al. : "Ultramicroscopy: Three-dimensional visualization of neuronal networks in the whole mouse brain.", Nat. Methods, 4, 331 (2007). DOI: 10.1038/nmeth1036
- Hama, H. et al. : "Scale: a chemical approach for fluorescence imaging and reconstruction of transparent mouse brain.", Nat. Neurosci., 14, 1481 (2011). DOI: 10.1038/nn.2928
- Susaki, E. A. et al. : "Whole-brain imaging with single-cell resolution using chemical cocktails and computational analysis.", Cell, 157, 726 (2014). DOI: 10.1016/j.cell.2014.03.042
- Tainaka, K. et al . : "Whole-body imaging with single-cell resolution by tissue decolorization.", Cell, 159, 911 (2014). DOI: 10.1016/j.cell.2014.10.034
- Murakami, T. C. et al. : "A three-dimensional single-cell-resolution whole-brain atlas using CUBIC-X expansion microscopy and tissue clearing.", Nat. Neurosci., 21, 625 (2018). DOI: 10.1038/s41593-018-0109-1
- Kubota, S. I. et al. : "Whole-body profiling of cancer metastasis with single-cell resolution.", Cell Rep., 20, 236 (2017). DOI: 10.1016/j.celrep.2017.06.010
- Tainaka, K. et al. : "Chemical Landscape for Tissue Clearing based on Hydrophilic Reagents.", Cell Rep., 24, 2196 (2018). DOI: 10.1016/j.celrep.2018.07.056
- Konno, A. and Okazaki, S. : "Aqueous-based tissue clearing in crustaceans.", Zoological Lett., 4, 13 (2018). DOI: 10.1186/s40851-018-0099-6
- Susaki, E. A. et al . : "Advanced CUBIC protocols for whole-brain and whole-body clearing and imaging.", Nat. Protoc., 10, 1709 (2015). DOI: 10.1038/nprot.2015.085
- Tatsuki, F. et al. : "Involvement of Ca2+- Dependent Hyperpolarization in Sleep Duration in Mammals.", Neuron, 90, 70 (2016). DOI: 10.1016/j.neuron.2016.02.032
- Hasegawa, S. et al. : "Comprehensive three-dimensional analysis (CUBIC-kidney) visualizes abnormal renal sympathetic nerves after ischemia/reperfusion injury.", Kidney Int., 96, 129 (2019). DOI: 10.1016/j.kint.2019.02.011
- Nojima, S. et al. : "CUBIC pathology: three-dimensional imaging for pathological diagnosis.", Sci. Rep., 7, 9269 (2017). DOI: 10.1038/s41598-017-09117-0
- Tainaka, K. et al. : "Chemical Principles in Tissue Clearing and Staining Protocols for Whole-Body Cell Profiling.", Annu. Rev. Cell Dev. Biol., 32, 713 (2016). DOI: 10.1146/annurev-cellbio-111315-125001
- Susaki, E. A. and Ueda, H. R. : "Whole-body and Whole-Organ Clearing and Imaging Techniques with Single-Cell Resolution: Toward Organism-Level Systems Biology in Mammals.", Cell Chem. Biol., 23, 137 (2016). DOI: 10.1016/j.chembiol.2015.11.009
- Eguchi, M. and Yamaguchi, S. : "In vivo and in vitro visualization of gene expression dynamics over extensive areas of the brain.", Neuroimage, 44, 1274 (2009). DOI: 10.1016/j.neuroimage.2008.10.046









