【連載】エクソソームと生命現象「第 4 回 エクソソーム糖鎖プロファイリングのススメ」
本記事は、和光純薬時報 Vol.87 No.1(2019年1月号)において、慶應義塾大学 医学部医化学 松田 厚志 様に執筆いただいたものです。
細胞が分泌する細胞外小胞の中でも、粒形100 nm前後の小胞はエクソソームと呼ばれ、固有のタンパク質やmicroRNAなどを内包している。さらに、その表層には脂質や糖タンパク質などが存在することから、血中循環腫瘍細胞や血中循環DNAに次ぐ第三のリキッドバイオプシー標的として注目されており、現在、microRNA、プロテオーム解析を中心に世界的な開発競争が展開されている。エクソソームの最外殻は細胞と同様、糖鎖で覆われており、糖鎖はエクソソームマーカー開発における格好のターゲットになる。臨床上利用されている腫瘍マーカーは糖鎖構造の違いを認識するものが多く、疾患特異的なエクソソーム上の糖鎖変化を捉えることができれば、有用なバイオマーカー開発につながるものと期待される。
タンパク質はほとんどが糖鎖をはじめとする様々な翻訳後修飾を受け機能性タンパク質として働く。ゲノム、タンパク質に次ぐ第三の生命鎖と呼ばれる糖鎖は細胞増殖、分化、細胞応答など様々な生命現象に関与すると考えられている。また、がん、免疫、感染症、アルツハイマー病など糖鎖が関わっているとされる疾患は数多く、特にがんでは、がんの転移、浸潤、増殖などでその重要性が明らかにされている。がんの診断・治療法の開発において、糖鎖研究への期待度は高く、糖鎖の分子生物学的意義を明らかにすることは重要課題の一つである。
糖鎖は一筆書きの核酸やアミノ酸配列と比べて、枝分かれや異なる結合様式(α, β-結合)の多様性が存在し、核酸のように増幅ができず、タンパク質のような有用なプローブ(抗体)が限られていることもその解析をより一層困難なものにさせる。しかし昨今の質量分析、マイクロアレイ基盤技術を中心とした糖鎖解析技術の革新は目覚ましく、これまでに新たな糖鎖腫瘍マーカーおよび開発アプローチ例も数多く報告されている。
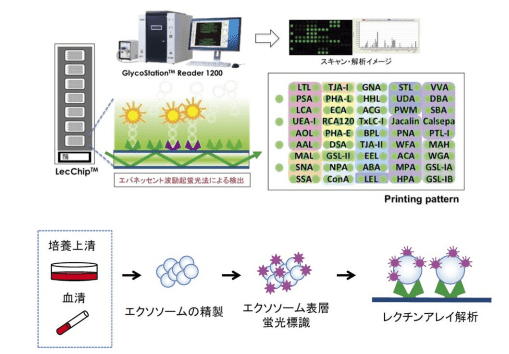
図1.レクチンマイクロアレイシステムとエクソソーム糖鎖プロファイリングの流れ
これら技術革新によって糖鎖は敷居の高い研究分野から、誰もが気軽に糖鎖解析を行える時代になった。これまでに筆者らは、糖鎖を構造特異的に認識し結合するタンパク質、レクチンを数十種類固相化したレクチンマイクロアレイシステムを活用し1)、各種糖鎖バイオマーカー開発を推し進めてきた2, 3)。本法最大の利点は、質量分析による解析に比べて感度・スループットの面で秀でていることである(図1)。
これまで、本システム応用の一環として、様々な生体試料からの解析を可能とするプロトコル開発を実施してきた結果、現在、体液、組織、細胞などレクチンアレイ解析の対象は多岐にわたる。粒子状のエクソソームは、細胞に比べてその粒形こそ小さくはあるが、その表面には無数の糖タンパク質、糖脂質糖鎖が存在する。よって格好のレクチンアレイ解析対象となる。
レクチンアレイ解析は数十種類のレクチン結合パターンから糖鎖構造を推定し、比較対象と差異のある糖鎖(レクチン)パターンを見出す。これを糖鎖プロファイリングと呼ぶ。我々が採用するエクソソーム解析プロトコルでは、精製したエクソソーム粒子上タンパク質を蛍光標識する。
そのため粒子形状を保ったままエクソソームを回収することが重要となる。また、レクチンマイクロアレイは高感度であるため回収量はそれほどなくても解析は可能であるが、他の糖タンパク質が混入するとそれがノイズとなるため正確なエクソソーム糖鎖プロファイリングに支障をきたす。よって精製エクソソームの純度も要求される。エクソソームの精製は高純度にかつ粒子状態を保ったまま回収可能なMagCapture™ Exosome Isolation Kit PS (以後MagCapture) を使用した。本Kitの使用は、特に後述する血中エクソソーム糖鎖解析の際に抜群の効力を発揮する。
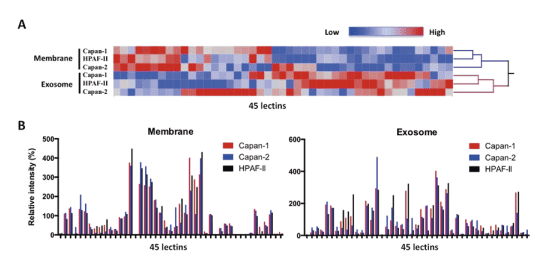
図2.膵臓がん細胞由来エクソソームと細胞膜糖タンパク質の比較糖鎖プロファイリング
(A) 階層型クラスター解析によるクラスタリング(B) 各細胞株由来細胞膜タンパク質、エクソソーム表層糖鎖のレクチンアレイ結合パターン
まず我々は培養細胞をモデルとして培養上清からエクソソームを単離・精製しレクチンマイクロアレイによる比較糖鎖プロファイリングを試みた。比較対象として、同一細胞株のペレットから細胞膜タンパク質を精製し、そのタンパク質上糖鎖プロファイルと比較した(図2)。
3種の膵臓がん細胞株(Capan-1,-2, HPAF-Ⅱ)から得られたレクチンアレイデータから、階層型クラスター解析を実施すると、これらプロファイルは株間ではなく、膜タンパク質・エクソソーム間で見事に分かれた(図2A)。
つまり、たとえ同じ細胞株であっても細胞膜タンパク質上糖鎖と分泌されるエクソソーム上糖鎖はその構造は異なることを示している。また同じエクソソームでもその詳細な糖鎖プロファイルは異なることから(図2B)、エクソソームを標的とした比較糖鎖プロファイリングが可能であることが示された。
培養上清をモデルとしたエクソソーム解析にはある程度目処がたった。血清での比較解析を実施する場合、夾雑する糖タンパク質が多量に含まれるためより慎重を期する。つまり、血中エクソソーム糖鎖解析には高純度にエクソソームを精製することが重要となる。
血清エクソソーム精製法として超遠心法やポリマー沈殿法、MagCaptureを使用した際の糖鎖プロファイリング法を比較した。超遠心法やポリマー沈殿法で精製した場合、健常者とがん患者間で糖鎖プロファイルに差は認められなかった。その要因として、本法にて精製したエクソソーム画分を電気泳動で確認すると、過剰なグロブリンタンパク質をはじめとする血清糖タンパク質のバンドが確認され、比較糖鎖プロファイリングに支障をきたしており、血清エクソソーム糖鎖解析にはエクソソームを高純度に精製可能なMagCaptureが最適なKitであることが判明した。
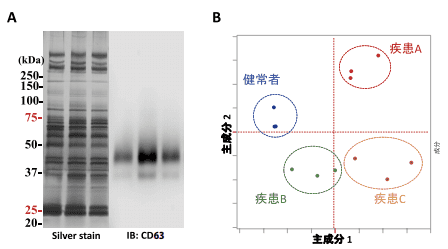
図3.血清エクソソームの比較糖鎖プロファイリング
(A) 各プール血清からの精製エクソソームの銀染色と抗CD63抗体ウエスタンブロット(B) レクチンアレイ解析データを用いた主成分解析
最終的にMagCaptureをエクソソーム精製に使用するKitとしたプロトコルにより、レクチンアレイ解析に必要な量として、血清量換算すると数 µLに相当するエクソソーム量があれば検出可能な高感度血中エクソソーム比較糖鎖解析プロトコルを確立した。本Kitはエクソソームを粒子状態が保たれたまま回収可能なことも心強い。本プロトコルに従い、実際に健常者・疾患群(A, B, C)プール血清中エクソソームの比較糖鎖プロファイリングを実施した。主成分解析の結果、これら血清エクソソーム表層糖鎖プロファイルは疾患ごとに異なることが示され(図3)、エクソソーム糖鎖が新たなエクソソーム診断ターゲットとなる可能性が示唆された。
現在臨床応用を念頭に糖鎖エクソソームマーカーの開発を試みている。ゲノム・プロテオーム解析を中心にエクソソームの本質が徐々に明らかにされつつある。近年、革新的な血中エクソソーム測定法の開発により、エクソソームの定量的計測が可能となりはじめている。臨床応用へ向けたイメージも尚一層つくようになった。疾患特異的エクソソーム糖鎖が見出せれば、このような革新的エクソソーム定量デバイスに応用し、より実践的マーカーの開発につながるものと期待される。他のオミクス解析との融合や、見出した特異的糖鎖のバリデーション法など改良を重ねる余地は多分にあるが、エクソソーム糖鎖マーカー開発へ向けた第一歩は踏み込めた。
参考文献
- Kuno, A. et al. : Nat. Methods, 2, 851 (2005). DOI: 10.1038/nmeth803
- Matsuda, A. et al. : Hepatology, 52, 174 (2010). DOI: 10.1002/hep.23654
- Matsuda, A. et al. : Anal. Chem., 87, 7274 (2015). DOI: 10.1021/acs.analchem.5b01329
- Yoshioka, Y. et al. : Nat. Commun., 5, 3591 (2014). DOI: 10.1038/ncomms4591
- Kabe, Y. et al. : Clin. Chem., 64, 1463 (2018). DOI: 10.1373/clinchem.2018.291963















