【連載】エクソソームと生命現象「第 2 回 エクソソームのプロテオーム解析」
本記事は、和光純薬時報 Vol.86 No.3(2018年7月号)において、公益財団法人がん研究会 植田 幸嗣 様に執筆いただいたものです。
微小分泌小胞の一種であるエクソソームは細胞内小胞輸送に由来する産物の一つであり、不要な分子を細胞外に放出したり、内包する分子を遠隔細胞に輸送、伝達する働きがあるとされる。一般的には直径数十~百ナノメートルほどの脂質二重膜構造を持ち、特定のタンパク質群(テトラスパニンファミリー、Rab ファミリー、Tsg101、Alix など)や miRNA が細胞内構成比率と比して特に多く含まれるものとされる。
ただし、粒子径を細かく分類してオミクス解析を行うと特定の粒子径依存的に分子構成が顕著に異なるとする研究結果が発表されるなど 1)、いまだエクソソームの分子生物学的定義は明確に定まっていない。実際に、様々な異なるエクソソーム精製法を用いた機能解析実験に基づいて(つまり精製純度の異なるエクソソームサンプルを用いて)、がんの転移、浸潤、血管新生、免疫細胞制御といった現象への関与が多数報告されている。
一方で、「病因細胞が持つ分子プロファイルを末梢血など体液中に放出された病因細胞由来エクソソームから読み取れること」は事実であり、すでに診断を目的としたエクソソームの利用は商業化が進んでいる。例えば、前立腺がん特異的な RNA 三種 PCA3 non-coding RNA、ERG mRNA、SPDEF mRNA を同時に尿中エクソソームから検出するテスト(ExoDx® Prostate IntelliScore)が CLIA(Clinical Laboratory Improvement Amendments)ラボのもとで開発されており、LDT(Laboratory Developed Tests:一つの試験検査施設内で設計・製造・使用される体外診断試験)として国際的な委託検査発注が可能となっている 2)。
また、同社は血漿からエクソソーム DNA/RNA、cfDNA(circulating free DNA)をワンステップで単離する技術を構築し、血液サンプルから非小細胞肺がんが持つ EGFR-T790M 変異を検出するテストも発表している(ExoDx® EGFR T790M)。同変異は EGFR 阻害薬の治療を行った肺がん患者の 6 割が獲得する薬剤耐性の原因であり、オシメルチニブなど同変異 EGFR にも有効な薬剤への切り替えを判断するために迅速な耐性獲得診断が重要とされる。
210 例の同変異保持肺がん患者に対する比較試験によると、すでに承認されている cfDNA を用いた診断法(cobas® EGFR Mutation Test v2)では T790M 検出の感度、特異度が 58%、80% だったのに対し、ExoDx® EGFR T790M テストではそれぞれ 92%、89% とより良好な診断結果が得られたと報告されている 3)。
こうした背景から、基礎生物学研究、臨床応用のいずれにおいてもエクソソームを高純度に、施設間差なく高い再現性を持って、誰でも簡便に単離精製可能なツールは不可欠なパーツと言える。特に、血清や血漿といったサンプルから精製したエクソソームのタンパク質を対象とした研究においては非常に高いレベルの精製効率が求められる。
血清・血漿は 60 mg/ml を超えるタンパク質濃度を持ち、リポタンパク質など高分子量複合体も多く存在するため、一般的にエクソソーム精製法として用いられる超遠心沈降法を用いてもなお多量の血清中のフリータンパク質(IgM、α2-マクログロブリン、補体成分など)やリポタンパク質が共存する。したがって超遠心沈降法によって精製した血清タンパク質を LC/MS による網羅的定量プロテオーム解析に供すると、含有量の上位をほぼ全て血清中フリータンパク質が占め、エクソソーム由来タンパク質はわずかしか検出されない 4)。
超遠心法以外にも抗体を用いたアフィニティー精製法やポリマー沈殿法、ゲル濾過法、切除組織浸漬液から直接回収する方法 5)、など様々なエクソソーム精製法が使用されているが、MagCapture™ Exosome Isolation Kit PS(以後 MagCapture キット)はエクソソーム膜を構成する脂質の一つであるフォスファチジルセリン(PS)を標的としたアフィニティー精製を原理としており、他と比べて様々な利点を持つ。
マグネットビーズに固相化された Tim-4 タンパク質と PS 間の結合はカルシウムイオン要求性であり、キレート剤を用いて溶出することにより非特異的なビーズ結合タンパク質を溶出させることなくエクソソームを特異的に溶出できるため精製純度が高い。また、マグネットビーズによる精製操作が支障なく行える範囲であればサンプルの容量に制限がないのも希薄な試料を用いる際に有効である。さらに変性溶解を伴わずに溶出を行うため、粒子数計測、検鏡、細胞投与実験などその後のアプリケーションを問わず使用できる特徴もある。
実際に同一の血清から図 1A に従ってエクソソームを精製、Orbitrap Fusion Lumos 質量分析計により網羅的なプロテオーム解析を行った結果を示す。総タンパク質同定数は超遠心精製エクソソームから 612 種、MagCapture キット精製エクソソームから 1,103 種となり、後者の方が約 1.8 倍も多くの同定数を得ることができた(図 1B)。
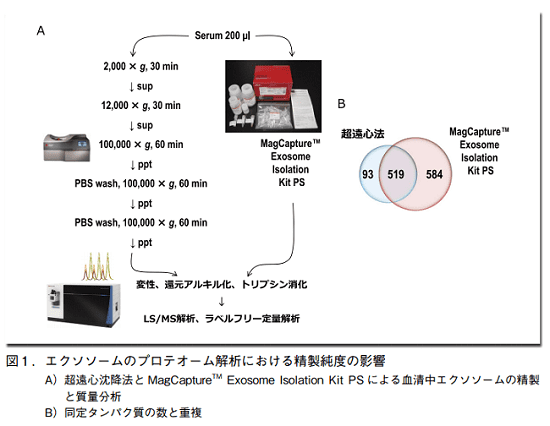
これは前者において血清中に存在する多量のフリータンパク質の残存が多く、それらが微量なエクソソーム由来シグナルをマスクしてしまった結果である。また、同定タンパク質を相対定量値と共に俯瞰してみると、エクソソームマーカータンパク質とされる分子群の同定数、そして相対含有量ともに MagCapture キット精製エクソソームの方が多いことが分かる(図 2)。このことからも同キットから得られたエクソソームの純度が既存の超遠心沈降法に比べて非常に高いと言える。
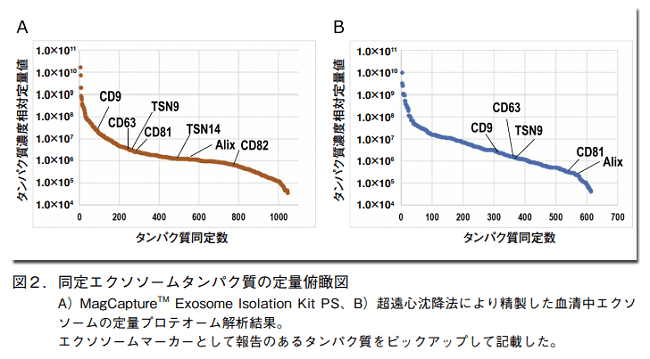
精製度の高いエクソソームを使用することは、エクソソームの機能を解明する上でも、診断・治療薬のターゲットを探索する上でも大変有利で信頼性も高いことは言うまでもない。この点において MagCapture キットは精製度、汎用性、再現性などの面からあらゆるエクソソーム研究の起点となりうる性能を持っている。
ただし、同キットで回収した産物もまた、PS リッチな膜成分を持つサイズ非依存的な構造体の集合であって、他の既存研究が指すエクソソームと同等のものかどうかはこれからのオミクス解析によって慎重に評価、定義していかなければならない。
MagCapture キットをはじめとした精製技術、そしてそれらを検出する技術の発展に伴って、エクソソームの本態解明と臨床利用がさらに進展することを期待している。
参考文献
- Zhang, H. et al. :"Identification of distinct nanoparticles and subsets of extracellular vesicles by asymmetric flow field-flow fractionation", Nat. Cell Biol., 20, 332 (2018). DOI: 10.1038/s41556-018-0040-4
- McKiernan, J. et al . :"A Novel Urine Exosome Gene Expression Assay to Predict High-grade Prostate Cancer at Initial Biopsy", JAMA. Oncol., 2, 882 (2016). DOI: 10.1001/jamaoncol.2016.0097
- Castellanos-Rizaldos, E. et al . :"Exosomebased Detection of EGFR T790M in Plasma from Non-Small Cell Lung Cancer Patients", Clin. Cancer Res ., (2018). DOI: 10.1158/1078-0432. CCR-17-3369
- 植田幸嗣:「プロテオーム解析から見たバイオマーカーとしてのエクソソームとその特徴」,細胞工学,32,71 (2013).
- Jingushi, K. et al. :"Extracellular vesicles isolated from human renal cell carcinoma tissues disrupt vascular endothelial cell morphology via azurocidin", Int. J. Cancer , 142, 607 (2018). DOI: 10.1002/ijc.31080















