1 Step RT-qPCR と 2 Step RT-qPCRのどちらを選ぶ?
遺伝子発現解析やウイルス検査などの分野において、RT-qPCR (Reverse Transcription quantitative PCR) は、現在代表的な分子生物学的手法の一つとなっています。高感度かつ定量的にRNAを検出できることから、基礎研究のみならず、臨床検査や感染症診断においても広く活用されています。RT-qPCRを実施する際には、「1 Step RT-qPCR」 と 「2 Step RT-qPCR」 の2つの方法から選択することが可能です。一見すると操作工程の違いに過ぎないようにも思えますが、目的によって適した方法は異なります。
本記事では、以下の順序で段階的に手法の解説を行います。
- PCR(コンベンショナルPCR)とは
- リアルタイムPCR (qPCR) とは
- 逆転写(Reverse Transcription:RT)とは
- RT-qPCRとは / 1 Step法と2 Step法の原理の違いと使い分け
PCR (コンベンショナルPCR) とは
PCRとは、Polymerase Chain Reactionの略称であり、DNAポリメラーゼを用いて特定のDNA配列を連鎖反応的に増幅する方法です。1980年代に開発されたこの技術は、分子生物学に飛躍的な発展をもたらし、現在では不可欠な基盤技術となっています。
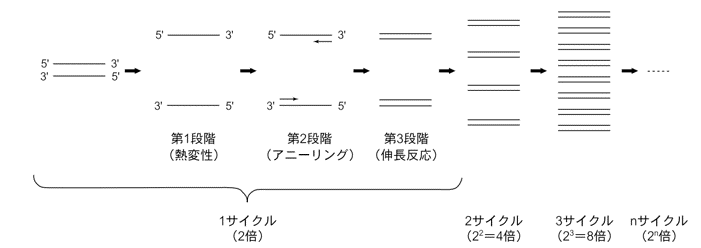
PCRの原理は、増幅したい標的DNAと、その両端配列に相補的な一対のDNAプライマー、耐熱性DNAポリメラーゼを用い、変性・アニーリング・伸長という3段階の温度変化を1サイクルとして繰り返すことにあります。これらの温度サイクルをnサイクル繰り返すことで、標的DNAは理論上2ⁿ倍に増幅され、例えば20サイクルでは約100万倍に達します。これら一連の温度変化は、サーマルサイクラーと呼ばれる装置によって精密に制御されます。
- 変性(Denaturation:94~96℃): 二本鎖DNAを熱変性して、一本鎖へと解離させます。
- アニーリング(Annealing:55~60℃): プライマーを一本鎖 DNA にアニーリングさせます。
- 伸長(Extension:72~74℃): DNAポリメラーゼがプライマーの3'末端から伸長し、新しいDNA鎖を合成します。
リアルタイムPCR (qPCR) とは
リアルタイムPCRは、PCRの増幅過程を蛍光シグナルとしてリアルタイムに検出・定量する手法です。リアルタイムPCRは、初期鋳型DNA量を定量することができるため、qPCR (quantitative PCR) と同義に扱われることが多いです。
通常のPCR (コンベンショナルPCR) では、反応終了後にアガロースゲル電気泳動を行い、増幅産物のバンドの有無や強度を確認することで結果を評価します。しかし、この方法では正確な定量は困難であり、さらにゲルの作製や泳動、染色、撮影といった工程に時間と手間を要します。
一方、リアルタイムPCRでは、 PCRの温度制御機能に加えて、蛍光シグナルを検出する機能を備えたリアルタイムPCR装置を用いて、DNAの増幅量をサイクルごとに連続的に測定します。これにより増幅曲線を取得し、指数関数的増幅段階における蛍光シグナルを解析することで、初期鋳型DNA量を定量することが可能となります。そのため、特に定量性が求められる解析において、リアルタイムPCRは通常のPCRと比較して大きな優位性を持っています。
このように、リアルタイムPCRは迅速かつ高感度にDNAの検出および定量を行うことができるため、遺伝子発現解析、遺伝子検査、感染症検査などの様々な目的で利用されています。
なお、リアルタイムPCRの検出系には、主に蛍光色素法と蛍光プローブ法の2種類があり、それぞれの違いについて以下にご紹介いたします。
リアルタイムPCRの検出系
①蛍光色素法(インターカレーター法)
蛍光色素法は、二本鎖DNAに特異的に結合して蛍光を発する色素を用いた検出系です。
PCR産物が増加するに伴ってDNAと結合する蛍光色素も増加し、蛍光強度が増加します。この蛍光強度からDNAの増幅の検出・定量を行います。
代表的な蛍光色素としては、SYBR™ Greenが使用されます。
なお、SYBR™ Greenは配列特異性を有さず二本鎖DNAに結合するため、非特異的増幅産物やプライマーダイマーにも結合します。そのため、反応終了後に融解曲線解析を行い、目的とする特異的増幅産物が得られているかを確認する必要があります。

②蛍光プローブ法
蛍光プローブ法は、特定のDNA配列に特異的に結合するよう設計されたオリゴヌクレオチドプローブを用いる検出法です。
このプローブは、5'末端側に蛍光色素 (レポーター) 、3'末端側に消光物質 (クエンチャー) を標識した構造を持っています。プローブが分解されていない状態では、レポーターとクエンチャーが近接しているため、FRET (Fluorescence Resonance Energy Transfer:蛍光共鳴エネルギー移動) により蛍光は抑制されています。PCRのアニーリング工程で、プローブは標的DNA配列にハイブリダイズします。その後、Taq DNA Polymeraseが伸長反応を進める際に、ポリメラーゼが有する5'→3'エキソヌクレアーゼ活性によって、結合しているプローブが分解されます。プローブが分解されると、レポーターとクエンチャーが物理的に分離し、蛍光の抑制が解除されることで、蛍光シグナルが増加します。この蛍光強度の増加をリアルタイムで測定することで、DNAの増幅を検出・定量することができます。代表的な蛍光色素とクエンチャーの組み合わせの例としては、以下があります。
【蛍光色素とクエンチャーの組み合わせの例】
・5' FAM - 3' TAMRA
・5' FAM - 3' BHQ1 (Black Hole Quencher)

- GeneAce Probe qPCR Mix II
- Double Dye Probe (蛍光プローブ) 合成サービス
*ニッポンジーン社HPに遷移します。
各検出系の特徴
| 検出系 | 蛍光色素法 | 蛍光プローブ法 |
|---|---|---|
| 検出原理 | 二本鎖DNA結合色素の蛍光を検出 | プローブ分解に伴う蛍光を検出 |
| 特異性 | やや低い: 非特異的産物やプライマーダイマーも検出 |
高い: プローブが標的配列に特異的に結合 |
| デザイン | 容易: プライマーの設計のみ |
複雑: プライマーに加えプローブ設計が必要 |
| コスト | 低い: プローブ不要 |
高い: プローブが別途必要 |
| 用途例 | ・遺伝子発現解析 (相対定量) ・スクリーニング |
・病原体検出 ・マルチプレックスPCR (SNP解析等) |
| 備考 | 特異性は主にプライマー設計や試薬性能に依存し、融解曲線解析による確認が必要 | 高い特異性を有し、マルチプレックス解析や検査用途に適する |
逆転写 (Reverse Transcription:RT) とは
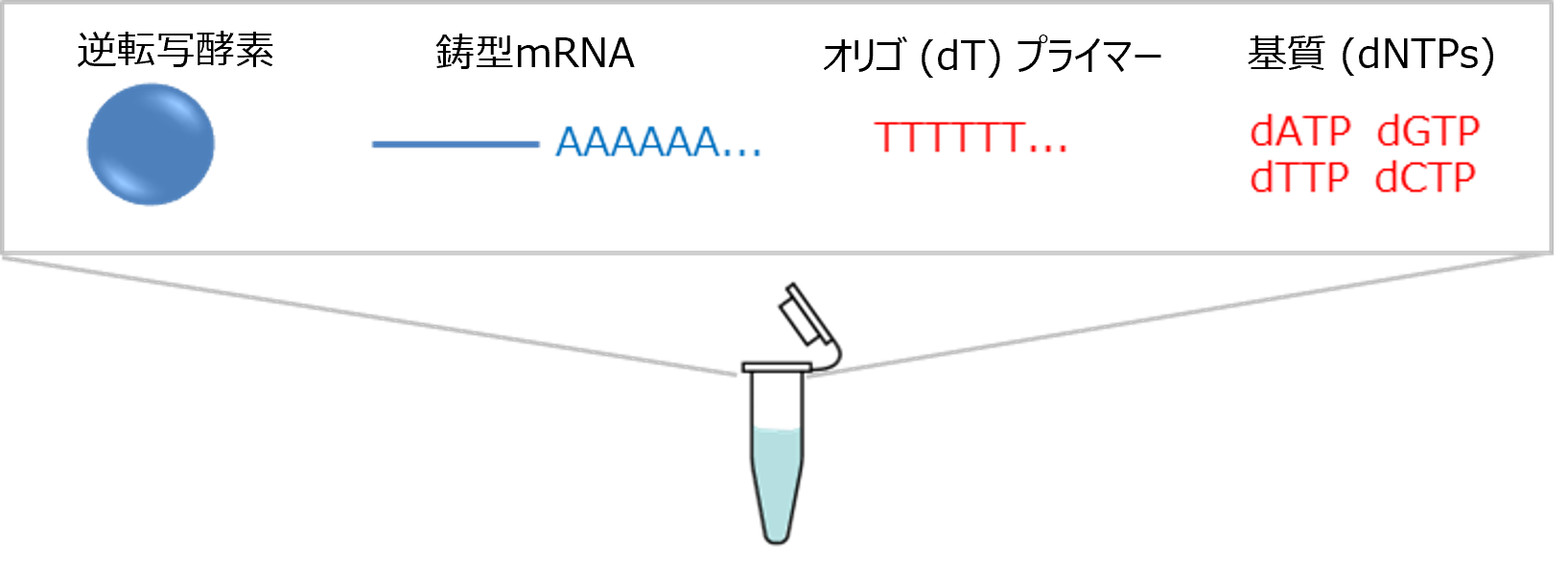
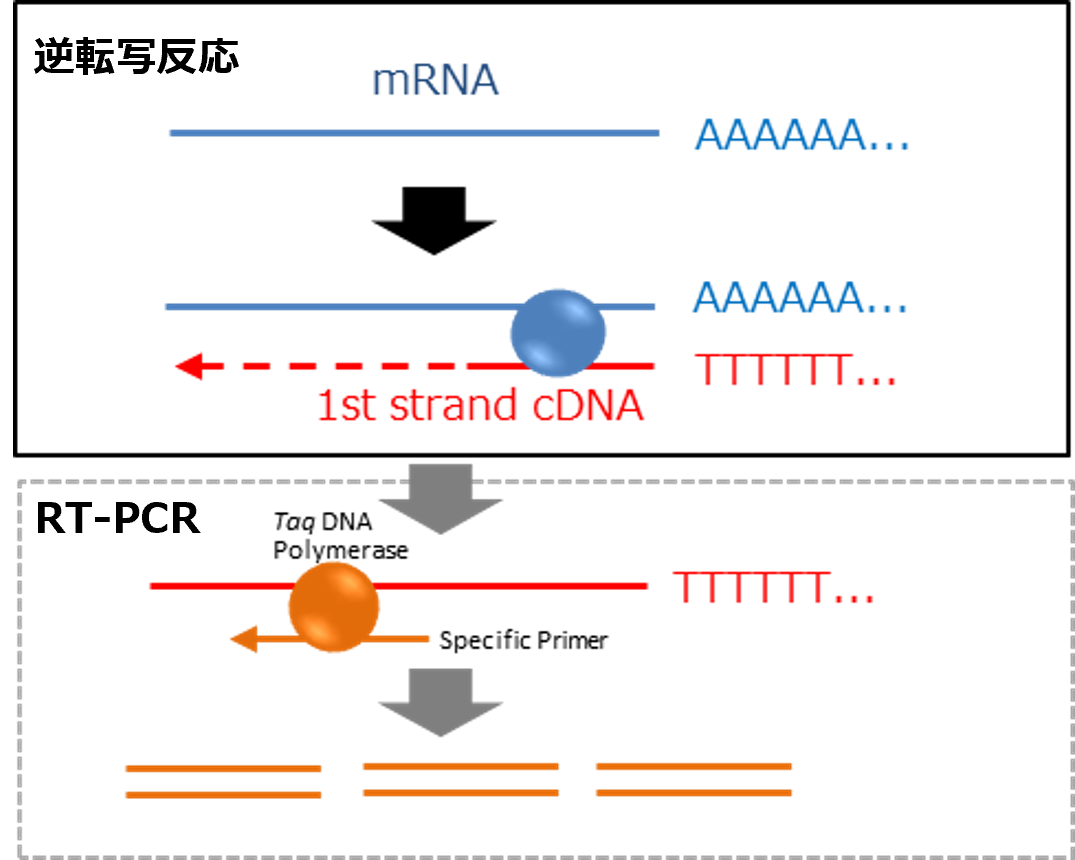
逆転写 (RT) は、RNAを鋳型として逆転写酵素によりcDNA (complementary DNA) を合成する反応です。
RNAの定量等の解析を行う際に、PCRではRNAを直接増幅することはできません。そのため、まずは逆転写酵素を用いてRNAからcDNAを合成する工程が必要となります。逆転写反応により得られたcDNAを鋳型としてPCRを行うことで、標的RNAの定量解析やシークエンス解析等が可能となります。

Pick Up! 1st strand cDNA合成キット 「GeneAce cDNA Synthesis Kit」
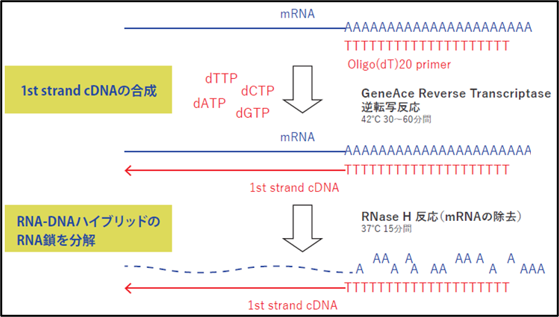
本製品は、RNAを鋳型に1st strand cDNAを合成するためのキットです。M-MLV由来 (RNase H-) 逆転写酵素「GeneAce Reverse Transcriptase」を採用しており、GeneAce Reverse Transcriptase はRNase H活性を持たないため完全長のcDNAの合成が可能です。
一方でcDNAの合成後はRNase H活性を持たないことで問題が生じる場合もあります。RT-PCRではcDNA-RNA鎖が残っていると、その後のPCRでcDNAの増幅が阻害される場合があります。この問題を解決するにはRNase H活性を欠損させた逆転写酵素 (GeneAce Reverse Transcriptase) でcDNA合成を行い、反応後にRNase Hで処理することが有効です。本製品にはRNase Hが含まれているため、cDNA合成後に処理することでPCR効率が向上する可能性があります。
RT-qPCRとは
RT-qPCRは、逆転写反応によって合成されたcDNAを鋳型としてqPCRを行い、RNAを検出・定量する手法です。
mRNA発現量解析やRNAウイルスの検出など、幅広い分野で利用されています。
RT-qPCRには、逆転写反応とqPCRを別々に行う「2 Step法」と、同一チューブで連続して行う「1 Step法」の2種類があります。
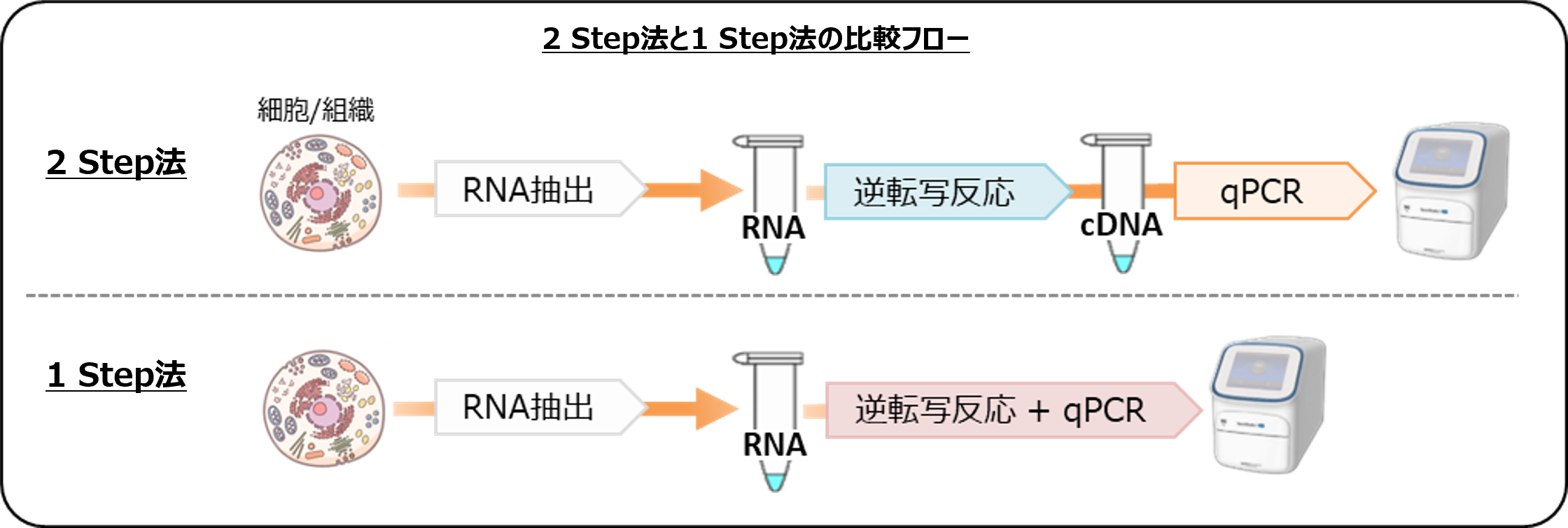
2 Step RT-qPCR (2 Step法)
2 Step RT-qPCRは、逆転写 (RT) 反応と qPCR反応をそれぞれ独立した反応系で実施する手法です。
逆転写反応では、解析目的に応じてランダムプライマー、オリゴ (dT) プライマー、あるいは配列特異的プライマーを使用します。RT反応によって合成されたcDNAは保存が可能であり、同一サンプルから複数の標的遺伝子を解析する場合に適しています。特に、1サンプルあたりで解析したい遺伝子数が多い研究や、追加解析が想定される実験において有用です。また、逆転写反応とqPCR反応を分離して行うため、それぞれの反応条件 (酵素量、反応温度、プライマー濃度など) を個別に最適化できます。そのため、増幅効率が低いサンプルや発現量の少ない遺伝子の検出においても、条件検討によって検出感度の向上が期待できます。
一方で、1 Step法と比較すると操作工程が多く、チューブの開閉回数や反応液の移し替え操作が増えるため、コンタミネーションのリスクが高まる点に注意が必要です。
1 Step RT-qPCR (1 Step法)
1 Step RT-qPCRは、遺伝子特異的プライマーを用いて、逆転写反応とqPCR反応を同一チューブ内で連続して行う手法です。
2 Step法と比較して操作工程が少ないため、時間の短縮が可能です。また、チューブの開閉や反応液の移し替え操作が不要となることから、コンタミネーションのリスクも低減できます。そのため、感染症検査など、あらかじめ標的遺伝子が決まっており、迅速な検出や定量が求められる場合に特に適した手法です。一方で、反応は単一チューブ内で完結するため、cDNAを保存することはできません。そのため、同じサンプルから別の遺伝子を解析する場合などには、元のRNAサンプルを適切に保存しておくか、再度RNAを抽出する必要があります。
使用製品例と所要時間の例
2 Step法

・ISOGENシリーズ
(約60分) GeneAce cDNA Synthesis Kit
約90分 ・GeneAce SYBR™ qPCR MixⅡ
・GeneAce Probe qPCR MixⅡ
約90分
1 Step法
・ISOGENシリーズ
(約60分) GeneAce One Step RT-qPCR Mix
(SYBR™系, Probe系)
約90分
各手法の対比表
| 手法 | 2 Step法 | 1 Step法 |
|---|---|---|
| 反応 | 逆転写とqPCRを個別に実施 | 同一チューブで連続的に実施 |
| 操作工程 | cDNAの移し替え操作を含む | 閉鎖系で一連の反応を実施 (コンタミネーションのリスクが低い) |
| 所用時間 | やや長い | 短い |
| cDNAの保存 | 保存・再利用可能 (複数の遺伝子解析に適する) |
保存不可 |
| 条件最適化 | 逆転転写とqPCRを個別に設定可能 | 個別での設定は不可 |
| 主な用途 | 遺伝子発現解析 | 病原体検出 |
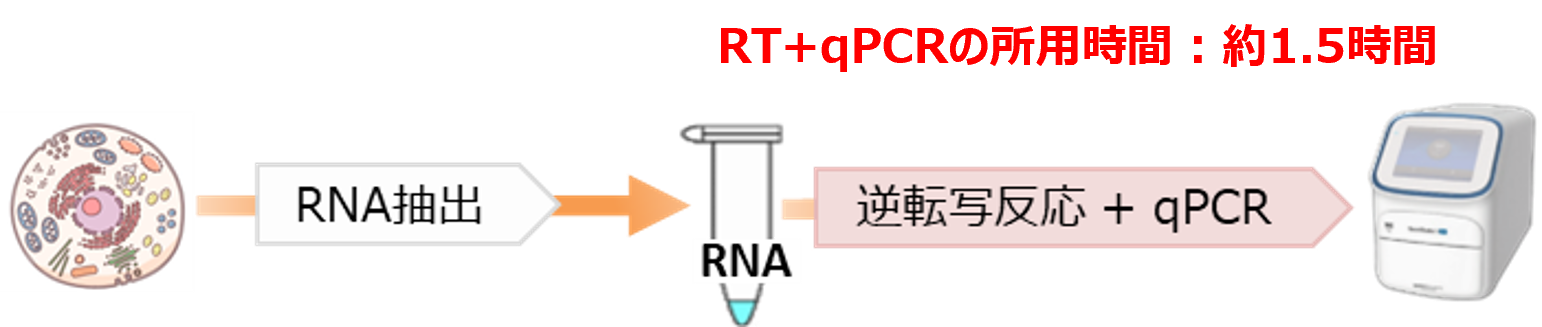
\お役立ち情報/ 簡易RNA抽出と1 Step RT-qPCRの組み合わせで大幅時短!
ニッポンジーンでは、細胞からの簡易的なRNA抽出試薬である「Template Prepper for Cell RNA」を販売しています。
本試薬と1Step RT-qPCR試薬と組み合わせて使用することで、RNA抽出からqPCRまでの所要時間を大幅に短縮できます。
また、96ウェルプレートにも対応しており、ハイスループットな実験系におすすめです!
本記事では、PCRに関する各種手法について紹介しました。それぞれの手法には特徴があり、解析目的や実験条件に応じた使い分けが重要です。
各手法の特性を正しく理解し、目的に合った方法を選択することは、信頼性の高い結果の取得だけでなく、実験の効率化やコスト削減にもつながります。






