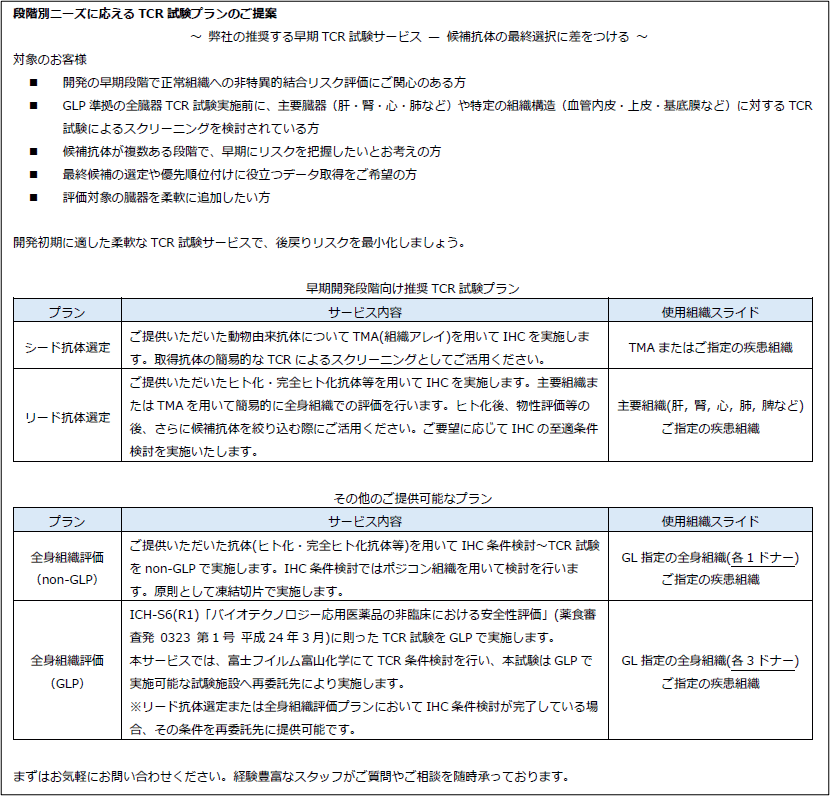
抗体医薬品候補のTCR (組織交差反応性) 試験 ~ 開発段階に応じた安全性評価と最適な試験プランについて ~ 第1回 TCR試験とは? ~抗体開発者必見!TCR試験の基礎解説~
本シリーズでは、バイオロジクスの非臨床安全性研究 (TCR試験含む) を担当された富士フイルム富山化学株式会社 富山研究開発センター猪又 晃 様より、全3回にわたり組織交差反応性 (Tissue Cross-Reactivity、TCR) 試験の基礎から実務的な導入方法、そして評価手法のポイントについて順を追って解説いただき、抗体医薬品開発における安全性評価の理解と実践をサポートします。
- 第1回 TCR試験とは? ~抗体開発者必見!TCR試験の基礎解説~
- 第2回 なぜ早期実施が推奨されるのか? ~候補抗体選定に差をつける早期TCR検討のすすめ~
- 第3回 TMA vs 凍結組織スライド、どちらが適切? ~TMAと凍結組織スライドの賢い使い分け~
第1回は「TCR試験とは?」として、その重要性と基礎的な概念についてご紹介します。
第1回は「TCR試験とは?」として、その重要性と基礎的な概念についてご紹介します。
モノクローナル抗体や関連する生物製剤は、がん、自己免疫疾患、感染症など様々な疾病に対する画期的な治療法として急速に普及しています。高い標的特異性を持つ一方、非特異的な組織結合 (オフターゲット結合) が副作用や毒性をもたらすリスクとして知られており、その安全性評価は患者の安全を確保する上で不可欠です。抗体医薬品は、開発初期に適切な安全性評価を行わなければ、臨床試験で重大な毒性問題が発覚し、開発の遅延や中止につながるリスクがあります。そのため、非臨床段階での安全性予測を強化するTCR試験が重要視され、適切な抗体候補の選定に大きく寄与しています。
TCR試験の役割と基本的な概念
TCR試験は、抗体候補がヒトおよび主要な非臨床動物種の正常組織にどのように結合するかを詳細に検査することで、安全性リスクを評価する試験です。抗体が意図せず結合する組織や細胞を早期に特定することで、潜在的な毒性や副作用を予測します。この試験は、治療の標的であるオンターゲット結合だけでなく、非標的部位へのオフターゲット結合も視野に入れて評価を行います。オフターゲット結合が確認された場合には、その生物学的意義を慎重に評価し、後続の開発戦略や安全性管理計画に反映させることが求められます。また、複数の動物種における組織結合のパターンを比較検討することで、非臨床毒性試験に用いる適切な動物モデルの選定を支援し、臨床試験の安全性予測精度を向上させます。
規制当局の指針とガイドライン
TCR試験は、米国食品医薬品局 (FDA) や欧州医薬品庁 (EMA) をはじめとする主要な世界各国の薬事規制当局によって、抗体医薬品の非臨床安全性試験の必須項目として位置づけられています。FDAは特に1990年代後半より、抗体医薬品の安全性評価にTCR試験の実施を勧告しており、ICH S6ガイドラインもこれを基に具体的な要件を定めています。EMAもFDAの指針を踏まえつつ、臨床試験の承認に至るまで十分な組織交差反応性データの提出を求める姿勢を見せています。これらの規制機関は、ヒトの正常組織を網羅的に評価することを求め、さらに主要な非臨床動物種と比較することで、人間における安全性リスクの推定と非臨床毒性試験の動物モデルの妥当性を裏付けることが重要としています。そのため、TCR試験は単にデータを取得するだけでなく、厳密かつ適切な試験設計と結果の生物学的解釈が求められ、規制対応の質を左右する要素となっています。
TCR試験における免疫組織化学 (IHC) 法の特徴と技術的課題
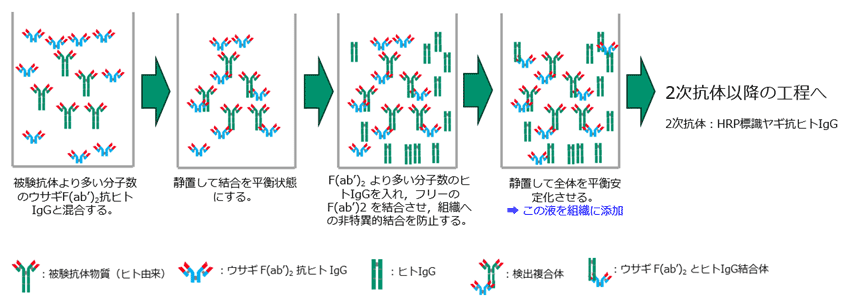
TCR試験の主流技術である免疫組織化学 (IHC) 法は、凍結保存された正常組織切片上に試験抗体を適用し、抗体と組織中の標的分子との結合を視覚的に捉える手法です。IHC法は抗体の結合部位を直接観察できるため、その特異性や局在を詳細に評価できるゴールドスタンダードと位置付けられています。凍結組織の使用は、パラフィン包埋組織と比較して抗原の天然構造保持に優れ、抗原変性による結合性低下を防ぐ点で重要です。このことが精度の高い安全性評価を可能にしています。一方で、技術的な課題も存在します。特にヒト由来やヒト化抗体を使用した場合、組織内の内因性ヒトIgGによる非特異的な背景染色が生じることがあり、結果の解釈が難しくなります。この問題に対しては、一次抗体と二次抗体をあらかじめ複合化して使用する「プレコンプレックス法」など、特異性を向上させる工夫が導入されています。また、堅牢なプロトコル設計、陰性対照の適用、経験豊富な病理専門家の評価により、信頼性の高いデータが確保されることが必須です。高精度の画像解析や定量化技術の活用も近年進んでいます。
プレコンプレックス法 (例)
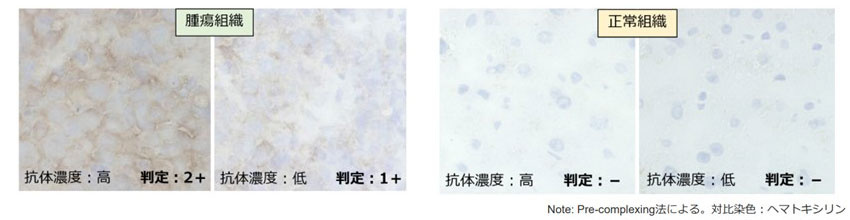
ヒト腫瘍組織において腫瘍細胞膜に発現する標的分子に対するTCR試験結果
TCR試験の歴史と今後の展望
TCR試験は、1990年代後半にFDAを中心にその重要性が認識され始めました。当初はバイオ医薬品の安全性評価における補助的な手法でしたが、技術の進歩とともに、抗体開発の必須試験として世界的に標準化が進みました。初期の取り組みでは、正常組織パネルの選定や解析手法にばらつきがありましたが、その後のガイドライン策定や技術革新によりIHC法の質が劇的に向上。プレコンプレックス法など非特異染色の対策技術や、高解像度画像解析の導入でより精緻なリスク評価が可能になりました。近年では、AIやデジタル病理学の活用によって画像解析の効率と客観性が高まり、これまで以上に迅速かつ正確なTCR評価が期待されています。将来的には、分子レベルでの相互作用解析やマルチオミクス解析との融合も視野に入り、安全性評価の精度がさらに向上する見込みです。抗体医薬品の安全性評価におけるTCR試験は今後も進化を続け、より早期段階のリスク軽減と臨床開発の成功率向上に寄与すると期待されています。
まとめと次回予告
TCR試験は、抗体医薬品開発における安全性評価の柱として欠かせないものであり、早期から適切に実施することで潜在的なリスクを把握し、後期の臨床段階でのトラブルを未然に防ぐことが可能です。FDAやEMAといった規制当局の厳しい指針のもと、IHC技術を中心に確立された方法論により、信頼性の高い安全性データを提供しています。特に、近年では技術的課題への対策や画像解析の高度化により、より正確な抗体の組織への結合特性評価が実現されており、今後もAI技術と融合したさらなる進化が期待されます。こうした背景を踏まえ、TCR試験は抗体の開発初期から臨床試験申請までの各段階で効果的に活用することが望まれます。
さて、第1回はここまでとなりますが、次回の第2回「なぜ早期実施が推奨されるのか? ~候補抗体選定に差をつける早期TCR検討のすすめ~」、第3回「TMA vs 凍結組織スライド、どちらが適切? ~TMAと凍結組織スライドの賢い使い分け~」へと続きます。引き続きご注目ください。
関連サービス