【総説】ミクログリアはシナプスを食べるか?
本記事は、和光純薬時報 Vol.94 No.2(2026年4月号)において、
国立精神・神経医療研究センター 神経研究所 疾病研究第二部 小山 隆太 様に執筆いただいたものです。
はじめに:ミクログリア研究のパラダイムシフト
1919年にPío del Río-Hortegaによって同定されたミクログリアは、長らく脳内の「掃除屋」あるいは免疫細胞として、死細胞や異物を処理する受動的な存在と考えられてきた。しかし2000年代以降、Cx3cr1-GFPマウスを用いたin vivo二光子励起顕微鏡観察により、ミクログリアは極めて動的であり、絶えず突起を伸縮させながら周囲を監視していることが明らかとなった1)。
この発見は、ミクログリアが神経回路の洗練、すなわちシナプス刈り込みに能動的に関与しているという仮説を生んだ。一方で、この仮説の中核には常に一つの根本的な問いが存在してきた。それは、「ミクログリアは本当に、生きた接続としてのシナプスを能動的に食べているのか」という問題である。固定組織においてミクログリア内にシナプス由来分子が検出されるという間接的証拠は多数報告されてきたが2)、それが能動的なphagocytosisの結果なのか、あるいは神経細胞側で切り離された残骸の回収にすぎないのかを、静的なスナップショットから判断することは困難であった。
この命題は、ミクログリア研究の「因果」を左右する。もしミクログリアが生きた接続を直接改変するなら、回路形成や学習・疾患の理解はミクログリアを含む因果モデルへと再編される。一方、残骸の回収にとどまるなら、ミクログリアは結果の後処理として位置づけられる。したがって本問題は、ミクログリアの役割を「必須の因子」と見るか「追随する因子」と見るかを分ける、基礎的かつ高いインパクトを持つ争点である。
本稿では、近年のライブイメージング研究によって明らかになった決定的証拠をもとに、「シナプス貪食」を巡る論争を整理するとともに、「食べる」という言葉の再定義、そして分子に加えて物理的特性がこの過程を制御するという新しい視点について概説する。
1 「食べる」の再定義:混乱を避けるために
ミクログリアによるシナプス除去を議論する際、まず整理すべきは「食べる」という行為の定義である。この分野では、phagocytosis、trogocytosis、engulfmentといった異なる現象(表1)が厳密に区別されないまま用いられてきたことが、議論の混乱を招いてきた。例えば、固定標本で「ミクログリア内にシナプス分子がある」ことは、phagocytosisともengulfmentとも両立しうる。それにもかかわらず、前提となる現象の定義が曖昧なままでは、研究間の結論が噛み合わず、「肯定(食べる)/否定(食べない)」の対立だけが先鋭化しやすい。本稿では、細胞が標的全体を取り込むphagocytosisや標的の一部のみを削り取るtrogocytosisなどを区別して議論を進める。これらを明確に区別することで、ミクログリアが「いつ」「どのような条件で」関与しているのかをより正確に理解することが可能となる。
表1.「食べる」の分類:あなたの知りたい「食べるんですか?」とはどれのことか?
| 名称 | 内容 |
|---|---|
| 細胞内機構(過程を表す用語) | |
| Synaptic phagocytosis | シナプス由来構造を大部分または全体として細胞内に取り込み、リソソーム系で分解する細胞内過程。 |
| Synaptic trogocytosis | ギリシャ語 trogo(かじる)に由来し、軸索や樹状突起との連続性を保った生きたシナプスから、その一部のみを切り取る部分的貪食過程。 |
| Nibbling | Synaptic trogocytosis の口語的・比喩的表現。「少しずつ削る」という直感的イメージを補足するために用いられる。 |
| 構造的状態(記述的用語) | |
| Synapse engulfment | 軸索または樹状突起との連続性を失ったシナプス構造が細胞内に取り込まれた状態。構造的な取り込み完了を指し、その後の分解過程は含意しない。 |
| Synapse stripping | 主に病態条件下で、神経細胞の細胞体や樹状突起表面からシナプス前終末が物理的に剥離される現象。必ずしも貪食を伴わない。 |
| Synapse shedding | 神経細胞自身がシナプス構造を能動的に切り離す過程。ミクログリアはその後の断片処理(clearance)を担う場合が多い。 |
| 構造的帰結(概念用語) | |
| Synapse elimination | 神経回路内に存在していたシナプス構造が結果として消失する現象を指す包括的用語。原因や主体は問わない。 |
| Synapse pruning | 神経回路の形成・成熟過程において起こる、機能的最適化を目的とした構造的シナプス減少を指す概念語。具体的な細胞機構は規定しない。 |
| Synapse culling | 不適切または過剰なシナプスが選択的に排除される過程を、「選別・間引き」という概念的視点から表現した比喩的用語。 |
| Synapse clearance | 不要となったシナプス構造や断片が、最終的に脳内から除去・処理される過程を指す広義の用語。複数の機構を含み得る。 |
注)本表で示した用語には、参考文献間における定義の揺らぎや、概念的に重なり合う部分が存在する。筆者自身も、各文献の文脈を踏まえつつ注意深く用語を選択しているが、ここで示した整理は現時点での理解に基づくものであり、今後の研究の進展に伴って更新されうることに留意されたい。
2 「見ているつもり」の落とし穴:先行研究の方法論的限界
2025年にAndohらは、ミクログリアによるシナプスtrogocytosisをライブイメージングで初めて直接的に捉えた3)。しかしそれ以前から、一部の研究者の間では「この現象はすでに報告されている」という誤った認識が共有されていた。その根拠として頻繁に引用されてきたのが、Weinhardら(2018)4)およびLimら(2021)5)の研究である。
Weinhardらは、ミクログリアがシナプスを部分的に取り込む現象をtrogocytosisとして提唱し、プレシナプス構造が標的であると結論づけた4)。しかしWeinhardらが用いたAAV-Syn::iRFPは、シナプス小胞やアクティブゾーンに局在する分子ではなく、神経細胞の細胞質に広く分布する蛍光タンパク質である。それにもかかわらず、論文中では"Presynaptic AAV-Syn::iRFP"という表記が用いられており、Synapsinプロモーターによる神経細胞特異的発現と、プレシナプス構造の特異的標識とが混同されている。また、軸索膜や軸索全体の連続性を示すマーカーが併用されていないため、取り込まれた蛍光シグナルが生きたシナプス末端由来なのか、すでに断片化した軸索デブリなのかを厳密に区別することはできない。しかしながら、論文タイトルは"Microglia remodel synapses by presynaptic trogocytosis and spine head filopodia induction"とされており、データが直接示す範囲を超えて解釈が先行している印象は否めない。
Limらは、ツメガエル視覚系において、軸索およびシナプス関連構造に由来する蛍光シグナルが、ミクログリア細胞内に時間依存的に蓄積することを示し、trogocytosisの可能性を示唆した5)。しかしこの研究で定量されたのは、ミクログリア細胞内に存在するこれらの蛍光シグナルの総量であり、分子定義された単一のシナプス構造が、軸索との連続性を保ったままリアルタイムでミクログリアへ移行する瞬間を直接捉えたものではなかった。
このように、WeinhardらとLimらの研究は、いずれもpresynaptic trogocytosisの概念を広めることには貢献した一方で、その実験的な実証には至っていなかった。
3 Andohらの研究が示した決定的証拠
これらの方法論的課題を体系的に解消したのがAndohら(2025)の研究である3)。本研究の本質的な強みは、「シナプスの分子定義」「生きた接続であることの保証」「十分な時空間解像度」という三つの条件を同時に満たす実験設計を構築した点にある。
Andohらは、シナプス小胞タンパク質シナプトフィジンを蛍光標識することで、取り込まれる構造が機能的なプレシナプスであることを分子レベルで定義した。さらに神経細胞膜に局在するiRFPを併用することで、trogocytosisが起こる瞬間にそのシナプスが軸索本体と連続した生きた状態にあることを直接確認している。また、1分間隔という頻度のライブイメージングにより、数分以内に完結するtrogocytosisを可視化することに成功した。
その結果、ミクログリアが軸索全体を損なうことなく、プレシナプス構造のみを選択的に削減するtrogocytosisの一連のダイナミクスが初めて直接的に記録された。論文中で提示された動画は、シナプス貪食を巡る議論に決定的な裏付けを与えるものである。
さらに重要なのは、ミクログリアがシナプスに接触すれば即座に貪食が起こるわけではない、という条件依存性である。Andohらは、補体C1qとホスファチジルセリン(PS)の結合が、ミクログリアの滞在時間(dwelling time)を延長する物理的な「ひっかかり」として機能することを示した。C1qは脳内で可逆的にシナプスへ結合・解離を繰り返すが、過剰活動が生じた局所では非アポトーシス的なcaspase-3活性化を介してPSが露出し、C1qが強固に結合する。これによりミクログリアはその部位に足止めされ、一定の滞在・拘束が成立したときにのみ、trogocytosisの実行へと進む。すなわち本研究は、「分子タグ(C1q-PS)」が化学的シグナルであると同時に、物理的拘束を生む装置として働くことを示し、シナプス削減を"反応"ではなく"条件成立の結果"として再定義した点でも重要である。
4 観察の盲点:なぜ「見えなかった」のか
これほど明瞭な現象が長らく捉えられなかった理由の一つは、観察対象の選択にある。多くのin vivo研究は樹状突起スパインに注目してきたが、Andohら3)やWeinhardら4)の研究が示すように、ミクログリアはポストシナプスだけではなくプレシナプスも標的にする。したがって、スパインとミクログリアの二者だけを観察し続けても、trogocytosisの決定的瞬間が頻繁に得られないのは、ある意味で必然であった(図1)。
むしろスパインに対するミクログリアの関与は、接触を介した形態変化の誘導やサイズ調節、突起形成の促進など、別種の調節として観測されることが多い。観察の焦点を「スパインが食べられるか」に固定してしまうと、ミクログリアの主要な標的と作用様式を取り逃がす。シナプス削減の実像に迫るためには、どこを観るべきかという前提そのものを更新する必要があったのである。
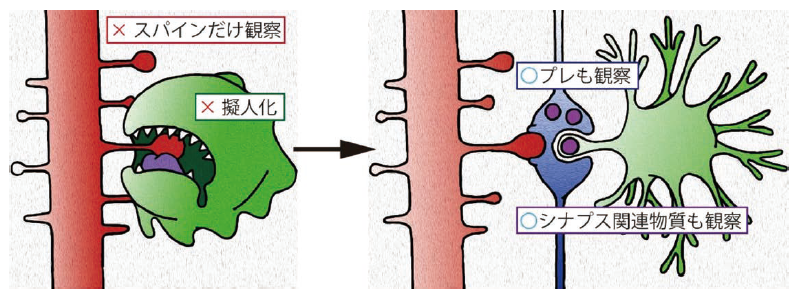
シナプス改変はスパイン観察のみでは見落とされやすく、プレシナプスブートンやシナプス小胞関連分子、軸索連続性マーカーを用いた分子定義が重要である。解釈においては、細胞の主体性(擬人化)を前提にせず、分子標識と標的側の物理条件に基づいて現象を捉える必要がある。
5 分子論と物理論の統合
ミクログリアの機能はしばしば「貪食対象としてどちら(のシナプス)を選ぶか」や、「貪食様式として何を選ぶか」という、ミクログリアを主体とする擬人化された枠組みで語られてきた。しかしCornellらは、貪食細胞によるphagocytosisとtrogocytosisの選択が、分子スイッチではなく標的側の皮質張力という物理量によって制御されることを示した6)。すなわち、柔らかい標的では局所で膜変形が起こりやすいためにtrogocytosisが成立し、硬い標的では膜変形が起こらずに、そのまま全体を取り込むphagocytosisへと移行する。
ここで重要なのは、貪食細胞側に「trogocytosis用」と「phagocytosis用」の別個のプログラムが備わっているというより、同一の駆動機構が標的側の物理的抵抗により異なる結果として現れる、ということである。すなわち、ミクログリアが「食べ方」を選んでいるのではなく、標的側の物理的特性が結果を規定している可能性がある7)。この視点は、特定の単一分子の有無だけでは説明しきれない条件依存性を理解する上で有用であり、C1qやPSといった分子機構を含む総和として規定される「力学的状態」が、シナプス削減様式を調節する可能性を示唆する。もしシナプスの硬さがこのような力学的状態の一要素としてミクログリアを介したシナプス可塑性に関与しているとすれば、きわめて興味深い。
おわりに:シナプスは「食べられる」のではなく「削られる」
「ミクログリアはシナプスを食べるか?」という問いに対し、我々は今や「イエス」と答えることができる。ただしそれは、単純なphagocytosisを意味するものではない。ライブイメージングが明らかにしたのは、ミクログリアが生きたシナプス接続を局所的に削減するtrogocytosisという実態である。この過程はミクログリアの意思ではなく、分子標識と標的側の物理的特性が重なったときにのみ成立する。ミクログリアは「何を食べるか」を決める存在ではなく、「削減が許容された構造」に応答する調整機構なのである。
謝辞
本稿の執筆はAMED(JP23jf0126004、JP24wm0625114、JP25wm0625518)およびJST(JPMJCR24B6)の支援を受けて行われた。本稿は、筆者のラボメンバーである安藤めぐみ博士、河野玲奈博士、大柿安里博士、宮田一馬氏からの批評を踏まえ、本文を修正したものである。
参考文献
- Nimmerjahn, A. et al. : Science, 308, 1314(2005).
- Paolicelli, R. et al. : Science, 333, 1456 (2011).
- Andoh, M. et al. : Nat. Commun., 16, 918 (2025).
- Weinhard, L. et al. : Nat. Commun., 9, 1228 (2018).
- Lim, T. et al. : eLife, 10, e62167 (2021).
- Cornell, C. E. et al. : Nat. Cell Biol., 27, 2078(2025).
- Zhu, T. et al. : iScience, 26, 105993 (2023).




