【総説】重水素創薬を拡充する重アルキル化剤
本記事は、和光純薬時報 Vol.94 No.2(2026年4月号)において、
大阪大学大学院薬学研究科・教授 澤間 善成 様、博士研究員(日本学術振興会PD) 阪 一穂 様に執筆いただいたものです。
1 はじめに
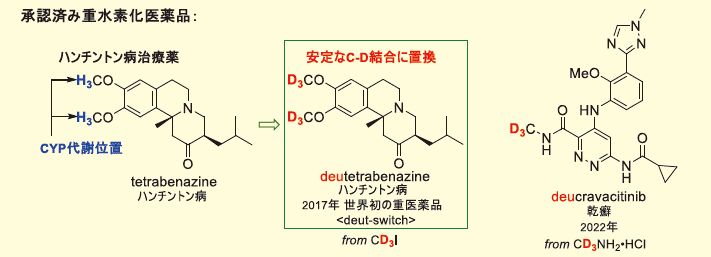
重水素(2H ; D)は、水素(1H ; H)の放射性をもたない安定な同位体である。近年、重水素化化合物は、ラマン分光や中性子散乱など様々な科学分野で活用されている。特に創薬分野では、重水素化医薬品(重医薬品;ヘビードラッグ)が注目されている1)。炭素-重水素(C-D)結合は炭素-水素(C-H)結合よりも強固になるという速度論的同位体効果が知られている。したがって、医薬品の代謝部位のC-H結合を安定なC-D結合に置き換えると、代謝安定性の改善が期待される。例えば、ハンチントン病治療薬のtetrabenazineの代謝部位となる2つのCH3O基をCD3O基に置換したdeutetrabenazineが初の重医薬品として2017年に承認された(図1)。deutetrabenazineは重水素導入により代謝安定性が向上し、服用回数の削減に繋がっている。親医薬品(H体)が既に存在し、その一部を重水素に置き換えたものをdeut-switch重医薬品と呼ぶ。また、deucravacitinibは窒素原子に置換したメチル基に重水素が導入された医薬品で、重水素導入により毒性代謝物の生成が抑制されている。重水素導入の効果は薬剤開発段階で発見され、重水素化体のみが医薬品として承認された。deucravacitinibのような親医薬品が存在しない重医薬品は、de novo重医薬品に分類される。de novo重医薬品の登場により、医薬品開発段階から重水素化体の活性や毒性を評価する必要性が一層増している。ヘテロ原子隣接位(α位)のC-H結合は特にシトクロムP450(CYP)により代謝されやすいため、この部位にC-D結合を導入することが重要である。これらの重医薬品は、市販のCD3IやCD3NH2を重水素化試薬として用いることで合成されている1)。しかし、市販されている重水素化試薬はそのほとんどがCD3化に限定されている。
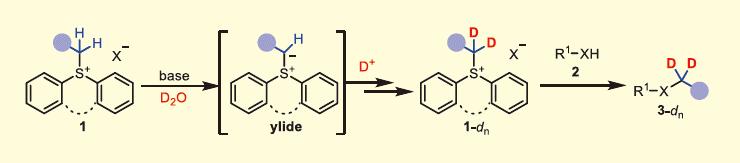
重水(D2O)は、天然に豊富に存在し、最も安価な重水素源である。したがって、D2Oを用いた重水素化法の開発が望まれるが、位置選択的に重水素を導入する手法はごく限られていた。そこで我々は、位置選択的に重水素を導入できるアルキル化試薬(重アルキル化試薬)の開発に着手した(図2)2,3)。アルキルスルホニウム塩(1)の硫黄α位の酸性度は、有機溶媒中で比較的高く、塩基性条件下イリドを形成する。したがって、D2O共存下であれば、イリドはデューテロン(D+)を捕捉し、硫黄α位選択的な重水素化が期待される。得られた重アルキルスルホニウム塩(1-dn)が、医薬品をはじめ多様なヘテロ求核種(2)に対する求電子種として作用すれば、ヘテロ原子隣接位選択的に重水素化された重アルキル付加体(3-dn)が得られると考えた。本手法を確立することで、多様な重アルキル基を簡便に導入できる。以下、本研究の詳細と試薬調製や使用法のノウハウを記載する。
2 重アルキル化試薬の調製
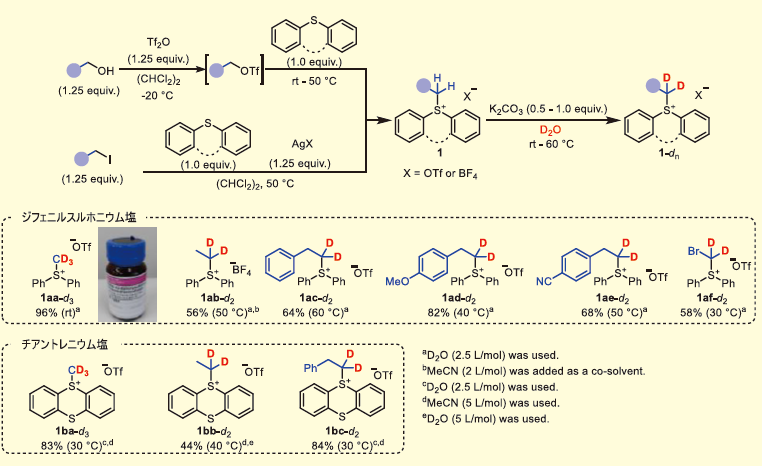
詳細な検討の結果、アルキルジフェニルスルホニウム塩(1a)とアルキルチアントレニウム塩(1b)を用いることで、本コンセプト(図2)を達成できることが明らかになった。1aと1bは、主に以下の方法で合成した(図3)。
【アルキルスルホニウム塩合成法1】
低温条件下、アルキルアルコールとトリフルオロメタンスルホン酸無水物(Tf2O)から、アルキルトリフラートを調製した。連続してスルフィド(ジフェニルスルフィドもしくはチアントレン)を添加することで1が得られた。1の反応混合液をクロロホルム/蒸留水で抽出した後、得られたクロロホルム層をMgSO4で乾燥した。減圧濃縮した後、濃縮残渣(固体または液体)を少量のクロロホルムに溶解し、貧溶媒としてジエチルエーテルを加えると、1が無色の固体として析出した。すなわち、この晶析処理で1を簡便に単離精製できる。なお、メチルジフェニルスルホニウム塩(1aa)とメチルチアントレニウム塩(1ba)は、市販のメチルトリフラートから合成した。
また、アルキル源の入手しやすさなどの観点から、ヨウ化アルキルを原料とした手法も利用した。例えば、ブロモメチルジフェニルスルホニウム塩(1af)は次のように合成した。
【アルキルスルホニウム塩合成法2】
銀トリフラート(AgOTf)共存下、ブロモヨードメタンとジフェニルスルフィドから、1afが得られた。1afの反応混合液からろ過によりヨウ化銀を除去したのち、ろ液を減圧濃縮した。得られた濃縮残渣を上と同様に晶析処理することで、1afを精製した。
なお、対アニオンが晶析に影響を与える場合がある。1abは【合成法2】で合成したが、銀塩としてAgOTfを用いると精製過程でスルホニウム塩が晶析しなかったため、AgOTfの代わりに銀テトラフルオロボレート(AgBF4)を利用した。精製や試薬としての取り扱いやすさから、1は固体として得られることが望ましい。したがって、対アニオンの探索も重要である。
得られたメチルジフェニルスルホニウム塩(1aa)は、D2O中、K2CO3存在下室温で定量的に重水素が導入された。メチル基(1aa)のみならずエチル基(1ab)、フェネチル基(1ac−1ae)、ブロモメチル基(1af)でも硫黄α位選択的に重水素化が進行した。1abは重水に対する安定性が低く、アセトニトリルを共溶媒に用いることで、重水素化効率が改善された。また重水素化は、アルキルジフェニルスルホニウム塩(1a)のみならず、多様なアルキルチアントレニウム塩(1b)にも適用できた。1bはD2Oに対する溶解性が低いため、共溶媒としてアセトニトリルを添加することが重要である。d3-メチルジフェニルスルホニウム塩(1aa-d3)およびd2-エチルジフェニルスルホニウム塩(1ab-d2)が製品化されている。
3 求電子反応による重アルキル基導入
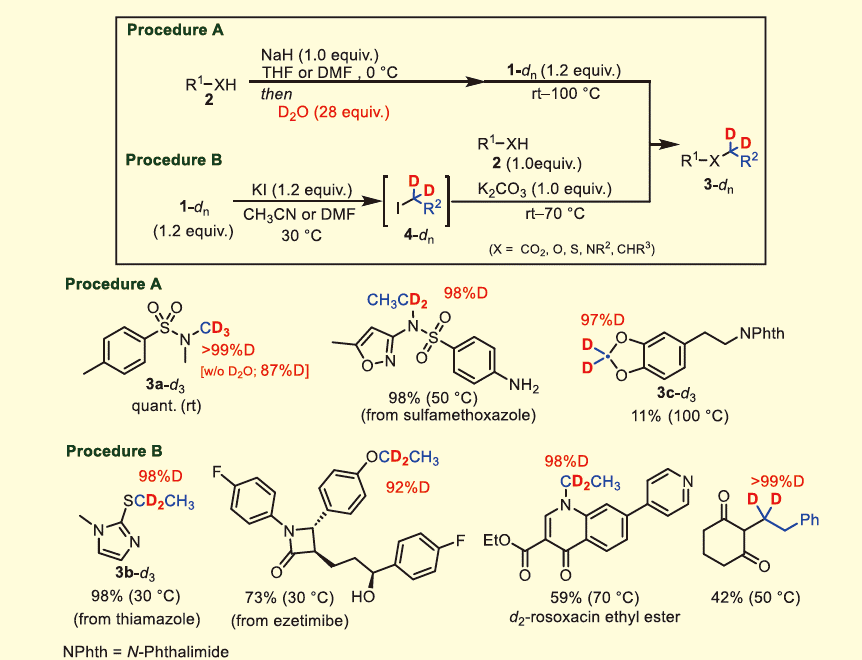
得られた重アルキルスルホニウム塩(1a-dn)は、求電子的重アルキル化に適用できる。N-メチルスルホンアミド(2a)を求核種として、水素化ナトリウム(NaH)で活性化したのち、d3-メチルスルホニウム塩(1aa-d3)を添加したところ、目的物(3a-d3)が良好な収率で得られたが、重水素化率は87%に低下した(図4)。重水素化率の低下は、求核種が塩基として作用することで、1aa-d3のC-D結合部位が反応系中に夾雑するH+源と反応し、C-H結合に変換されたためと推測した。そこで、NaHで2aを活性化したのち、D2Oを少量添加したところ、3a-d3の重水素化率は改善し、高重水素化率で重水素が導入された化合物が得られた。以下、この手法をProcedure Aとする。一方、thiamazole(2b)を求核種とした際、Procedure Aでは反応が複雑に進行してしまい、重アルキル付加体(3b-d2)は得られなかった。この問題はヨウ化カリウム(KI)を用いることで解決された。d2-エチルジフェニルスルホニウム塩(1ab-d2)とKIを混合すると、速やかにd2-ヨウ化エチル(4b-d2)が生じた。これを単離することなく、2bとK2CO3を連続的に添加したところ、3b-d2が高い重水素化率で得られた。本手法を、以下Procedure Bとする。Procedure AおよびBを適用することで、スルホンアミドやチオール、フェノール、アミン、α,γ-ジケトンなど、多様な求核種に重アルキル基を導入でき、医薬品の後期重アルキル化が可能である。基質適用例の一部を図4に示した。カテコール(2c)を基質とした場合、d2-ブロモメチルジフェニルスルホニウム塩(1af-d2)を用いると、d2-メチレンジオキシベンゼン誘導体(3c-d2)が得られた。これらの反応はまず、Procedure Aで検討した。反応が複雑に進行したり、重アルキル付加体(3-dn)と分離不可能な副生物が生じたりした場合、Procedure Bを採用した。また、重アルキルチアントレニウム塩(1b-dn)も、求電子的重アルキル化試薬として利用でき、かつラジカル種としても活用できることを見出している3)(詳細は割愛する)。
4 多様な重アルキル化試薬への変換
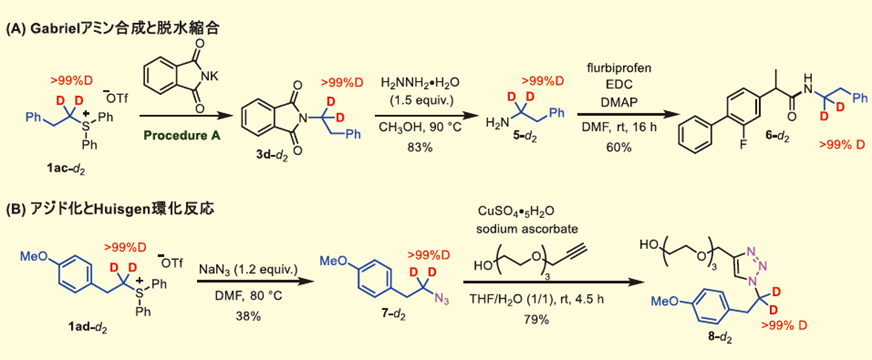
重アルキルスルホニウム塩(1-dn)は、さらに多様な重アルキル化合成試薬に変換できる(図5)。前項では、1a-dnとKIを共存させることで、ヨウ化重アルキルへと変換できることを示した。また、フタルイミドカリウムを求核種としてProcedure Aを適用すると、N-(d2-フェネチル)フタルイミド(3d-d2)が得られた。3d-d2はGabrielアミン合成の中間体である。3d-d2のフタロイル基は、ヒドラジン一水和物を共存させることで除去でき、d2-フェネチルアミン(5-d2)が得られた。5-d2は、医薬品flurbiprofenのカルボン酸との脱水縮合反応により、対応するアミド(6-d2)が得られた。また、1ad-d2は、ナトリウムアジド(NaN3)が共存すると、対応する重アルキルアジド(7-d2)へと変換された。7-d2は、アジドとのHuisgen環化反応により、トリアゾール8-d2が得られた。これらの反応では、いずれも重水素化率を損なうことなく進行することが特徴である。
5 展望
以上、著者らはアルキルスルホニウム塩を基盤とした新規重アルキル化法を確立した。重アルキルスルホニウム塩(1-dn)は、求電子的重アルキル化試薬として機能し、医薬品をはじめとする多様な化合物の後期重アルキル化を達成した。また、1-dnはハロゲン化物、アミン、アジドなどの重アルキル化合成試薬にも変換できた。さらに、重アルキルチアントレニウム塩(1b-dn)は、可視光照射下で重アルキルラジカル種として利用でき、位置選択的な重水素化化合物の多様性拡大に成功した。安価で天然に豊富に存在するD2Oを重水素源とした本手法は、重水素創薬をはじめ、科学の発展に大きく寄与することが期待される。
参考文献
- 重医薬品に関する近年の総説
(a) Ogasahara, R., Ban, K. and Sawama, Y. et al. : ChemMedChem, 19, e202400201 (2024).
(b) Zahng, L. et al. : ChemBioChem, 26, e202400837 (2025).
(c) Chen, Y. et al.: ChemMedChem, 20, e202400836 (2025).
(d) Chen, J. et al. : Eur. J. Med. Chem., 287, 117371 (2025).
(e) Olaizola, I. et al. : Top. Curr. Chem., 383, 31 (2025). - Ban, K. and Sawama, Y. et al. : Angew. Chem. Int. Ed., 62, e202311058 (2023).
- Ban, K. and Sawama, Y. et al. : Bull. Chem. Soc. Jpn., 97, uoae109 (2024).




