【総説】核酸合成用環状ホスホロアミダイト型キャッピング剤「EDCP」
本記事は、和光純薬時報 Vol.94 No.2(2026年4月号)において、
徳島文理大学薬学部 張 功幸 様に執筆いただいたものです。
1 はじめに
オリゴヌクレオチドの医薬分野への応用は急速に拡大しており、それに伴い、より高収率かつ高純度で目的のオリゴヌクレオチドを得ることの重要性が高まっている。現在オリゴヌクレオチドの化学合成には、三価のリン化合物を用いるホスホロアミダイト法が広く利用され、その合成は通常、CPG(controlled pore glass)やPS(polystyrene)担体上で、3′→5′方向にヌクレオチド単位で1塩基ずつ伸ばしていくことで達成される。その伸長サイクルは、以下の4工程からなる。
(1) 5′末端のジメトキシトリチル(DMTr)基の除去
(2) 生じた5′-ヒドロキシ基と伸長したいヌクレオシドのホスホロアミダイト体のカップリング
(3) カップリングしなかった(未反応の)5′-ヒドロキシ基の以降の伸長を防ぐためのキャッピング
(4) カップリングで生じた亜リン酸部のリン酸への酸化
この一連のプロセスにおいて、キャッピングは目的のオリゴヌクレオチドの合成に直接影響を与えないが、オリゴヌクレオチドの精製を困難にする1塩基欠損オリゴヌクレオチド(n-1塩基長のオリゴヌクレオチド)などの副生成物の生成を抑制する役割を担っている。目的のオリゴヌクレオチドと1塩基欠損オリゴヌクレオチドの分離は容易ではないことから、高収率かつ高純度で目的物を得るためにキャッピングの果たす役割は大きい。現在では、キャッピング剤として、Ac2O/N-メチルイミダゾール/ピリジン(またはルチジン)の組み合わせが広く利用されているが、DMTr基の脱保護に伴う収率の低下1)や核酸塩基部との反応による塩基修飾(主に、グアニン塩基との反応2,3))などの報告もあり、改善の余地がある。さらに、キャッピング時にTHF溶媒が使用される場合には、ホスホロチオエートオリゴヌクレオチドの脱硫化が見られることも報告されている4)。一方で、異なるタイプのキャッピング剤としてホスホロアミダイト型キャッピング剤も開発されている。ホスホロアミダイト型キャッピング剤は、(2)のカップリング時に使用するユニットと同じホスホロアミダイト構造を持つため、カップリングと同条件でキャッピングが可能となり、従来の伸長サイクルに組み入れることが容易である。さらに、一般的にAc2Oよりも高いキャッピング能(反応性)を有する。その先駆けとして、1994年にAgrawalらのグループがdiethyl N,N-diisopropylphosphoramidite(DDP)を報告した5)(図1)。その後、マイクロチップ上でのオリゴヌクレオチド合成用に開発されたUniCap phosphoramidite6)、高脂溶性ユニットをもつLipocap7)やcholesteryl phosphoramidite8)などが開発されてきた(図1)。
一方で、伸長するホスホロアミダイト体(ヌクレオシド、非ヌクレオシドを問わず)よりも高い反応性をもつホスホロアミダイト化合物は理想的なキャッピング剤になると考えられる。そこで、私たちは環状構造によるコンパクト化により反応性の向上を狙い、ethano N,N-dicylohexylphosphoramidite(EDCP)を開発した9)(図2)。EDCPはオリゴヌクレオチド合成において、高いキャッピング能に加えて、幾つかの特長を有しており、この度、富士フイルム和光純薬株式会社より販売されることとなった。本稿では、EDCPの性質や特長、オリゴヌクレオチド合成への適用について紹介したい。
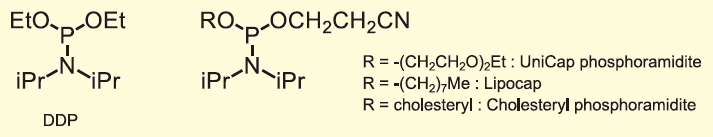

2 EDCPの性質と特長
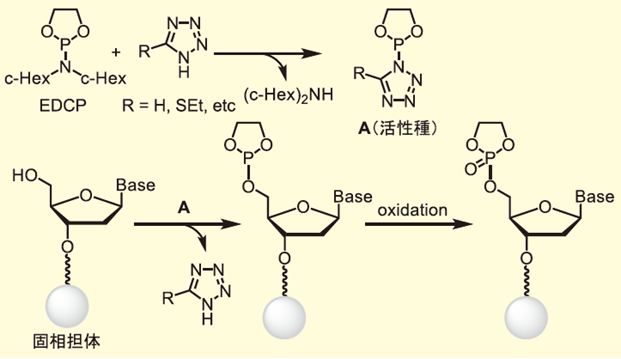
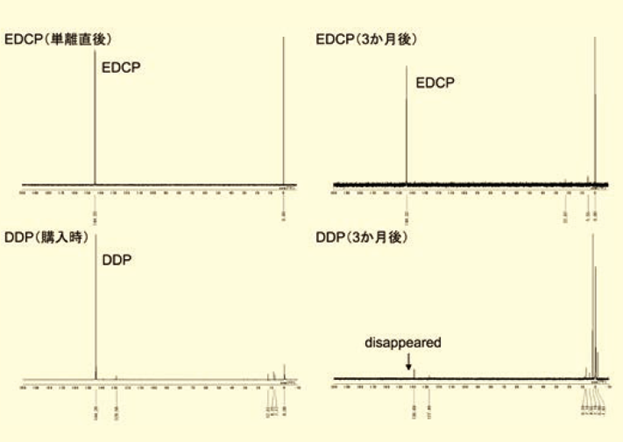
EDCP(図2)はコンパクトな5員環のジオキサホスホラン構造を有し、既存のホスホロアミダイト体よりも立体障害が小さいため、高い反応性を示すことが期待できる。一方で、EDCPはこれまで一般的なホスホロアミダイト体に利用されているジイソプロピルアミノ基と異なりジシクロヘキシルアミノ基をもつ。しかし、図3に示すように、EDCPによるキャッピングは通常のカップリング条件を利用することで1H-テトラゾールや5-エチルチオ- 1H-テトラゾール(ETT)などのアクチベーターとの活性種(A)形成時に除去されるため、そのキャッピング能に影響しないと推察される。このような構造の特徴をもつEDCPはMeCNに対して高い溶解性を示し、オリゴヌクレオチド合成(0.1 mol/LのMeCN溶液)に問題なく使用できる。詳細は後述するが、EDCPは標準的なDNA合成のカップリング条件を利用することで優れたキャッピング能を示す。また、EDCPは結晶性の固体(融点54-56℃)であるため、安定性が高く、必要量を量り取りやすい。実際、EDCPと液体であるDDPをそれぞれアルゴン封入下、室温で3か月放置したところ、31P NMRスペクトルからDDPは完全に分解しているのに対して、EDCPはほとんど変化していないことが分かる(図4)。

3 オリゴヌクレオチド合成におけるEDCPのキャッピング能
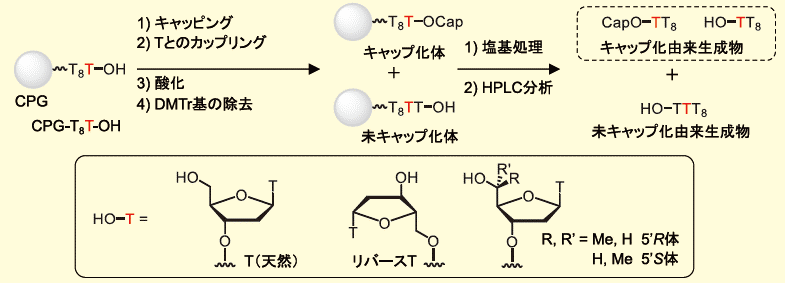
オリゴヌクレオチド自動合成機によりDMTr-offモードで予め合成したCPG-T8T-OH(T=T、リバースT、5′-C-Me-Tの5′R体と5′S体)を用いてEDCPのキャッピング能を評価した(図5)。評価手順としては、0.2μmol合成スケールで通常のDNA合成条件により、CPG-T8T-OHに対して、キャッピング→Tとのカップリング→酸化→DMTrの除去を行った注1。その後、塩基処理として28%アンモニア水、室温、2時間処理を行い、得られた粗成績体をHPLCにより分析した。なお、EDCPとDDPのキャッピングには、0.1 mol/LのMeCN溶液として、ETT(0.25 mol/LのMeCN溶液)を使った通常のDNAカップリング条件を用い、従来のキャッピング剤(Ac2O/N-メチルイミダゾール/ピリジン)では通常のキャッピング条件を用いた。本評価系では、キャップされたものは、9塩基長のチミジル酸(TT8)およびそのキャップ化アナログ(CapO- TT8)として検出されるのに対し、未キャップ体は10塩基長のチミジル酸(T TT8)の形で検出される。
注1: キャッピング能を評価するために、カップリングの前にキャッピングを行った。この系では、キャップ化されればTとのカップリングは起こらず、未キャップ化体のみがTとカップリングして、オリゴヌクレオチドが伸長する。
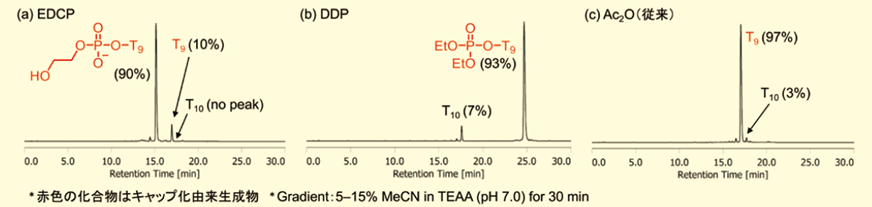
評価結果を表1に示す。天然のチミジン(T=T、CPG-T9-OH)に対するキャッピングにおいて、EDCPはDDPや従来のキャッピング剤(Ac2O)よりも高い反応性を示し、未キャップ体由来(T10)の生成物は全く確認されなかった(図6)。しかし、キャップ化由来生成物として、エチレングリコールが結合したT9とT9が確認された(図6a)。これらは塩基処理によって環状リン酸部に求核剤が攻撃した後、それぞれ、エンドサイクリック切断とエキソサイクリック切断により得られた生成物であると考えられる。一方、DDPではリン酸トリエステル体の形で存在している(図6b)。これは、28%アンモニア水、室温、2時間処理といった温和な条件10)に対して、非環状構造のリン酸トリエステル体は安定であることを意味している。しかし、EDCPで生じたエチレングリコールが結合したT9(Cap=CH2CH2OH、図5)はT9よりもさらに高極性であるため、実際のオリゴヌクレオチド合成(DMTr-onモード)ではカートリッジカラム精製において完全に除去できる(後述参照)。また、50 mM K2CO3/エチレングリコール、室温、4時間処理を行えば、エチレングリコールが結合したT9は消失し、全てT9として得ることができる。
また、EDCPはリバースTや5′R体、5′S体などのよりかさ高いヒドロキシ基(2級アルコール)に対しても高いキャッピング能を示す(表1)。5′- C-Me-Tでは、従来のAc2Oを用いる場合では、約半分が未キャップ体であり、DDPでも2割強の未キャップ体が残る。それに対して、EDCPは通常のDNAカップリング条件下で定量的なキャッピングを実現できる。
キャッピング剤の副反応の1つとして、グアニン塩基の6位酸素原子との反応による2,6-ジアミノプリン塩基への変換が知られている2)。そこで、EDCPをキャッピング剤として利用し、オリゴヌクレオチド合成に頻用される2種類の保護体{N2-イソブチリル体(dGiBu)とN2-イソプロピルフェノキシアセチル体(dGiPrPac)}を担持したCPGから10塩基伸長し、T10Gを合成した(図7)。この系では、グアニン塩基が10回キャッピング条件にさらされることになるが、HPLC上で2,6-ジアミノプリン塩基に変換された生成物は検出されず、EDCPによるグアニン塩基の修飾は認められなかった。

4 EDCPを使用したオリゴヌクレオチド合成
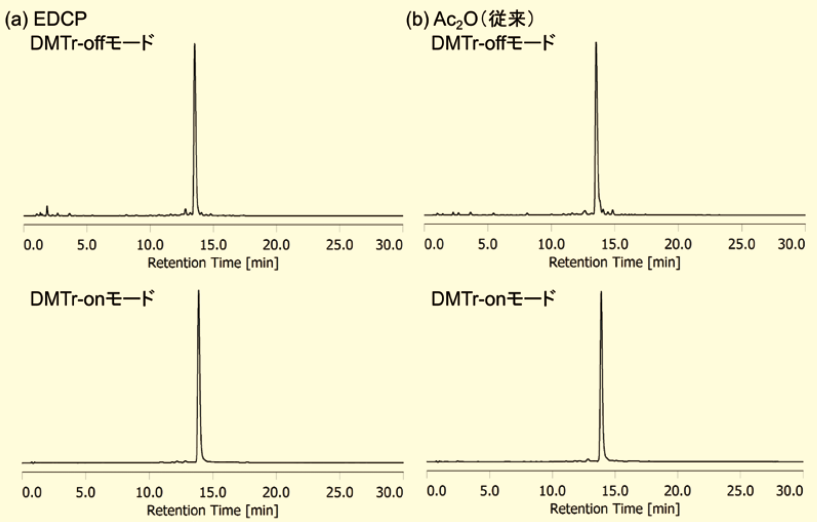
dABz、dGiBu、dCBz、Tのホスホロアミダイトを用いて、12塩基長のオリゴヌクレオチド(5′-GGAGTTCTCGT-3′)の0.2μmolスケール合成(DMTr-offモードとDMTr-onモード)を行った。合成は表2に示す試薬を用い、標準的なDNA合成条件に従った。なお、EDCPのキャッピングについては、DNAのカップリング条件を用いた。合成後は、28%アンモニア水、55℃、16時間の塩基処理を行い、DMTr-onモードでは、塩基処理後カートリッジカラムによる簡易精製を行った。結果、いずれのモードにおいても、従来のAc2Oを用いたキャッピングと同様、目的のオリゴヌクレオチドを高純度で得ることができた(図8)。
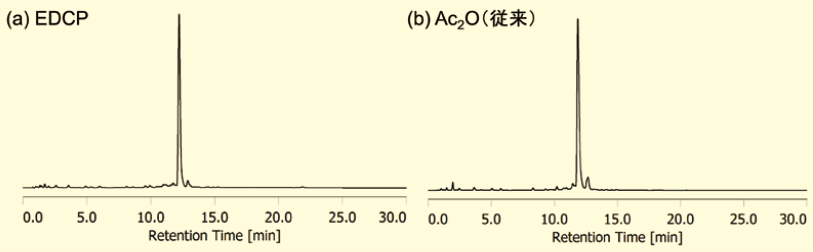
次に、修飾オリゴヌクレオチド合成を想定して、よりかさ高い基質である5′-ホスホロアミダイト体を用いたオリゴヌクレオチドのリバース合成(0.2 μmolスケール)を行った。リバースホスホロアミダイトのカップリングはRNAのカップリング条件、EDCPのキャッピングはDNAのカップリング条件を用いて、Tを担持したCPGから3′-GGAGTTCTCG-5′-5′-T-3′(イタリックはリバースヌクレオチド)を合成した結果、目的のオリゴヌクレオチドが高純度で得られることが明らかとなった(図9)。
また、2′-O-TBS保護のホスホロアミダイト体を用いてRNAを一部導入したDNAオリゴヌクレオチドの合成を試みた。合成条件として、DNAの合成条件を基に、EDCPを用いたキャッピングにDNAのカップリング条件、2′-O-TBS保護のホスホロアミダイト体のカップリングにRNAのカップリング条件、TBS基の脱保護に、Et3N・3HF/DMSO、65℃、2.5時間処理を行ったところ、目的のRNA含有オリゴヌクレオチドを首尾よく合成できることが確認された。このことから、EDCPはキャッピング剤として、RNA合成に適用できることが示唆された。

5 おわりに
以上、最近私たちが開発した環状ホスホロアミダイト型キャッピング剤EDCPについて紹介した。EDCPの構造は、オリゴヌクレオチドの合成時に使用するホスホロアミダイト体と基本的に同じであり、使用する反応条件もDNAのカップリング条件と同じである注2。そのため、本稿で紹介した以外に、オリゴヌクレオチド合成に利用されている様々な条件をそのまま利用でき、ホスホロチオエート修飾などの修飾核酸の合成にも適用できると考えられる。さらに、EDCPを用いることで、従来のAc2Oを用いたキャッピングに含まれる様々な試薬の影響を排除することができるため、より効率的なオリゴヌクレオチド合成に繋がることが期待される。オリゴヌクレオチド合成の際に、EDCPをぜひ試してみてください。
注2: 5′-C-Me体のようなかさ高い基質に対しても定量的にキャッピングできる(表1)。本稿ではアクチベーターとしてETTを用いたが、より酸性度の低い1H-テトラゾールを用いても十分なキャッピング能を有している可能性がある。
参考文献
- Cedillo, I. E. et al. : US 9403865 B2 (2016).
- Eadie, J. S. et al. : Nucleic Acids Res., 15, 8333 (1987).
- Masaki, Y. et al. : Sci. Rep., 12, 12095 (2022).
- Ren, Q. et al. : RSC Adv., 14, 21590 (2024).
- Yu, D. et al. : Tetrahedron Lett., 35, 8565 (1994).
- Glen Report 17.13 (September 2004).
- Natt, F. et al. : Tetrahedron, 53, 9629 (1997).
- Ren, Q. et al. : Tetrahedron, 150, 133773 (2024).
- Ito, Y. et al. : J. Org. Chem., 91, 2755 (2026).
- Glen Report 20.24 (October 2008).




