【連載】ペプチド医薬合成基礎講座 「第4回 環状ペプチド合成の新潮流」
本記事は、和光純薬時報 Vol.88 No.1(2020年1月号)において、サイエンスライター 佐藤 健太郎 様に執筆いただいたものです。
注目を受ける環状ペプチド
本連載の第1回で述べた通り、ペプチド医薬の可能性が改めて注目されている。低分子合成医薬は低コストかつ経口投与が可能であるなど多くの利点を持つが、昨今行き詰まりを指摘されている。また抗体医薬をはじめとしたバイオ医薬は製造コストが高くつき、経口投与は不可能である上、巨大分子であるタンパク質は細胞内に入り込めないことなどから、適用可能な疾患は限られている。ペプチド医薬が期待されるのは、この両者の「いいとこ取り」ができると考えられるためだ。
ただしペプチドとてアミノ酸が連結してできている以上、胃酸や消化酵素の攻撃で分解されてしまうことや、細胞膜の透過性が悪いといった問題は、タンパク質と変わりない。しかし、免疫抑制剤として用いられるシクロスポリンは、ペプチド骨格でありながらこれらの問題点をクリアし、経口投与で利用可能な医薬品となっている。
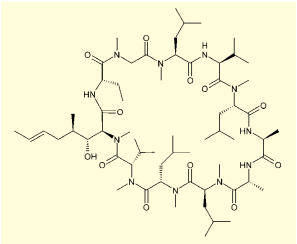
図1.シクロスポリン
これは、シクロスポリンがペプチドとしては特殊な構造を持つためだ。シクロスポリンは11のアミノ酸が環状骨格を成しており、N-メチルアミノ酸やD-アミノ酸など、通常のタンパク質には含まれないアミノ酸を多く含有する。このため消化酵素にペプチドと認識されにくく、攻撃を受け付けない。また、環状のしっかりした骨格で、N-メチル基によって脂溶性も上がっていることから、膜透過性が改善されると考えられる。
ただしこうしたペプチドは、合成難度が高いという問題がある。N-メチルアミノ酸は反応性が低く、通常の手法ではカップリングの効率が低下する。それ以上に問題なのは大環状骨格の形成で、有機合成の手法が大いに進んだ現代においても極めて厄介な問題として残されている。長い直鎖状の前駆体の両端が出合い、望み通りに反応する確率は低く、多量化が起こりやすくなる。これを防ぐためには、溶媒を多量に用いて環化を行う(高度希釈法)必要がある。
こうした事情のため、環状ペプチド骨格を持った化合物の合成は長時間・高コスト及び高い技術を要し、スクリーニングサンプルとして多数の化合物を供給するのは難しいと考えられてきた。
フレキシザイムによる環状ペプチド合成
こうした常識を覆し、多種多様な環状ペプチドの供給を可能にしたのが、菅裕明・東京大学教授らの開発した一連の技術だ。その手法は、既存のペプチド合成やタンパク質発現技術などとは全く異なる、極めて独創性の高いものだ。
よく知られている通り、DNAの持つ遺伝情報は3塩基が1組となり、1つのアミノ酸に対応するようになっている。この情報がmRNAに写し取られ、リボソームにおいて対応するタンパク質が合成される。この時、タンパク質の原料となるアミノ酸はtRNAに結合する形で運ばれ、リボソームにおいて連結されてゆく。
菅らは、人工的に「進化」させることで創り出したRNA触媒「フレキシザイム」を用い、tRNAに任意のアミノ酸を導入することに成功した1)。このtRNAを用いれば、天然の20種のアミノ酸に限らない、多様なアミノ酸(N-メチルアミノ酸やβ-アミノ酸を含む)を連結させることが可能になる。いわば、自然が創り出したタンパク質合成システムを改造してしまうことで、好きなアミノ酸鎖を合成するという手法だ。
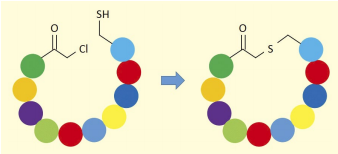
図2.クロロアセチル基とシステイン残基間の環化反応
ただしこれだけでは、単に珍しいアミノ酸を含んだ直鎖状ペプチドが得られるに過ぎない。そこで菅らは、N-クロロアセチルアミノ酸とシステインを導入する手法を考案した。両官能基は自発的に反応し、大環状骨格を持ったペプチドを与える。また、アルキン部位を持ったアミノ酸と、アジド基を持ったアミノ酸を導入することで、いわゆるクリック反応で環化を行うことも可能である。
またこの両者を併用することで、二環性骨格のペプチドの合成にも成功している。抗がん剤ロミデプシンなど、天然の生理活性物質に二環性骨格のペプチドが多く存在していることを考えれば、この手法は有用であろう。
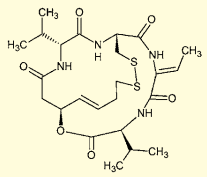
図3.ロミデプシン
ランダムな配列のDNAを多数用意すれば、これに対応した多様な環状ペプチドを一挙に作り出し、ライブラリを構築することができる。菅らはこうしたシステムを整備し、標的タンパク質に対して高い活性を示すペプチドを、素早く創出する強力な創薬プラットフォームを築き上げた2)。この技術をもとに設立されたバイオベンチャーであるペプチドリーム社は、内外の製薬企業と提携を進め、注目を集める存在となっている。
こうして得られたペプチドは、抗体に匹敵する基質特異性を示すものもあり、医薬候補化合物として十分な活性を示す。タンパク質間相互作用(PPI)の阻害など、合成低分子では難しい標的も、環状ペプチドでは対象になりうる。また、薬理作用を持った低分子を、標的タンパク質に親和性を持った環状ペプチドと結合させ、標的に送り込む「ペプチド-医薬複合体」(PDC)などの手法も研究されている。
環状ペプチドの化学合成
こうした生化学的手法でなく、化学合成による環状ペプチドの合成も、もちろん数多く研究されている。前述の通り、大環状骨格を形成する際には、分子間反応を防ぐために高度希釈法を用いる必要があり、この点がネックとなる。
そこで、ペプチドの側鎖部分を担体に結合させた後で必要なアミノ酸鎖を伸ばし、環化させた上で切り出す手法が試されている。ポリマーに担持させた状態で環化を行うため、二量化を防ぐことができるという考えだ。たとえばNicolasらは、固相上でPyBOP-HOAtによる環化反応を行い、環状ペンタペプチドをほぼ定量的に得ることに成功している3)。
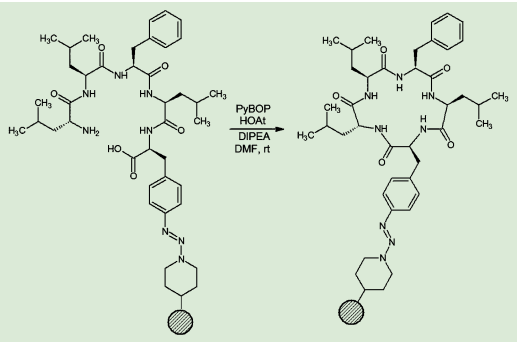
図4.固相上でのペンタペプチド環化反応
ただしこの方法では反応性が十分でなく、液相での高度希釈法の方がよい結果を与えるケースも少なくない。たとえばMalesevicらは、固相上での環化反応と、高度希釈法による液相での環化反応を比較し、前者が収率1%であったのに対し、後者では収率が36%であったケースを報告している4)。固相でも液相でも、環化の際に両端の反応点が近づくコンホメーションを取りうるか否かが重要と考えられる。
千葉らは、脂溶性タグを取りつけたペプチドが、THFなどの溶媒にはよく溶けるものの、高極性溶媒では沈殿してくることを利用し、効率的なペプチド合成技術(molecular hiving)を編み出している。この脂溶性タグは環化反応においても有効に働く。たとえばアミド窒素に対してタグを導入したヘプタペプチドは、低極性溶媒中でペプチド鎖部分が折り畳まれて、環化に有利なコンホメーションとなる。このため、ペプチドが20mMという比較的高濃度で反応を行っているにもかかわらず、収率よく環化反応が進行する5)。タグの存在により、この後の精製操作も簡便であり、トリフルオロ酢酸による処理でタグの除去も容易である。
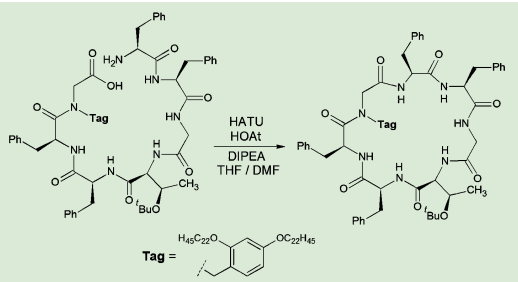
図5.脂溶性タグを活用した環化反応
大環状ペプチドはアミド結合のみで形成されるものでなく、シスチン結合のように側鎖を介した骨格のものも多数知られている。こうした骨格を、できるだけ簡便に構築しようという試みもなされている。たとえばKaleらのグループは、無保護のN末端アミノ基及びシステイン残基を持ったペプチドに対し、各種のビス求電子剤を作用させることで、効率よく大環状骨格を構築できることを報告している6)。
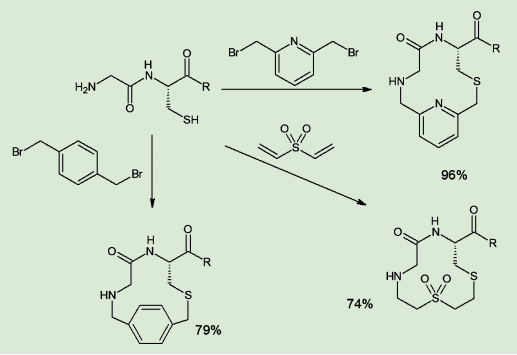
図6.ビス求電子剤による環化反応
ペプチド側、求電子剤側とも多様な化合物が適用可能であり、反応条件も比較的容易なものであるため、ライブラリ構築も可能である。また、合成された化合物の中から、プロテアーゼの一種であるトロンビンの阻害剤が見つかっているなど、医薬候補化合物としてのポテンシャルを備えた骨格といえよう。
その他、ネイティブケミカルライゲーション法を環化反応に適用する方法など、多くの手法が研究されている。環状ペプチドの医薬としての応用が注目を集めると同時に、その合成法も大いに進歩しており、今後さらに新たな手法が出てくることであろう。
参考文献
- Ohuchi, M. et al. : Curr. Opin. Chem. Biol., 11, 537 (2007). DOI: 10.1016/j.cbpa.2007.08.011
- 小嶋達矢 他:生物物理, 52, 4 (2012).
- Torres-Garcia, C. et al. : J. Org. Chem., 79 (23), 11409 (2014). DOI: 10.1021/jo501830w
- Malesevic, M. et al. : J. Biotechnol., 112, 73 (2004). DOI: 10.1016/j.jbiotec.2004.03.015
- Fujita, Y. et al. : Org. Lett., 15, 1155 (2013). DOI: 10.1021/ol4003477
- Kale, S. S. et al. : Sci. Adv., 5, eaaw2851 (2019). DOI: 10.1126/sciadv.aaw2851
関連記事









