【特別講座】ターボ Grignard 試薬の展開
本記事は、OrganicSquare Vol.44 (2013年6月号)において、サイエンスライター 佐藤 健太郎 様に執筆いただいたものです。

世紀の反応
エーテル溶媒に浸した金属マグネシウムに、ハロゲン化アルキルの溶液をゆっくりと滴下し、Grignard 試薬を生成させる。これは、有機合成化学者なら必ず経験する実験であろう。筆者も初めて Grignard 試薬を作った際には、先輩に見守ってもらいながら、反応が暴走しないようにおっかなびっくりで実験を行ったことをよく覚えている。無事実験を終えた後、何か化学者としてひとつステップを上がったようで、少し誇らしい気持ちになったものであった。
実際、Grignard 試薬の生成は、有機合成化学の一丁目一番地というべきものであり、誰もが身につけておくべきテクニックだろう。試薬メーカーから多くの Grignard 試薬が売り出され、容易に手に入るようになった今も、その重要性に変わりはない。
V. Grignard によってこの反応が報告されたのは 1900 年、その功績でノーベル化学賞が授与されたのは 1912 年のことだ。しかし Grignard 試薬は、一世紀以上を経た今も最も使用頻度の高い有機合成手法の一つであり続けている。人名反応は数あれど、これだけ長きにわたって化学者に愛用されている反応は、他にほとんど例を見ない。
Grignard 試薬は単に息が長いというだけでなく、様々な応用がなされ、有機合成化学の発展に大きな寄与をしている点でも傑出している。銅塩を併用する Michael 付加反応、パラジウム触媒を用いるクロスカップリングなどは、そのよい例だろう。
そして近年の大きな進歩としては、P. Knochel らによる「ターボ Grignard 試薬」の開発が挙げられる。これは Grignard試薬の用途をさらに広げる方法論として、大きな注目を浴びている。今回は、その生成と性質についてご紹介したい。
Grignard 試薬の限界
Grignard 試薬は、R-MgX の式で表される。R に当たる置換基としては、アルキル・アルケニル・アルキニル・アリールなど、幅広い範囲の化合物が使用可能である。また求電子剤の方も、アルデヒド・ケトン・エステル・ニトリル・アミドなどなど、様々な官能基が利用できる。この守備範囲の広さが、Grignard 試薬が長らく使われてきた大きな要因といえる。
しかしこれは裏を返せば、基質が制限されることにもつながる。すなわち、エステルやニトリルなどの官能基が含まれる化合物は、自己反応してしまうために Grignard 試薬側としては利用できない。また、一部のヘテロ環化合物などにも、直接マグネシウムを作用させても分解してしまい、Grignard試薬を生成できないものがある。このため従来 Grignard 試薬の生成には、構造が比較的シンプルなハロゲン化アルキル・ハロゲン化アリールなどが用いられるケースがほとんどであった。Knochel によるターボ Grignard 試薬の大きなポイントは、この限界を破ることに成功した点にある。
ターボ Grignard 試薬の登場
前述のように、Grignard 試薬生成には、ハロゲン化物とマグネシウムの反応によるのが最も一般的である。これと別に、ハロゲン-金属交換反応によって Grignard 試薬を作る方法もある。すなわち、ハロゲン化物(R-X)と Grignard 試薬(R'-MgX)を混合しておくと、交換反応が起きて R-MgX という化学種が生成してくる。
この反応は比較的高い温度を必要とし、基質の分解など副反応を起こしやすい。しかし Knochel らは、この反応の際にリチウム塩を共存させておくと、交換が低温でも素早く進むことを発見した。条件を最適化した結果、イソプロピルマグネシウムクロリドと塩化リチウムの錯体(iPrMgCl・LiCl)を、ハロゲン化アルケニルまたはハロゲン化アリールと低温(-40℃)で反応させることで、対応するアルケニル及びアリール Grignard 試薬が効率よく得られることが判明した 1)。
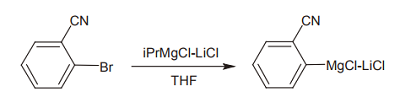
この iPrMgCl・LiCl は、高速で交換反応を起こすため、「ターボ Grignard 試薬」と通称される(場合により、イソプロピルでなく sec-ブチルマグネシウムクロリドが用いられるケースもある)。リチウムイオンの存在によって Grignard 試薬の会合状態が分解されること、リチウムが結合することによって、マグネシウムが負電荷に近い性質を帯び、求核性が向上することなどが高い反応性の原因と考えられている。
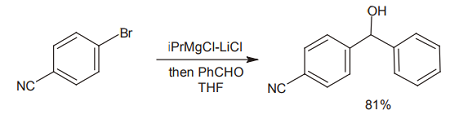
このターボ Grignard 試薬は、低温で生成させることができ、この温度ではエステル・ニトリルなどの比較的求電子性の低い官能基とは反応しない。これにより、たとえば下図のような基質から対応する Grignard 試薬を生成させ、その後でアルデヒドを加えてやれば、分子内のニトリル部分は無傷のままに付加体を得ることが可能になる。今までであれば、ニトリル部分をあとで導入するか、別の形にいったん変換しておき、Grignard 反応の後に酸化してニトリルに戻すといった手順が必要であった。すなわちターボ Grignard 試薬の導入は、合成工程数の大幅な短縮につながる。
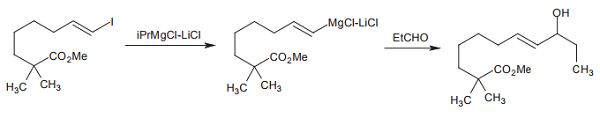
同様に、ヨウ化アルケニルにターボ Grignard 試薬を作用させることで、対応する Grignard 試薬を生成させることもできる。こちらでも、分子内のエステルなどの官能基は影響を受けない 2)。
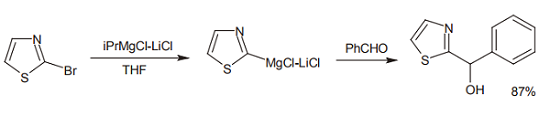
通常 Grignard 試薬を作りにくいヘテロ環化合物なども、同様に反応する。たとえば 3,5-ジブロモピリジン、3-ブロモチオフェン、2-ブロモチアゾールなども、ターボ Grignard 試薬と交換反応し、アルデヒドとの付加体を収率よく与える1)。
直接法
塩化リチウムは、ハロゲン-金属交換のみならず、通常の Grignard 試薬生成においても有効である。削状あるいは粉末状の金属マグネシウムと、塩化リチウムを THF に加え、ここにハロゲン化アリールの溶液を滴下すると、通常の条件(塩化リチウムがない場合)よりもずっと低温で、Grignard 試薬が生成する。
例えば下図の例では、-20℃、60 分で反応が進行する 3)。
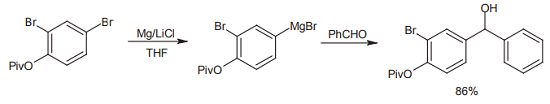
ターボ Grignard 試薬を用いる場合同様、この条件でエステルやニトリルなどの官能基は影響を受けない。得られた試薬は、アルデヒドなどの各種求核剤と反応する他、後述するようにクロスカップリング反応などに用いることもできる。
C-H 引き抜きによる Grignard 試薬生成
有機金属化合物の生成法としては、C-H 結合を強塩基で引き抜き、メタル化する方法もよく用いられる。Knochel らは、ここまでのターボ Grignard 試薬の知見を生かし、C-H 引き抜きによる Grignard 試薬の生成法も報告している 4)。彼らは塩基として、2,2,6,6-テトラメチルピペリジン(TMP)とターボ Grignard 試薬 iPrMgCl・LiCl から合成されるマグネシウムアミドを用いている。この試薬は、Knochel-Hauser 塩基とも呼ばれる。
この TMPMgCl・LiCl は、ピリジンやイソキノリンなど各種ヘテロ環化合物を、直接 Grignard 試薬に変える。これら電子不足ヘテロ環の場合、多くは窒素に隣接する C-H 水素が引き抜かれる。またベンゼン環の場合は、ピリジンやエステルなどが directing group となり、これらに隣接する水素が置換される。これらの反応の際には、ハロゲン元素がついていてもこれとは反応せず水素原子だけを引き抜くなど、ターボ Grignard 試薬とは異なる挙動を示す。
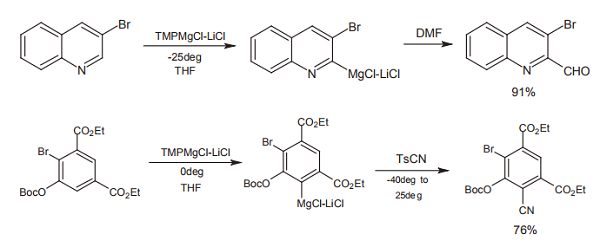
他の金属との組み合わせ
ターボ Grignard 試薬によって生成させた各種 Grignard 試薬は、他の金属へとトランスメタル化し、様々なカップリング反応に用いることができる。たとえば CuCN・2LiCl を加えて銅にトランスメタル化を行い、ハロゲン化アルキルとカップリングさせることができる。同様に、銅にトランスメタル化させた上で酸塩化物と反応させれば、収率よくケトンが得られてくる 1)。
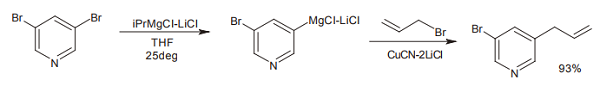
また、パラジウム触媒を用いて、ハロゲン化アリールなどとクロスカップリングを行うこともできる。ただしこの場合、生成した Grignard 試薬に塩化亜鉛(Ⅱ)を加え、いったん亜鉛上にトランスメタル化した上で、カップリングを行う必要がある 5)。
さらに最近になり、インジウムを用いる、より簡便なクロスカップリング反応が報告された 6)。削状マグネシウム、塩化リチウム、塩化インジウム(Ⅲ)を THF に加え、ここに室温でハロゲン化アリールまたはハロゲン化ベンジル溶液を滴下していくと、有機インジウム化合物が生成する。ここにハロゲン化アリールとパラジウム触媒を加えることで、クロスカップリングが行える。
ハロゲン化アリール同士を、比較的簡単な操作でクロスカップリングできるわけだから、合成的な価値は極めて高い。基質にエステル・アミド・アミノ・ニトロ・ニトリルなどの官能基が含まれていても、問題なくクロスカップリングが行える点でも優れている。
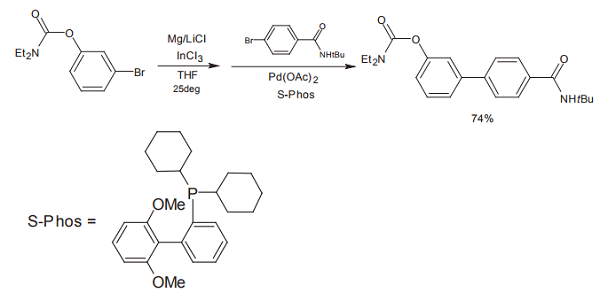
一世紀にわたって有機合成化学を支えてきた Grignard 試薬は、ここに至ってまた新たな生命を吹き込まれたといえる。
その後もターボ Grignard 試薬は多様な展開を見せており、適用範囲も着々と広がっている。iPrMgCl・LiCl や s-BuMgCl・LiCl といった試薬は入手も容易で、旧来の Grignard 試薬に比べてずっと操作が簡便であるのも、特筆すべき点といえるだろう。穏和な条件下に炭素-炭素結合生成が行えるこの試薬は、すべての合成化学者が活用可能なものであり、記憶に値するものといえるであろう。
参考文献
- Krasovskiy, A., Knochel, P.:Angew. Chem. Int. Ed., 43, 3333 (2004). DOI: 10.1002/anie.200454084
- Ren, H., Krasovskiy, A., Knochel, P.:Org. Lett., 6, 4215 (2004). DOI: 10.1021/ol048363h
- Piller, F. M. et al.:Angew. Chem. Int. Ed., 47, 6802 (2008). DOI: 10.1002/anie.200801968
- Krasovskiy, A. et al.:Angew. Chem. Int. Ed., 45, 2958 (2006). DOI: 10.1002/anie.200504024
- Piller, F. M. et al.:Angew. Chem. Int. Ed., 47, 6802 (2008). DOI: 10.1002/anie.200801968
- Bernhardt, S. et al.:Chem. Eur. J., 19, 828 (2013). 10.1002/chem.201203795




