【総説】カーボンナノチューブに内包させて用いる増感色素の開発
本記事は、和光純薬時報 Vol.87 No.2(2019年6月号)において、山口大学大学院 創成科学研究科 三宅 秀明様、岡山大学大学院 環境生命科学研究科 田嶋 智之様、高口 豊様に執筆いただいたものです。
はじめに
半導体性を示す単層のカーボンナノチューブ(SWCNTs)は、優れた光吸収特性も併せ持つため光電変換デバイスへの応用が期待されている。ただし、単純にSWCNTsに光照射したとしても、大きな励起子束縛エネルギーのため光電変換を実現することは困難である1-3)。そこで、優れた電子アクセプターであるフラーレンと複合化したシステムが精力的に研究されている4-8)。励起電子をフラーレンで抽出することで効率的な光誘起電子移動が実現できるためである。
しかし、近年Flavelらによる精密な検討によって、SWCNT/C60システムにおける重大な課題が明らかとなった9)。SWCNTsとC60のヘテロ接合を利用した太陽電池の場合、半径の小さいSWCNTsでは高い量子効率で発電するものの、半径が大きくなるほど効率は低下し、0.95 nm以上ではほぼ0となってしまったのである。近年、カーボンナノチューブの合成法は著しく発展しており、大量生産にも成功しつつあるが、比較的安価な製品には直径が1 nmを超えるものが多い。もし直径0.95 nm以下のSWCNTsに使用が限られるとすれば、カーボンナノチューブ系光電変換デバイスの実用性は限られてしまう。一方、何らかの方法によってこの限界を打破することができれば、実用化への起爆剤となり得る。
このような背景の中、我々はSWCNTsに増感色素を内包させることで、上記の限界打破に成功した10)。すなわち、直径が約1.4 nmのSWCNTsを用いて、水からの効率的な光触媒的水素製造を達成した。これまでに、内包色素の光励起からSWCNTsへのエネルギー移動は報告されていたが11-14)、光誘起電子移動についてはこれが初めての実証例となった。本稿ではその内容について紹介する。
増感色素の設計・合成およびSWCNTへの内包
まず、SWCNTsに内包させる色素の分子設計を行った。色素分子はSWCNTsの限られた空間に導入する必要があるため、出来る限りコンパクトなサイズであることが望まれる。また、内包色素からの光誘起電子移動を実現するためには、光励起によって分子内電荷分離を起こしやすいドナー・アクセプター構造が必要であると考えた。それらの要件を勘案して、電子供与性の高いフェロセンと電子受容性の高いチオカルボニル基を有する色素を設計した(図1a)。具体的には、チオフェンとベンゾチアジアゾールからなるπ共役系を中心とした色素1を目的分子と設定し、チオフェン誘導体3を出発原料として、直接アリール化反応および硫化反応によって合成した15)(図1b)。
色素1とその前駆体2の違いはチオカルボニル(C=S)とカルボニル(C=O)の違いのみであり、分子形状はほぼ同じである。しかし、その性質には顕著な違いが見られた。化合物2の極大吸収波長は455 nm(ε = 2.60 x 104)であり橙色を呈するのに対して、色素1は極大吸収波長508 nm(ε = 2.36 x 104)を中心として幅広く可視光を吸収し、濃い赤紫色を呈する(図1c)。C=O結合に比べてC=S結合の方がHOMO-LUMOギャップが小さいため、このような変化がもたらされたと考えられる。
化合物1および2はいずれもサイクリックボルタンメトリーにおいて可逆な酸化還元挙動を示すが、その酸化還元電位(vs Fc/Fc+)にも差異がみられた(1: Eox = 0.20 V, Ered = -1.57 V; 2: Eox = 0.10 V, Ered = -1.35)。
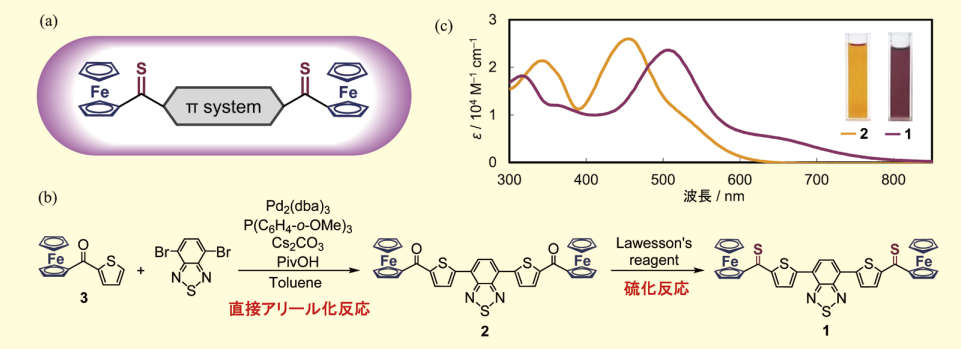
図1.
(a) 設計した増感色素分子, (b) 色素1の合成, (c) 色素1および化合物2の吸収スペクトル(1,1,2,2-テトラクロロエタン溶液)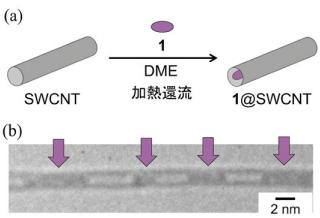
図2.
(a) SWCNT内部空間への色素1導入, (b) 1@SWCNTのTEM画像SWCNTs内部空間への色素導入は、有機溶媒中で加熱還流することによって行った。具体的には、SWCNTsと色素1の混合物に1,2-ジメトキシエタン(DME)を加え、3時間加熱還流を行った後、クロロホルムで繰り返し洗浄することで余分な色素1を除去し、目的の色素内包SWCNTs(1@SWCNT)を得た(図2(a))。
得られた1@SWCNTを透過型電子顕微鏡(TEM)で観察したところ、カーボンナノチューブの内部に色素分子が内包されている様子が確認された(図2(b))。
増感色素内包型 SWCNTs光触媒の調整
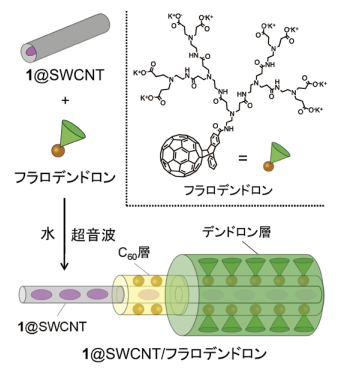
図3.
1@SWCNTとフラロデンドロンの複合体我々はこれまでに、フラーレンに親水性のデンドリマー部位を結合させたフラロデンドロンを独自に開発しており16)、その特性を活かしたSWCNT光触媒による水からの水素製造を達成してきた17-21)。これまでに用いたSWCNTsの直径は1 nm以下のものであったが、今回開発した増感色素による効果を明らかにするため、直径が約1.4 nmであるSWCNTsを用いた光触媒について検討した。
まず、SWCNTsとフラロデンドロンの混合物に水を加え、超音波照射を行うことで、複合体SWCNT/フラロデンドロンの分散液を得た。増感色素を内包させたSWCNTsについても同様の操作を行い、対応する複合体1@SWCNT/フラロデンドロンを得た(図3)。得られた複合体は、色素内包SWCNTを中心とするナノ同軸ケーブル構造を形成して水中に分散していると考えられる。
得られた分散液(SWCNT/フラロデンドロンと1@SWCNT/フラロデンドロン)の吸収スペクトルを測定し、900 nmの値で規格化して比較した(図4)。それらの差スペクトルは色素1の吸収スペクトルと類似しており、内包された色素1による吸収であることが示唆された。色素内包によって吸収帯が長波長側にブロードニングしているが、これは他の色素内包SWCNTsにも見られる現象であり、その要因は分散力によって色素分子とSWCNTsが相互作用するためと考えられる11, 12)。
得られたSWCNT複合体に、電子リレー分子としてメチルビオローゲン(MV2+)、犠牲電子ドナーとして1-ベンジル-1,4-ジヒドロニコチンアミド(BNAH)、助触媒としてポリ(N-ビニル-2-ピロリドン)保護白金ナノ粒子(PVP-Pt)を加え、光触媒を調製した。
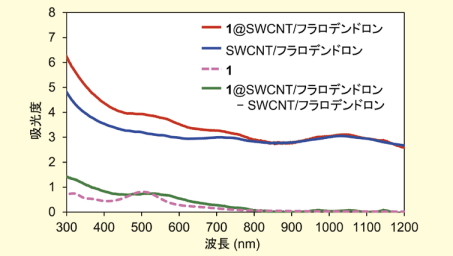
図4.可視近赤外吸収スペクトル
1@SWCNT/フラロデンドロン(赤)およびSWCNT/フラロデンドロン(青)の重水分散液, 色素1の1,1,2,2-テトラクロロエタン溶液(ピンク破線), 1@SWCNT/フラロデンドロンとSWCNT/フラロデンドロンの差スペクトル(緑)光触媒的水素発生実験の結果
前述の通り、今回用いるSWCNTsの直径(約1.4 nm)はFlavelらによって示された太陽電池への適用限界の値(0.95 nm)を大幅に超過しているため、SWCNTsの励起による光誘起電子移動は起こらないことが予想される。一方、SWCNTsに内包された色素の励起による光誘起電子移動が起こる可能性がある。そこで、色素1内包型(1@SWCNT/フラロデンドロン)と非内包型(SWCNT/フラロデンドロン)の両者について光触媒的水素発生実験を行い、その活性を比較した。
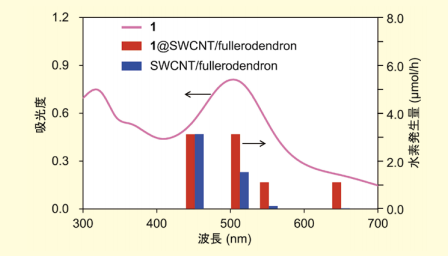
図5.
色素1の吸収スペクトル(1,1,2,2- テトラクロロエタン溶液)と SWCNT 光触媒による水素生成量のアクションスペクトル実験から得られた水素発生量のアクションスペクトルを、色素1の吸収スペクトルとあわせて図5に示した。各光触媒システムに波長450 nmの単色光を照射した場合、水素の発生量について色素1内包型(3.1 µmol/h)と非内包型(3.4 µmol/h)に大きな差は見られなかった。これは、この波長領域においてはC60が光吸収体として作用しているためと考えらえる。しかし、C60がほとんど光吸収しない波長500 nm以上の領域においては、顕著な差が表れた。すなわち、非内包型の場合には水素の発生量は比較的少なかったが(510 nm: 1.7 µmol/h; 550 nm: 0.15 µmol/h; 650 nm: 0.011 µmol/h)、色素1内包型ではより多く水素が発生した(510 nm: 3.2µmol/h; 550 nm: 1.2 µmol/h; 650 nm: 1.3 µmol/h)。この光触媒活性の増加は色素1の吸収スペクトルの蛍光と一致している。したがって、色素1の吸収によって光誘起電子移動が進行し、水素が発生したと考えられる。
増感色素による光触媒的水素発生のメカニズム
図6(a)には、本光触媒システムに関わる物質のエネルギー準位図を示した。SWCNTsは複数のヘリシティの混合物を用いているが、代表的な(13,8)SWCNTの伝導体(C1, C2)および価電子帯(V1, V2)を示してある。内包された色素1が光を吸収すると、電子が励起されてLUMOへと遷移する。そして、励起電子は1のC60へ、ホールはSWCNTのV1バンドへと移動すると考えられる。
この過程によって生成する電荷分離状態1@SWCNT+·/C60-·が本システムの鍵となる。図6(b)に示した反応機構に沿って上記の過程を説明すると、最初の段階は内包色素1の光吸収による励起である(1→1*)。次に、励起電子がC60へ、ホールがSWCNTsへ移動することによって電荷分離状態1@SWCNT+·/C60-·が生成する。その後、1@SWCNT+·/C60-·のホールはBNAHを酸化し、電子はMV2+を経由して白金助触媒へと移動し、水素を発生させる。以上をもって基底状態 1@SWCNT/C60 が再生し、触媒サイクルが完結する。
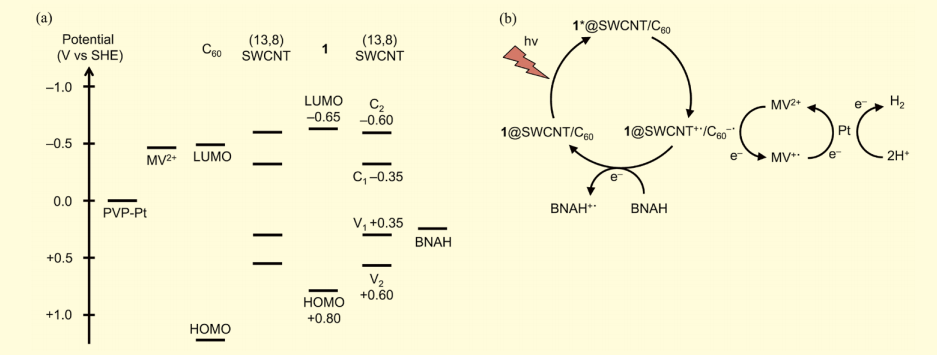
図6.
(a) 色素内包型 SWCNT 光触媒のエネルギー準位図,(b) 色素内包型 SWCNT 光触媒による水素生成の反応機構実際に、BNAH と MV2+ の存在下 1@SWCNT/C60 に光照射(波長 650 nm)を行ったところ、MV2+ の還元による MV+·の生成が確認できた。一方、1 を内包していない場合には MV+·の生成が見られなかったため、色素 1 によって光誘起電子移動が起きていることが明らかとなった。
おわりに
今回我々は、SWCNTs に内包させて用いる増感色素を新たに開発した。その色素を内包させた SWCNTs を光触媒に活用することで、水素生成における増感効果を実証した。これはSWCNTs に内包された分子による光誘起電子移動を初めて実証した事例である。また、光電変換デバイスに応用する際の限界直径(0.95 nm)を大幅に超える SWCNTs(直径約 1.4 nm)を用いて活性向上を実現できたことは、実用上極めて意義深い。今回は水素生成用光触媒に応用したが、他の光触媒や太陽電池も基本原理は類似しているため、様々な応用研究への展開が期待される。
謝辞
本研究の一部は、岡山県特別電源所在県科学技術振興事業の研究委託、JSPS 科 研 費 15H03519、16K05895、17K14448、文部科学省地域産学官連携科学技術振興事業費補助金地域イノベーション戦略支援プログラム(研究機能・産学集積高度化地域)、やまぎん地域企業助成基金、中国電力技術研究財団、宇部興産学術振興財団、大阪新薬株式会社との共同研究からの助成を受けて実施された。
キーワード
光誘起電子移動
物質が光エネルギーを吸収し、励起されたことにより起こる電子移動。結果的に励起電子とホールが離れることで電荷分離状態が生成する。太陽電池や光触媒の根幹を成す現象である。
増感色素
光化学反応や太陽電池などにおいて、上記の光誘起電子移動を促進させるために添加する色素。光に対する感度を向上させる効果がある。
参考文献
- Wang, F., Dukovic, G., Brus, L. E. and Heinz, T. F. : Science, 308, 838 (2005). DOI: 10.1126/science.1110265
- Dukovic, G., Wang, F., Song, D., Sfeir, M. Y., Heinz, T. F. and Brus, L. E. : Nano Lett., 5, 2314 (2005). DOI: 10.1021/nl0518122
- Maultzsch, J., Pomraenke, R., Reich, S., Chang, E., Prezzi, D., Ruini, A., Molinari, E., Strano, M. S., Thomsen, C. and Lienau, C. : Phys. Rev. B, 72, 241402 (2005). DOI: 10.1103/PhysRevB.72.241402
- Bindl, D. J., Wu, M.-Y., Prehn, F. C. and Arnold, M. S. : Nano Lett., 11, 455 (2011). DOI: 10.1021/nl1031343
- Jain, R. M., Howden, R., Tvrdy, K., Shimizu, S., Hilmer, A. J., McNicholas, T. P., Gleason, K. K. and Strano, M. S. : Adv. Mater., 24, 4436 (2012). DOI: 10.1002/adma.201202088
- Ramuz, M. P., Vosgueritchian, M., Wei, P., Wang, C., Gao, Y., Wu, Y., Chen, Y. and Bao, Z. : ACS Nano, 6, 10384 (2012). DOI: 10.1021/nn304410w
- Gong, M., Shastry, T. A., Xie, Y., Bernardi, M., Jasion, D., Luck, K. A., Marks, T. J., Grossman, J. C., Ren, S. and Hersam, M. C. : Nano Lett., 14, 5308 (2014). DOI: 10.1021/nl5027452
- Blackburn, J. L. : ACS Energy Lett., 2, 1598 (2017). DOI: 10.1021/acsenergylett.7b00228
- Pfohl, M., Glaser, K., Graf, A., Mertens, A., Tune, D. D., Puerckhauer, T., Alam, A., Wei, L., Chen, Y., Zaumseil, J., Colsmann, A., Krupke, R. and Flavel, B. S. : Adv. Energy Mater., 6, 1600890 (2016). DOI: 10.1002/aenm.201600890
- Murakami, N., Miyake, H., Tajima, T., Nishikawa, K., Hirayama, R. and Takaguchi, Y. : J. Am. Chem. Soc., 140, 3821 (2018). DOI: 10.1021/jacs.7b12845
- Yanagi, K., Iakoubovskii, K., Kazaoui, S., Minami, N., Maniwa, Y., Miyata, Y. and Kataura, H. : Phys. Rev. B, 74, 155420 (2006). DOI: 10.1103/PhysRevB.74.155420
- Yanagi, K., Iakoubovskii, K., Matsui, H., Matsuzaki, H., Okamoto, H., Miyata, Y., Maniwa, Y., Kazaoui, S., Minami, N. and Kataura, H. : J. Am. Chem. Soc., 129, 4992 (2007). DOI: 10.1021/ja067351j
- Loi, M. A., Gao, J., Cordella, F., Blondeau, P., Menna, E., Bartova, B., Hebert, C., Lazar, S., Botton, G. A., Milko, M. and Ambrosch-Draxl, C. : Adv. Mater., 22, 1635 (2010). DOI: 10.1002/adma.200903527
- Okazaki, T., Iizumi, Y., Okubo, S., Kataura, H., Liu, Z., Suenaga, K., Tahara, Y., Yudasaka, M., Okada, S. and Iijima, S. : Angew. Chem., Int. Ed., 50, 4853 (2011). DOI: 10.1002/anie.201007832
- Miyake, H., Tajima, T. and Takaguchi, Y. : Chem. Lett., 46, 48 (2017). DOI: 10.1246/cl.160866
- Takaguchi, Y., Sako, Y., Yanagimoto, Y., Tsuboi, S., Motoyoshiya, J., Aoyama, H., Wakahara, T. and Akasaka, T. : Tetrahedron Lett., 44, 5777 (2003). DOI: 10.1016/S0040-4039(03)01425-4
- Tajima, T., Sakata, W., Wada, T., Tsutsui, A., Nishimoto, S., Miyake, M. and Takaguchi, Y. : Adv. Mater., 23, 5750 (2011). DOI: 10.1002/adma.201103472
- Sasada, Y., Tajima, T., Wada, T., Uchida, T., Nishi, M., Ohkubo, T. and Takaguchi, Y. : New J. Chem., 37, 4214 (2013). DOI: 10.1039/C3NJ00790A
- Murakami, N., Tango, Y., Miyake, H., Tajima, T., Nishina, Y., Kurashige, W., Negishi, Y. and Takaguchi, Y. : Sci. Rep., 7, 43445 (2017). DOI: 10.1038/srep43445
- Kurniawan, K., Tajima, T., Kubo, Y., Miyake, H., Kurashige, W., Negishi, Y. and Takaguchi, Y. : RSC. Adv., 7, 31767 (2017). DOI: 10.1039/C7RA05412B
- Kurniawan, K., Murakami, N., Tango, Y., Izawa, T., Nishikawa, K., Watanabe, K., Miyake, H., Tajima, T. and Takaguchi, Y. : Proc. Nat. Res. Soc., 1, 01004 (2017).




