【総説】パーキンソン病とその関連疾患の血液バイオマーカーとしての血中カフェイン濃度の有用性
本記事は、和光純薬時報 Vol.92 No.1(2024年1月号)において、国立研究開発法人量子科学技術研究開発機構 量子医科学研究所 脳機能イメージング研究部 徳田 隆彦様に執筆いただいたものです。
1.パーキンソン病の客観的なバイオマーカーの必要性とその開発研究の現状
パーキンソン病(PD)は有病率が10万人あたり約150人に上る我が国で2番目に多い神経変性疾患であり、また加齢によって有病率が増加し後期高齢者では100人に2〜3人が発症する。PD患者脳に生じている特異的な生化学的・病理学的異常を反映する客観的なバイオマーカー(BM)が必要である。著者らは世界で最初にPDの原因蛋白と考えられているα-synuclein(α-syn)1)およびそのoligomer2)をヒト髄液中で定量できるELISA系を開発して報告している。ただ、現在のところ、血液BMに関しては、有用性・汎用性が確立されたBMは存在していない。最近の画期的な研究成果として、順天堂大学脳神経内科 奥住・波田野らのグループが、免疫沈降法(IP)とRT-QuIC(Real-time quaking-induced conversion)法を組み合せた方法(IP/RT-QuIC法)によって、患者血清中のα-synシード(シードは蛋白凝集の核となる分子会合体)を検出し、それによってPD/多系統萎縮症(MSA)とコントロールとを高い精度で鑑別できることを、2023年6月に報告した3)。RT-QuIC法が、シヌクレイノパチーの診断において優れた診断能を有することを、筆者らを含む複数のグループが報告しているが4)、RT-QuIC法は試薬と実験条件の厳密な調整が必要で、その安定した実施には熟練を要し、広く施行できる方法ではない。
2.Metabolomics解析によるパーキンソン病の血液バイオマーカー探索―カフェインの同定
候補分子にとらわれず、対象とする組織・体液中の分子を網羅的に解析し、疾患群と対照群の比較を行うUnbiased/Non-targeted analysisも疾患BMの探索には有用である。特に、全ての蛋白分子・転写産物・代謝産物情報を網羅的に収集・解析する手法はそれぞれProteomics、Transcriptomics、Metabolomicsと呼ばれ、こうした技術を用いたBM探索はオミックス(Omics)アプローチと総称される。その中で、代謝産物に対する解析(Metabolomics)について、著者らは、順天堂大学の服部信孝教授が代表となって2014年10月~2020年3月まで行われたAMED-CREST研究(「疾患における代謝産物の解析および代謝制御に基づく革新的医療基盤技術の創出」研究)を行った。この研究では、PD患者に特異的な代謝変化をバイオマーカーとして同定・検証すること、および同変化を是正する創薬シーズを同定することを目的として、PD患者およびコントロールを対象としたMetabolomics解析研究を実施した。その結果、複数のPD患者コホートの血液サンプルにおける網羅的/特定パスウェイ代謝産物解析により、順天堂大学の藤巻・波田野らは、ヒト血漿中のカテコラミン代謝、カフェイン・キサンチン代謝・酸化還元代謝に関連する複数のPD特異的代謝産物を報告した5)。一般的に、Metabolomics解析はProteomics解析と同様に新規のBM候補の同定によってその対象疾患の新たな病態メカニズムが明らかになる可能性があるという長所を有しているが、再現性が課題である。ただ、血中カフェイン濃度については、波田野らは異なるPDコホートでも血中カフェイン濃度が低下していたことをすでに報告している6)ので、その再現性は確認されている。また、網羅的なMetabolomics解析は、新規のBMの同定には有用であるが、個々の患者に対する臨床検査として使用するには労力と費用がかかりすぎるために、Metabolomics解析から得られた個別のBMの定量系を別途に開発することが必要になる。カフェインについても、著者らは、血中カフェインのELISA法による測定系を構築している(後述)。
上記の藤巻らの報告では、PD患者ではカフェインおよびその代謝産物8種が低下しており、その代謝関連酵素をコードする遺伝子にPD特異的なSNPを認めず、さらにPD群ではコントロール群に比し内服カフェイン量と血中濃度の相関が弱いことから、PD患者の小腸ではカフェイン吸収能低下が生じていると考えられた5)。以上から、血中カフェイン濃度は、確度の高い診断バイオマーカーとして臨床応用が可能なだけでなく、カフェインの経口以外の経路での投与・その誘導体による治療介入が有用である可能性が示された。さらに順天堂大学グループは、進行性核上性麻痺・MSA患者血清でも、PD同様にカフェイン・カフェイン関連代謝産物全てが低下していることを報告している7)。
3.パーキンソン病とカフェインの関連性
疫学的報告から、カフェイン含有飲料の定期摂取がPD発症抑制効果を示すことが確立されている8)。米国食事摂取基準2015年版の諮問委員会の報告書では、コーヒー摂取とPD発症のリスク低下との関連は、中等度のレベルの科学的根拠をもって確認されていると記されている9)。この報告書の根拠となった2014年のメタ解析の報告によると、コーヒーの1日3杯程度(コーヒー1杯あたり約60mgのカフェインが含まれている)の摂取で最もリスクが低下し(相対危険度0.71;95%信頼区間0.64~0.79)、3杯以上でもリスク低下は同程度であることが報告されている9)。コーヒー摂取によるPD発症リスクの低下のメカニズムの一つとしてカフェインの関与が推測されている。他の多くの化学物質とは異なり、カフェインは血液脳関門を通過して脳実質へ入り、その化学作用の一つとして、アデノシンがアデノシンA2A受容体に結合するのをブロックすることにより覚醒作用を発揮する。PDとアデノシンA2A受容体の関連性としては、運動機能の低下をもたらす脳内GABA(γ-アミノ酪酸)を分泌する神経は、ドパミンにより抑制されアデノシンA2A受容体からの刺激で興奮し、通常は両者のバランスが保たれているが、PDではドパミンが不足するので、アデノシンA2A受容体からの刺激が優勢になる。したがって、アデノシンA2A受容体拮抗薬と呼ばれる薬剤(イストラデフィリン)は、アデノシンA2A受容体を阻害し、GABA作動性神経の過剰興奮を抑制することで、アンバランスになった神経シグナル伝達を正常化すると考えられている。カフェインにも、同様のアデノシンA2A受容体抑制効果を介した作用が考えられており、MPTP(1-methyl-4-phenyl-1,2,3,6-tetrahydropyridine)を投与したPDの動物モデルでは、カフェインによってアデノシンA2A受容体が遮断されることで、ドパミン神経の変性を抑制されることが示されている10)。また、別のメカニズムとしては、ドパミンはその代謝過程で活性酸素を生じやすいため、抗酸化物質としてのカフェインがドパミン神経細胞変性の保護作用を発揮する可能性も考えられる。
4.カフェインELISAの開発と血中カフェイン濃度のPD-BMとしての有用性の検証
上述したように、PDの発症機序におけるカフェイン代謝の関与が示唆されている。著者らも、PD患者における血液中カフェイン濃度のPDバイオマーカーとしての有用性に注目したが、これまで我が国ではカフェイン濃度を定量できる測定系が、順天堂大学グループが用いたHPLC以外には存在しなかった。そこで、我々は2018年に、より簡便に臨床応用が可能なELISAによるカフェイン測定系を、オリジナルに開発・作製した。我々の作製した競合ELISA系は、0.15〜150 ng/mLの範囲でカフェインの定量が可能であった(図A)。
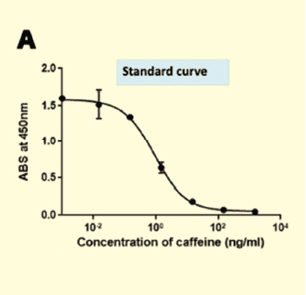
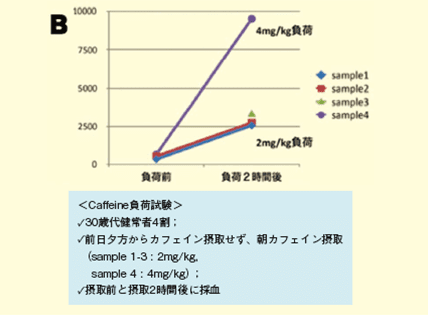
実際のヒト血液中では、2,000倍希釈の測定で7〜7,000ng/mLのカフェイン濃度の定量が可能で、コーヒーの摂取によって血中濃度が5〜10倍に増加することも確認した(摂取したカフェインが排出される半減期は約5〜7時間、完全排泄までに10~14時間)(図B)。
また、北海道大学(HU)と京都府立医科大学(KPU)の2つの異なったPD患者/MSA患者/対照患者コホート(KPUコホート : 31 PD, 18 MSA, 33 age-matched controls ; HUコホート : 50 PD, 50 MSA, 45 age-matched controls)で、我々のカフェインELISAを用いた血中カフェイン濃度の検討を行った11)。我々のELISAによって両群の被検者の血液中カフェイン濃度の安定的な定量が可能で、PD群では対照群と比較して、血中カフェイン濃度が有意に低下していた(図C, D)。
また、MSA群でも対照群と比較して、血中カフェイン濃度が低下しており、HUコホートでは両群に有意差を認めた(図C, D)。
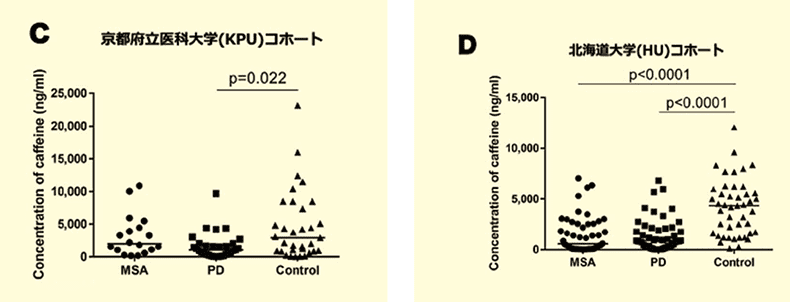
(D : PD患者/MSA患者/対照患者 : n=50/50/45)での我々のカフェインELISAを用いた血中カフェイン濃度の検討
また、血中カフェイン濃度によるPD患者とMSA患者の対照者との弁別能は、HUコホートでは、ROC曲線による解析でのAUCが、PD vs Controlでは0.821、MSA vs Controlでは0.810と高い弁別能を有していた(図E, F)。
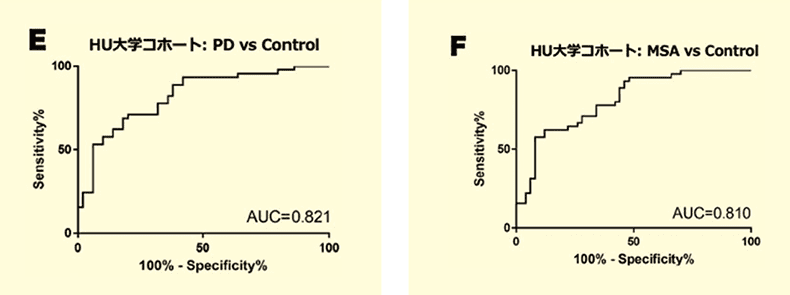
以上の結果は、順天堂大学グループが血漿のメタボローム解析で明らかにした「PD患者では血漿中カフェイン濃度が、対照群よりも減少している」という報告を、我々が独自に開発した臨床応用がより簡便なカフェインELISA法によっても再現できたことを示している。今後、より大規模のコホートで、その有用性が検証できれば、我々のカフェイン定量ELISA系はPDおよび関連疾患の実臨床への応用が期待できる。
参考文献
- Tokuda, T., et al. : Biochem. Biophys. Res. Commun., 349, 162 (2006).
- Tokuda, T., et al. : Neurology, 75, 1766(2010).
- Okuzumi, A., et al. : Na™ed., 29, 1448(2023).
- Shahnawaz, M., et al. : JAMA neurology, 74, 163(2017).
- Fujimaki, M., et al. : Neurology, 90, e404(2018).
- Hatano, T., et al. : J. Neurol. Neurosurg. Psychiatry, 87, 295(2016).
- Takeshige-Amano, H., et al. : Mov. Disord., 35, 1438(2020).
- Ascherio, A., et al. : Ann. Neurol., 50, 56(2001).
- Qi, H., et al. : Geriatr. Gerontol. Int., 14, 430(2014).
- Chen, J.F., et al. : J. Neurosci., 21, RC143(2009).
- Ohmichi, T., et al. : Front Neurol., 11, 580127(2020).




