【総説】2-OG 骨格を持たない次世代HIF 活性化分子PyrzA
本記事は、和光純薬時報 Vol.90 No.4(2022年10月号)において、佐賀大学農学部 天然資源化学分野 川口 真一様、生化学分野 辻田 忠志様に執筆いただいたものです。
低酸素誘導因子(HIF)は、脊速やかに核へ移行して、VEGF(血管内皮増殖因子)、EPO(エリスロポエチン)、GLUT1(グルコーストランスポーター1)などのタンパク質発現を上昇させ、低酸素障害に対して保護作用のある血管新生、造血、代謝リプログラミングが促進される3, 4)。したがって、HIFの安定化は、心筋梗塞や脳卒中などの貧血や虚血状態の改善に有効であると注目されている。
しかし、前述したタンパク質群は、低酸素ストレスの緩和に対して「正」と働く一方で、ある一定種のがん細胞に対しては増殖活性を補助してしまう「負」の側面も有する。このため、学術研究者や製薬会社は、酸素状態にさらすことなくHIFを活性化可能な低分子化合物の探索に取り組んでいる。
HIFは通常酸素状態ではプロリン水酸化酵素ドメイン含有タンパク質(PHDs)によって水酸化され、von Hippel-Lindau (VHL) E3ユビキチンリガーゼによってユビキチン化される。ユビキチン化されたHIFは、プロテアソームを通じて速やかに分解される。このようにHIFを分解に導く最初の段階はPHDsによるHIFの水酸化であることから、PHDsの機能を阻害することでHIFの活性化が試みられてきた。
PHDsがHIFを水酸化するためには補因子2-オキソグルタル酸(2-OG)が必要であり、これを母骨格としたPHD阻害剤の開発が製薬各社から進められてきた。現在までに日本では、5社からPHD阻害剤によるHIF活性化機構に基づく腎性貧血の治療薬が販売されている(図1)5-9)。
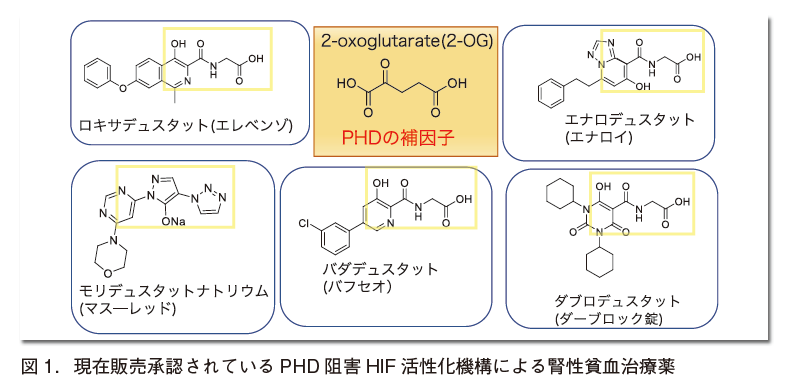
いずれのPHD阻害剤も共通点として2-OG骨格を有している(モリデュスタットナトリウムはカルボキシル基がバイオアイソスターであるトリアゾール基に変更されている)。一方で、HIFにはHIF-1α、HIF-2α、HIF-3αのアイソフォームが存在し、また、それらを制御するPHDsもPHD1、PHD2、PHD3のアイソフォームが存在する。このアイソフォーム同士は密接にリンクしながら、低酸素ストレス緩和とそれに関連する副作用を制御できると遺伝子改変マウスの表現系より予想されており、PHDsの選択的な阻害にチャレンジするモチベーションとなっている。
PHD1、PHD2、PHD3タンパク質においての2-OGと相互作用を示すPHD側鎖の環境はそれぞれ酷似しており、PHDsの選択的な阻害を達成するには2-OGとの拮抗阻害でない形式でPHDsの機能阻害が必要であると考えられた。すなわち、2-OG骨格を持たないPHDs阻害剤の開発が必要であるため、著者らはランダムスクリーニングを実施し、2-OG骨格を持たないPHDs阻害剤PyrzA(5-(1-acetyl-5-phenylpyrazolidin-3-ylidene)-1,3-dimethylbarbituric acid)を見いだした10)。
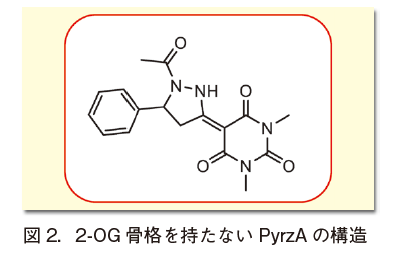
PyrzAはジメチルバルビツール酸およびピラゾリジン骨格からなる化合物であり、2-OG骨格を持たない(図2)。ドッキングシミュレーションによるPHD2とPyrzAの結合位置予測では、PyrzAはヒトHIF-1αの第402番目のプロリン残基と良い重なりを示した(図3)。
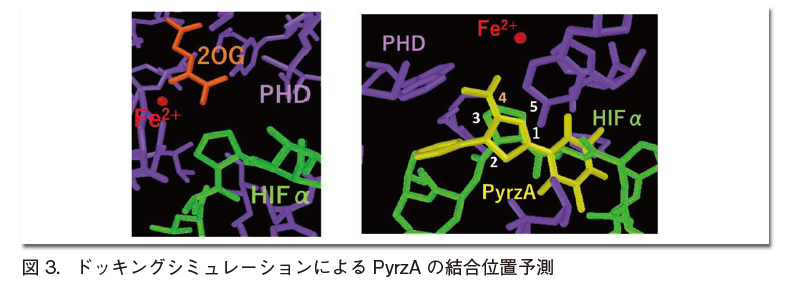
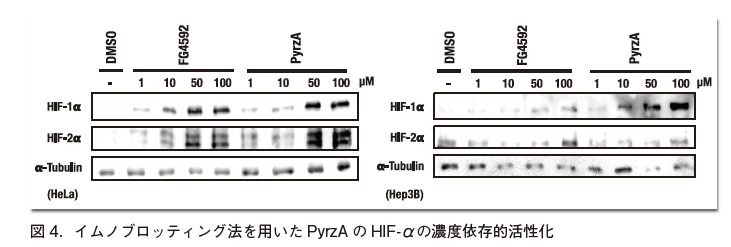
このように、HIF-1α と拮抗阻害を示す分子はPyrzAが初めてである。HeLa細胞およびHep3B細胞の2種類の細胞にPyrzAを加え、イムノブロッティング法によって、HIF-1α、HIF-2αのタンパク質の安定化を確認した(図4)。細胞による多少の違いはあるもののPyrzAはロキサデュスタット(FG4592) と同様、濃度依存的にHIF-1α、HIF-2αいずれも安定化させた。
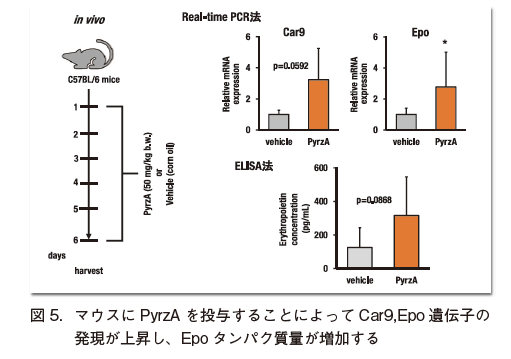
野生型C57BL6のメスの6週齢マウスにPyrzAを5日間腹腔内注射したところ、腎臓のCar9(炭酸脱水酵素9)およびEpoのmRNAはいずれもコントロールに対して発現上昇を示した(図5)。加えて、血漿中のエリスロポエチン量もコントロールに対して上昇傾向にあることが示された。以上のようにPyrzAはin vivo においても効果が見込まれる。
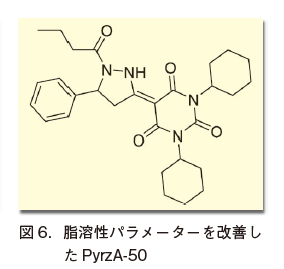
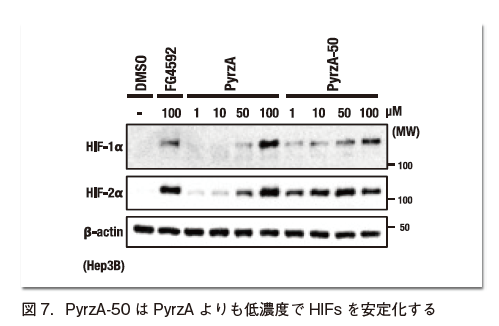
PyrzAの脂溶性のパラメーターである分配係数cLogP値は、計算値で-0.91とされ、経口投与を目的とする化合物の値としては低い11)。そこで、PyrzAの側鎖構造変換を繰り返して図6に示す化合物を得た。本化合物のcLogP値は3.26となり数値の大幅な改善に成功した。本化合物は、PyrzAよりも約50倍低い濃度でHIFの転写活性を示すことが明らかとなったので、これをPyrzA-50と名付けた。PyrzA-50はHep3B細胞においてHIF-1α、HIF-2αともにPyrzAよりも低い濃度で安定化した(図7)。
以上のようにPyrzA、PyrzA-50は次世代のPHD阻害によるHIF活性化薬となりうる有望な分子である。PHDs阻害の機構の解明やPHDs阻害の選択性の解明などに課題は残っているものの、活性が高く、in vivo での活性を示し、2-OG骨格を持たない分子という特徴を有する。今後、低酸素研究やがん研究のツールとして期待できることに加え、我々は虚血性疾患の治療薬まで昇華できるか研究を推進する予定である。
利益相反の申告:著者の川口および辻田はテトラクリエイト株式会社の技術顧問であり、テトラクリエイト株式会社はPyrzAおよびPyrzA-50の製造販売を担っていることを申告する。
参考文献
- Semenza, G. L. and Wang, G. L. : Mol. Cell.Biol ., 12, 5447( 1992).
- Semenza, G. L. : N. Engl. J. Med ., 365, 537(2011).
- C armeliet, P. et al . : Nature , 394, 485( 1998).
- Kaelin, W. G. and Ratcliff e, P. J. : Mol. Cell. ,30, 393( 2008).
- Arend, M. P. et al . : WO2004/108681.
- Ogoshi, Y. et al . : ACS Med. Chem. Lett ., 8,1320( 2017).
- Beck, H. et al . : ChemMedChem , 13, 988(2018).
- Rabinowitz, M. H. et al . : Annu. Rep. Med.Chem., 45, 123( 2010).
- T hevis, M. : Drug Test. Anal ., 8, 858( 2016).
- Sonoda, K. et al . : ACS Pharmacol. Transl.Sci ., 5, 362( 2022).
- Sonoda, K. et al . : Manuscript in preparation.




