肺がんにおけるEGFR薬剤耐性変異
本記事は、カルナバイオサイエンス株式会社が発行しているニュースレターを再編集し掲載しています。
はじめに
キナーゼ阻害薬はimatinibが2001年にがん治療薬として上市されて以来各ターゲットに対するFirst-in Class中心の探索に加え、薬剤耐性を獲得した変異体に対する次世代薬剤の開発も大きく展開しております。世界のがん統計2020で死亡原因の第1位、そして新規症例数の第2位は肺がんであり1)、中でも肺がんの多くを占める非小細胞肺がん (NSCLC) の1種、肺腺がんでは、治療薬であるEGFR阻害剤投与後の患者間でEGFRの薬剤耐性変異発生が高い頻度で観察されています。
受容体型チロシンキナーゼであるEGFR (Epidermal growth factor receptor: 上皮成長因子受容体) はリガンドが細胞外ドメインに結合すると二量体を形成し、これにより活性化構造をとることで、自己のチロシンリン酸化を介して細胞内にシグナルを伝えています。下流経路としてはMAPK, PI3K-AKT及びSTAT3/5などが知られており、EGFRは細胞増殖やアポトーシス制御に関与しています2)。
EGFR薬剤耐性変異
EGFR変異陽性肺がんでみられるEGFR変異の約8割は、エキソン19の5アミノ酸程度の欠損 (del19) やエキソン21の点突然変異 (L858R) のいずれかであり2)、これらのEGFR変異体はリガンド非依存的に恒常的に活性化しています。AstraZeneca社の調査では、肺腺がんにおけるEGFR変異発生率は、アジア太平洋地域で20-76%、ヨーロッパ地域で6-41%、北アメリカで3-42%であると報告されています3)。
臨床結果によると、EGFR変異、del19又はL858Rを伴う腫瘍を有する肺がん患者に一次療法として第一世代、第二世代又は第三世代のEGFR阻害薬を使用した場合の客観的奏効率は約60-85%です4)。しかし投与を受けた患者において、腫瘍反応は顕著な腫瘍縮小を伴う一方、その反応は通常持続しません。第一世代及び第二世代のEGFR阻害剤で治療された患者の50~70%で見られる疾患進行に関連する最も主要な分子耐性メカニズムはEGFRの二次変異であるゲートキーパー変異、T790Mの獲得です4) (Fig.1) 。T790M変異はATP結合ポケット内に起こるため、EGFRに対するEGFR阻害剤の親和性を低下させると考えられています5)。
T790M薬剤耐性変異の有無に関わらず、一次EGFR変異、del19及びL858Rを効果的に阻害する薬剤として開発された第三世代のEGFR阻害剤がosimertinibです。しかしながら、二次療法としてのosimertinibはT790M/(del19 or L858R) 陽性のNSCLC患者に対して一旦は臨床的効果を示しますが、平均10か月の投与期間後に疾患が進行してしまいます。そして再発した二次療法患者の20~40%が、osimertinibとの共有結合に必要なEGFRのシステイン残基に三次変異(C797S)を獲得していることが分かってきました4) (Fig.1)。
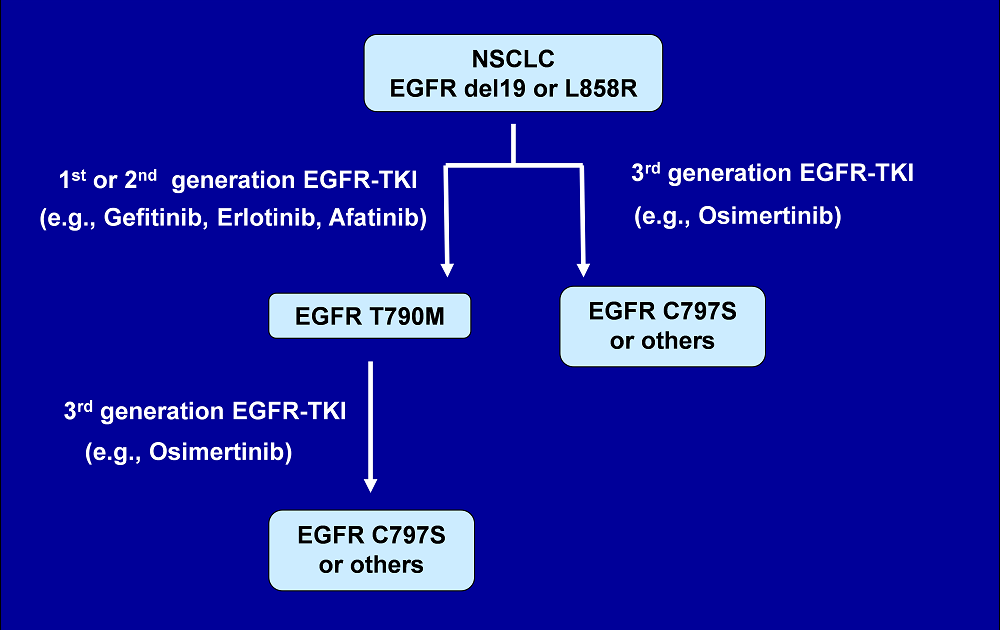
Fig1. Evolution of EGFR mutant lung cancer on therapy
第四世代のEGFR阻害剤開発
EGFR (del19 or L858R)/T790M/C797S変異体は、承認されている第一世代、第二世代または第三世代のEGFR阻害剤のいずれによっても阻害されないため、現在はEGFR (del19 or L858R)/T790M/C797S変異体を阻害できる第四世代のEGFR阻害剤の研究開発が進められています。中でもBLU-945及びBBT-176は現在第1/2相臨床試験の段階にあり、今後の進展が期待されています6)7)。
おわりに
このように、EGFR変異体を原因とするNSCLCに対しては、患者数が多いにも関わらず、既存のEGFR阻害剤の持続投与により薬剤耐性変異が発生してしまうため、より効果的な治療薬が求められており、EGFR阻害薬に対する耐性克服を狙った新たな次世代のEGFR阻害剤の開発が望まれています。
本文中の変異を含むEGFRキナーゼタンパク質シリーズ製品はカルナバイオサイエンス社より提供されています。
参考文献
- Sung, H. et al. : CA Cancer J Clin., 71(3), 209 (2021).
- Kobayashi, Y. et al. : Cancer Sci., 107(9), 1179 (2016).
- Midha, A. et al. : Am J Cancer Res., 5(9), 2892 (2015).
- Engelhardt, H. et al. : J Med Chem., 62(22), 10272 (2019).
- Kobayashi, S. et al. : N Engl J Med., 352(8), 786 (2005).
- Schalm, S. et al. : ESMO Congress, p1296 (2020).
- Lim, S.M. et al. : ESMO Congress, tip1365 (2021).
このニュースレターの中で論文から引用した情報の日本語翻訳文はカルナバイオサイエンス社が作成しました。




