【総説】低分子系半導体−p型
本記事は、東京大学大学院新領域創成科学研究科物質系専攻 工学部応用化学科 岡本 敏宏准教授に執筆いただいたものです。
20世紀中頃、有機化合物が電気を流す半導体的な性質を示すことは知られていた。しかしながら、電流はほとんど流れず、安定性が悪かったため、電気が全く流れない絶縁体としての認識が持たれていた。
1984年にKudoらの研究グループ1)によって、merocyanine dye (メロシアニン色素, 図1参照)の低分子系半導体を活性層に用いた有機電界効果トランジスタ(OFET)において、10-7から10-5 cm2/Vs程度のキャリア移動度が世界で初めて報告された。これを機に研究が活発になり、1990年代にはいり、ベンゼン環が棒状(直線状)に5つ縮環したアセン系化合物であるpentacene(ペンタセン, 図1参照)を用いた多結晶薄膜トランジスタ(Thin-film transistor, TFT)において、アモルファスシリコンと同等の1.0 cm2/Vsの正孔移動度が実現していることが明らかとなった2)。
ペンタセンは昇華精製により高品質なものが容易に入手可能であり、真空蒸着法で簡便に特性評価ができる。しかしながら、ペンタセンは、浅い最高被占軌道(Highest Occupied Molecular Orbital, HOMO)レベル(EHOMO = 4.84 eV, B3LYP/6-311G(d)レベル)を有し、また、中央の環の6,13位の炭素の反応性が高いため、大気中で容易に酸化されてしまうことがよく知られている3)。
大気安定性(化学的安定性)を改善する目的で、アセン系化合物の一部のベンゼン環をヘテロ環に置換したヘテロアセン系化合物が研究されている。 図1に示した2,6-diphenylbenzo[1,2-b:4,5-b']dichalcogenophene (2,6-ジフェニルベンゾ [1,2-b:4,5-b']ジカルコゲノフェン, DPh-BDX)4)、 2,7-diphenyl[1]benzothieno[3,2-b]benzothiophene ([1]ベンゾチエノ[3,2-b][1]ベンゾチオフェン, DPh-BTBT)5)は、大気下で安定に駆動可能な深いHOMOレベル(図1参照)を有し、大気下でペンタセンと同等の2.0 cm2/Vsの正孔移動度を達成している。また、BTBT骨格にベンゼン環をさらに縮環させたdinaphtho[2,3-b:2',3'-f]thieno[3,2-b]thiophene(ジナフト[2,3-b:2',3'-f]チエノ[3,2-b]チオフェン,DNTT, 図1)は、より高い正孔移動度である2.9 cm2/Vsを達成している6)。
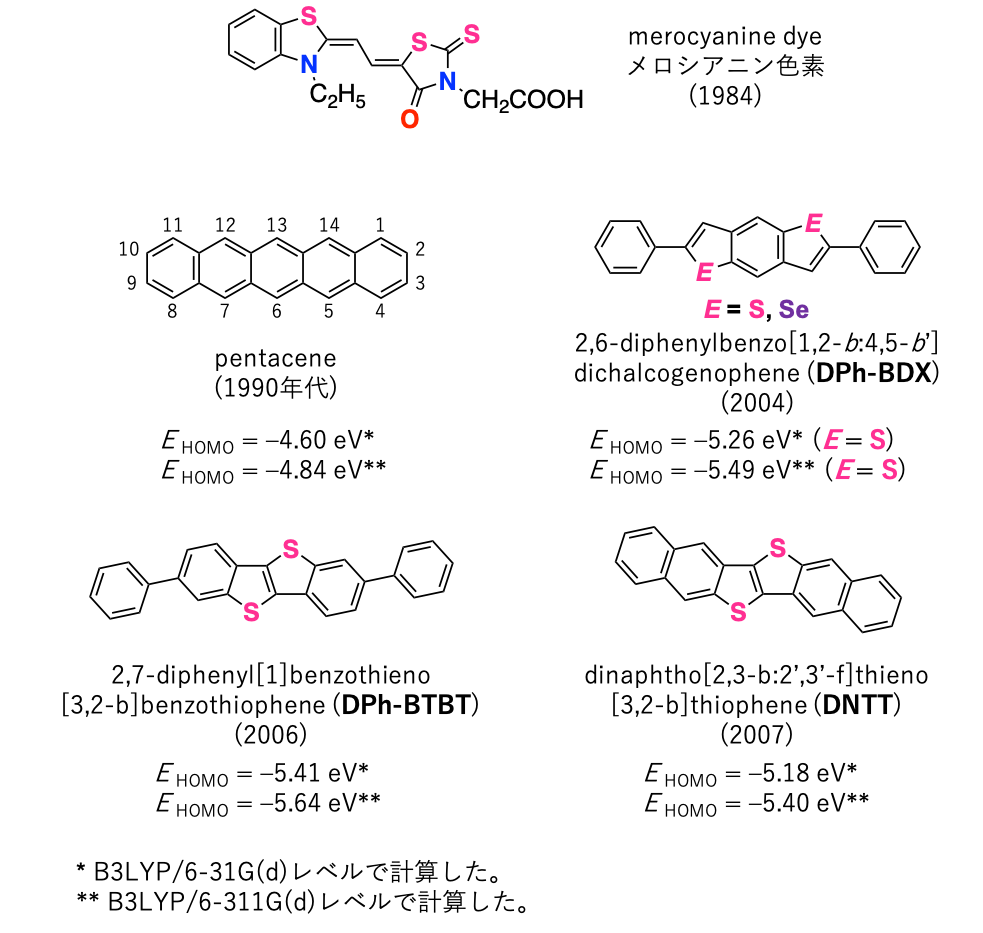
図1. 低分子系半導体−p型①.
上記で述べたペンタセンや一連のヘテロアセン系分子群は、一般的な有機溶媒であるクロロホルムやトルエンなどに対して、室温付近で極めて溶解性が低いため、有機半導体の強みである印刷プロセスの適用は困難であった7), 8)。そこで、これらの分子骨格に嵩高い置換基9)や長鎖アルキル基(通常、炭素数が8以上)を導入した誘導体が開発された。
これらは、有機溶剤に対する溶解性が飛躍的に改善され、印刷プロセスによる製膜が可能となった。たとえば、ペンタセンの6,13位に嵩高い置換基であるトリイソプロピルシリル(TIPS)エチニル基を導入した6,13-bis(triisopropylsilylethynyl)pentacene(6,13-ビス(トリイソプロピルシリルエチニル)ペンタセン, TIPS-Pentacene)は、溶解性の改善に加えて、エチニル基部位が電子求引性置換基として機能し、ペンタセンの大気不安性を同時に解消した画期的な化合物である9)。
開発当初では、TIPS-Pentaceneの塗布製膜、続く加熱処理後の正孔移動度は、ペンタセンよりも一桁低い0.17 cm2/Vsであったが、製膜方法の改良や高分子との相分離構造の利用により1 cm2/Vs以上まで正孔移動度が向上した10)。また、ごく最近では、製膜方法の改良が進み、準安定な結晶相への誘起による高正孔移動度が達成されている11)。
また、長鎖アルキル基が導入された2,9-dialkyldinaphtho[2,3-b:2',3'-f]thieno[3,2-b]thiophene (2,9-ジアルキルジナフト[2,3-b:2',3'-f]チエノ[3,2-b]チオフェン, Cn-DNTT)では、無置換体に比べて、アルキル鎖間のvan der Waals相互作用により、分子の自己組織化が促進され、多結晶(7.9 cm2/Vs)12)および単結晶薄膜(10 cm2/Vs)13)でそれぞれ高い正孔移動度を達成している。
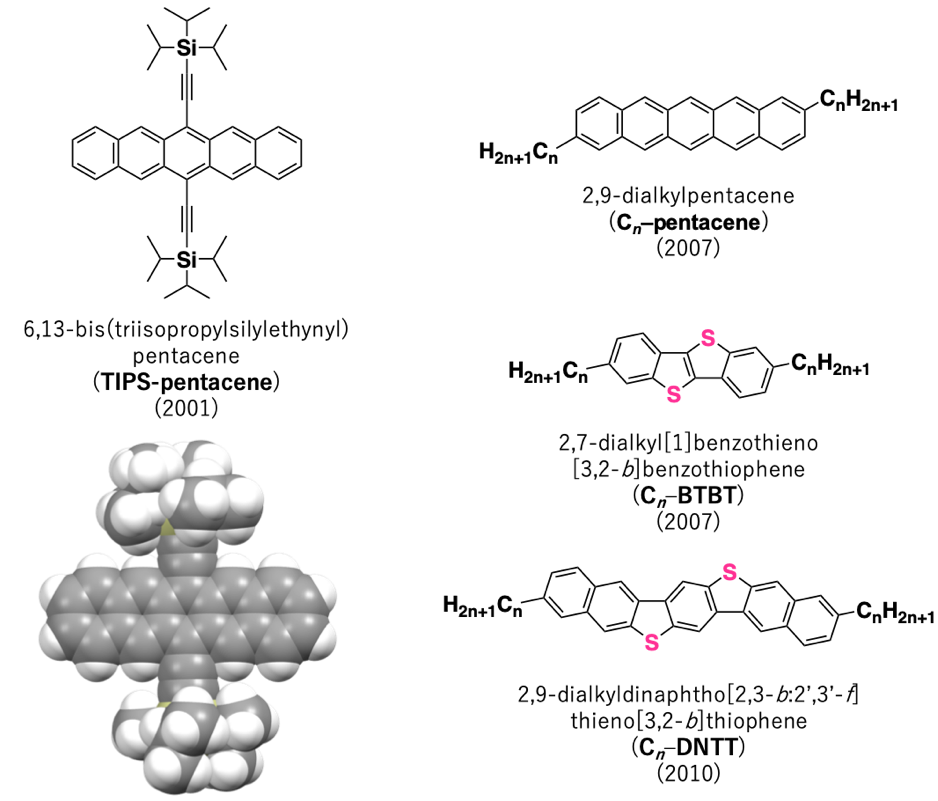
図2. 低分子系半導体−p型②.
これらの置換基の導入は、塗布プロセスを可能とする反面、熱などの外的刺激により元々の相(結晶相など)から流動性の高い相(液晶相や他の結晶相)へ相転移しやすくなる問題が生じる。たとえば、長鎖アルキル基を導入したペンタセン、BTBTやDNTTなどの棒状もしくは擬棒状パイ電子系骨格は、分子長軸まわりの回転運動や並進運動が起こりやすいため、デシル基(C10-)が置換されたペンタセン(C10-pentance, n = 10)、BTBT(C10-BTBT, n = 10)やDNTT(C10-DNTT, n = 10)は、それぞれ89 ºC、 109 ºCや117 ºCで相転移の存在が報告されている14) -16)(図2, 3)。
実デバイスの電極配線やパターニングのためには通常150-200℃17)のプロセス、さらに、自動車の車内などの高温下における使用を鑑みると、熱ストレスに対する耐久性も兼ね揃えた塗布型有機半導体の開発が必要である18)。
上記の課題を解決するために、筆者らはパイ電子系骨格の形状と軌道形態にこだわった分子設計を展開している。筆者らがパイコアに「屈曲」という新たな概念を導入し分子設計した第1世代屈曲型パイコア(図3)は、大きな軌道係数を有する張り出した硫黄元素間の有効的な軌道の重なりによる高移動度化、屈曲骨格から生じる分子内もしくは局所ダイポールによる溶解性の向上、キャリアのコヒーレンスを実現するために、分子揺らぎ(分子間振動)を小さくするための分子設計、すなわち、分子の並進および回転運動の抑制による高移動度化、さらに、相の構造安定化に伴う熱耐久性の向上を目論んだ分子群である。
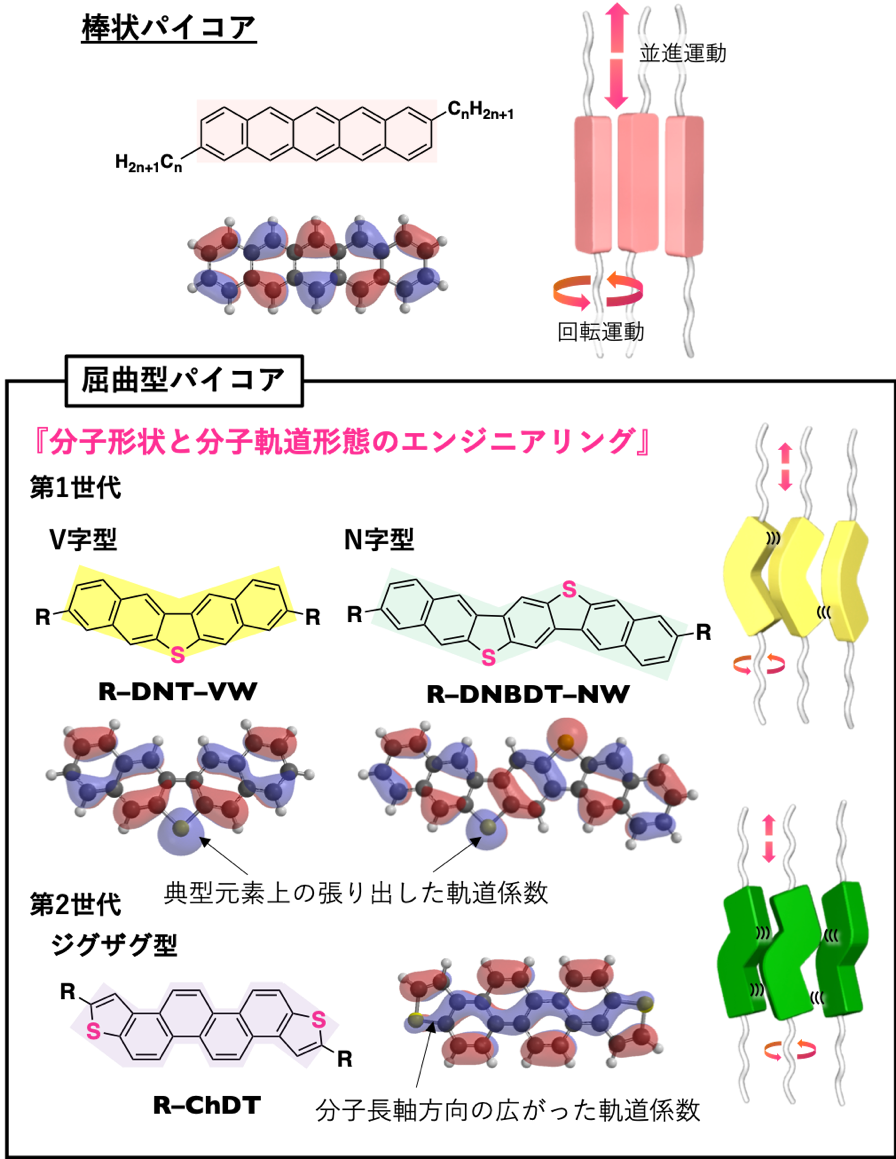
図3. 棒状パイコア vs. 屈曲型パイコア.
一連の第1世代屈曲型パイコアは、集合体構造 (単結晶) で二次元伝導に有利なヘリングボーン型構造を有し、3,9-ジヘキシルジナフト[2,3-b:2',3'-d]チオフェン (3,9-dihexyldinaphtho[2,3-b:2',3'-d']thiophene, C6-DNT-VW)や3,11-ジデシルジナフト[2,3-d:2',3'-d']ベンゾ[1,2-b:4,5-b']ジチオフェン(3,11-didecyldinaphtho[2,3-d:2',3'-d']benzo[1,2-b:4,5-b']dithiophene, C10-DNBDT-NW)の塗布単結晶薄膜で10 cm2/Vsを超える移動度を示す有機半導体であった(図4)19), 20)。さらに、屈曲型パイコアは、塗布プロセス可能な材料ではこれまで実現困難であった200℃以上の結晶安定性を有し、デバイス状態でも高い熱ストレス耐性を実現した20)。
また、ごく最近、分子軌道形態にこだわって新たに開発した第2世代屈曲型パイコアは、第1世代と同様の半導体性能を有するだけでなく、理論計算から、分子間振動が起こりやすい分子長軸方向について、棒状分子および第1世代分子と比較してトランスファー積分の変化が非常に小さいことが明らかになり21)(図4)、さらなる高移動度化が期待される分子群である。
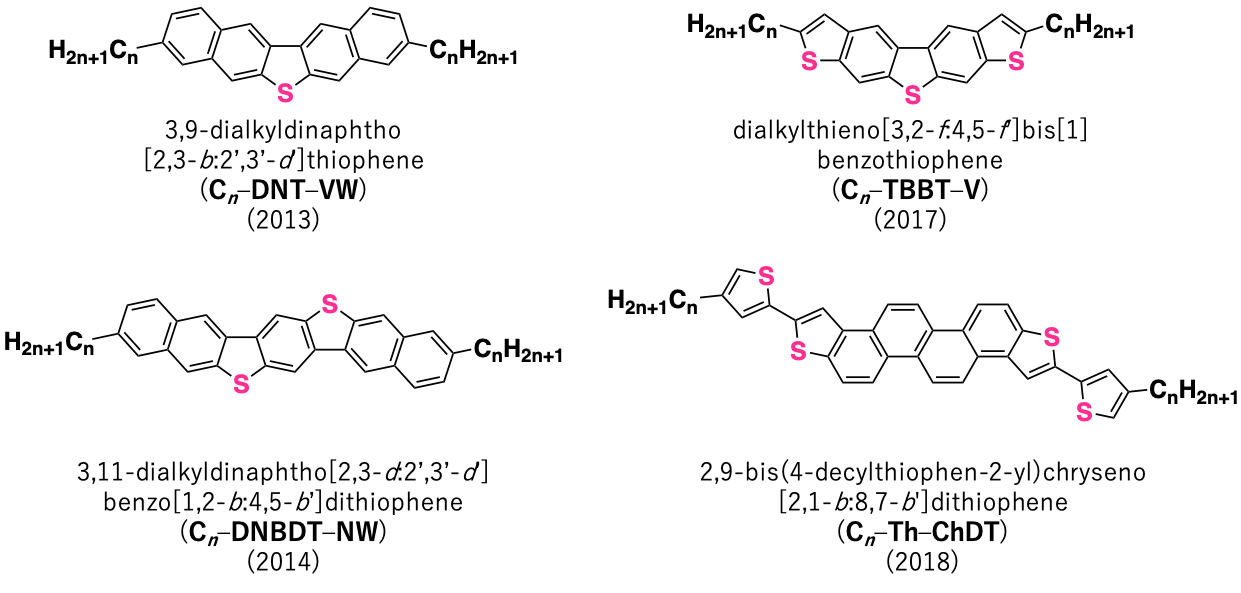
図4. 低分子系半導体−p型③.
参考文献
- Kudo, K., Yamashina, M. and Moriizumi, T.: Jpn. J. Appl. Phys., 23, 130 (1984).
- Lin, Y. Y., Gundlach, D. J., Nelson, S. F. and Jackson, T. N.: IEEE Electron Device Letters, 18, 606 (1997). DOI: 10.1109/55.644085
- Maliakal, A., Raghavachari, K., Katz, H., Chandross, E. and Siegrist, T.: Chem. Mater., 16, 4980 (2004). DOI: 10.1021/cm049060k
- Takimiya, K., Kunugi, Y., Konda, Y., Niihara, N. and Otsubo, T.: J. Am. Chem. Soc., 126, 5084 (2004). DOI: 10.1021/ja0496930
- Takimiya, K., Ebata, H., Sakamoto, K., Izawa, T., Otsubo, T. and Kunugi, Y.: J. Am. Chem. Soc., 128, 12604 (2006). DOI: 10.1021/ja064052l
- Yamamoto, T. and Takimiya, K.: J. Am. Chem. Soc., 129, 2224 (2007). DOI: 10.1021/ja068429z
- Minakata, T. and Natsume, Y.: Synth. Metals, 153, 1 (2005). DOI: 10.1016/j.synthmet.2005.07.210
- Minakata, T. and Natsume, Y.: Appl. Phys. Lett., 93, 153306 (2008). DOI: 10.1063/1.3001931
- Anthony, J. E., Brooks, J. S., Eaton, D. L. and Parkin, S. R.: J. Am. Chem. Soc., 123, 9482 (2001). DOI: 10.1021/ja0162459
- Park, S. K., Jackson, T. N., Anthony, J. E. and Mourey, D. A.: Appl. Phys. Lett., 91, 063514 (2007). DOI: 10.1063/1.2768934
- Giri, G., Verploegen, E., Mannsfeld, S. C. B., Atahan-Evrenk, S., Kim, D. H., Lee, S. Y., Becerril, H. A., Aspuru-Guzik, A., Toney, M. F. and Bao, Z.: Nature, 480, 504 (2011). DOI: 10.1038/nature10683
- Kang, M. J., Doi, I., Mori, H., Miyazaki, E., Takimiya, K., Ikeda, M. and Kuwabara, H.: Adv. Mater., 23, 1222 (2011). DOI: 10.1002/adma.201001283
- Nakayama, K., Hirose, Y., Soeda, J., Yoshizumi, M., Uemura, T., Uno, M., Li, W., Kang, M. J., Yamagishi, M., Okada, Y., Miyazaki, E., Nakazawa, Y., Nakao, A., Takimiya, K. and Takeya, J.: Adv. Mater., 23, 1626 (2011). DOI: 10.1002/adma.201004387
- Ebata, H., Izawa, T., Miyazaki, E., Takimiya, K., Ikeda, M., Kuwabara, H. and Yui, T.: J. Am. Chem. Soc., 129, 15732 (2007). DOI: 10.1021/ja074841i
- Okamoto, K., Kawamura, T., Sone, M. and Ogino, K.: Liq. Cryst., 34, 1001 (2007). DOI: 10.1080/02678290701478970
- Kuwabara, H., Ikeda, M. and Takimiya, K.: WO 2010/098372 A1 (2010).
- Kuribara, K., Wang, H., Uchiyama, N., Fukuda, K., Yokota, T., Zschieschang, U., Jaye, C., Fischer, D., Klauk, H., Yamamoto, T., Takimiya, K., Ikeda, M., Kuwabara, H., Sekitani, T., Loo, Y.-L. and Someya, T.: Nat. Commun., 3, 723 (2012). DOI: 10.1038/ncomms1721
- Iino, H., Kobori, T. and Hanna, J.-i.: J. Non-Cryst. Solids, 358, 2516 (2012). DOI: 10.1016/j.jnoncrysol.2012.03.021
- Okamoto, T., Mitsui, C., Yamagishi, M., Nakahara, K., Soeda, J., Hirose, Y., Miwa, K., Sato, H., Yamano, A., Matsushita, T., Uemura, T. and Takeya, J.: Adv. Mater., 25, 6392 (2013). DOI: 10.1002/adma.201302086
- Mitsui, C., Okamoto, T., Yamagishi, M., Tsurumi, J., Yoshimoto, K., Nakahara, K., Soeda, J., Hirose, Y., Sato, H., Yamano, A., Uemura, T. and Takeya, J.: Adv. Mater., 26, 4546 (2014). DOI: 10.1002/adma.201400289
- Yamamoto, A., Murata, Y., Mitsui, C., Ishii, H., Yamagishi, M., Yano, M., Sato, H., Yamano, A., Takeya, J. and Okamoto, T.: Adv. Sci., 5, 1700317 (2018). DOI: 10.1002/advs.201700317
シリーズ一覧





