【連載】エンドトキシン便り「第4話 エンドトキシン(LPS)の不活化と除去」
本記事は、和光純薬工業 試薬化成品事業部開発第一本部 BMS 開発部 BMS センター 高岡 文が執筆したものです。
はじめに
弊社には、さまざまな分野の方々から、エンドトキシンを除きたい、あるいは不活化したいという要望が寄せられます。最適な方法はそれぞれのケースで検討して決めることになりますが、その際にどのような選択肢があるのか、問題点になりやすいことは何かを知っておくことが重要です。
詳しくは既報1)をご参照いただきたいのですが、本稿では、除去や不活化の原理、実施例を紹介し、さらに除去、不活化のバリデーションの注意点についても簡単に述べます。
エンドトキシンの不活化方法
(1)乾熱処理
乾熱は、対象物がガラスや金属のような熱に耐える素材である場合は、もっとも信頼できるエンドトキシン不活化法です。薬局方のエンドトキシン試験法では、試験に使用する器具で耐熱性のものについては、「通例、少なくとも 250 ℃で 30 分の乾熱処理を行う」と記載されています。
(2)湿熱処理
希薄なエンドトキシン溶液を加熱すると、ライセート試薬に対する反応性や細胞に対するサイトカインの産生誘導能が低下することは種々報告されています。ただし、このような活性低下は LPS ミセルの高次構造変化が原因している可能性も示唆されており2)、不可逆な不活化とは言い切れない点に注意を要します。
オートクレーブによる不活化処理では、ある程度の効果は見込めるものの、混入しているエンドトキシンの濃度や共存物質により効果の程度は大きく異なります。
(3)酸/アルカリ処理
LPS 分子は希酸により加水分解されて Lipid A が遊離し不溶性になること、不溶化にともない発熱性が低下することが知られています。また、アルカリとエタノールやジメチルスルホキシドの共存により LPS から脂肪酸の離脱とミセルサイズの減少、および発熱性、ニワトリ致死活性の低下が水中よりも速やかに起こることも報告されています3)。
これを応用した方法、例えば 0.03~0.1N NaOH を添加した 95% エタノール中で 30~60 分間 30℃で保持するといった方法は、注射用水による最終洗浄と組み合わせて用いれば、プラスチックなどの高温加熱できない素材の器材からエンドトキシンを除くのに有用です。
(4)ガンマ線照射滅菌
プラスチック製器材の滅菌で汎用されるガンマ線照射滅菌の効果は、乾熱と比較して充分ではありません。これは、滅菌済みが保証されている器材であっても必ずしもエンドトキシンフリーではない理由のひとつです。
エンドトキシンの除去方法
(1)蒸留
古くから注射用水の製造法として用いられてきた方法で、蒸留後、微生物による再汚染がないように管理できれば、脱エンドトキシンの工業スケールでの実用的な方法です。
(2)膜ろ過
エンドトキシンの活性本体である Lipid A の分子量は約 2000 です。菌体から自己溶解などで放出された LPS は、水中では通常見かけの分子量が 1~100 万程度のミセルを形成しているので、分画分子量 1~2 万以下の限外ろ過や逆浸透(RO)膜によるろ過で除去できます。
(3)選択吸着
LPS 分子はリン酸基や KDO を持つため、負電荷を帯びており、また Lipid A 部分は疎水性ですので、これらの性質を利用して LPS を除去する方法が開発されています。
例えば、弊社ではアクロディスクシリンジフィルターという正荷電ナイロン 6,6 膜を用いたシリンジフィルター(孔径は 0.2µm、日本ポール製)を販売しています。ただし、静電力を利用した除去は、共存するイオンの影響を受けやすいという特性があります。
表 1 は、ろ過時に共存する NaCl 濃度とエンドトキシン除去率を調べた結果ですが、この程度の影響を受ける可能性があることを考慮する必要があります。
表1 NaCl の共存濃度とエンドトキシン除去率
| 共存する NaCl (%) | エンドトキシン(EU/mL) | 除去率 (%) | |
|---|---|---|---|
| ろ過前 | ろ過後 | ||
| 0 | 9.580 | 0.01073 | 99.9 |
| 1 | 7.647 | 1.641 | 78.5 |
| 5 | 7.647 | 5.237 | 31.5 |
リムルス ESⅡ シングルテストワコー(カイネティック-比濁法)
5 mL のエンドトキシン溶液をアクロディスクでろ過
また、通常のアクロディスクよりも高価ですがイオンの影響を受けにくいタイプの膜を用いた、アクロディスク・ムスタングフィルターもあります。
セルロースなどの担体にエンドトキシンを特異的に吸着するリガンドを結合した、エンドトキシン特異的吸着剤もいくつか市販されています。弊社でも、セルロース粒子に ε-ポリリジンを結合したセルファイン®ET クリーン(JNC(株))を取り扱っています。この ET クリーンを使用すると、BSA や γ-グロブリン等の蛋白溶液から効率よくエンドトキシンを除去できることが報告されています。
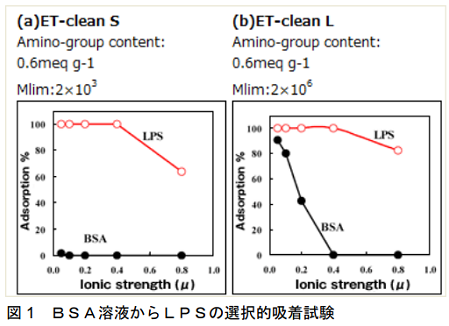
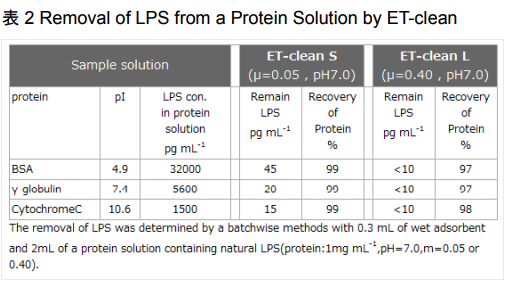
図 1 および表 2 は JNC 株式会社 HP より転載
膜ろ過や選択吸着を使用する場合は、サンプルの種類ごとにエンドトキシン除去率やサンプルの回収率評価が必要です。
エンドトキシン不活化・除去工程のバリデーション
エンドトキシンの不活化や除去(以下、脱パイロジェンと称す)の工程を設定する場合には、チャレンジテストによるバリデーションを行わなければなりません。すなわち、既知量のエンドトキシンを対象物に付加したエンドトキシンインジケーター(EI)を用い、脱パイロジェン処理後にエンドトキシンを測定します。
例えば、USP <1211> の乾熱滅菌のバリデーションでは、負荷した LPS が元の量の 1/1000 を超えて残存していない(3 log 減少以上の失活が起こる)ことをエンドトキシン試験結果で示さなければならないとされています。
滅菌工程のバリデーション用に市販されている EI を用いる場合、使用方法はメーカーの指示に従ってください。エンドトキシン回収率の計算には無処理の EI のエンドトキシン濃度を 100% として、処理後の EI のエンドトキシンの失活率を求めます。
実際の脱パイロジェン対象物で EI を調製する場合に有用なガイドが、LAL users group から提示されており4)、調製方法や取り扱い方法、評価法について述べられています。
なお、USP では、近く Depyrogenation を <1221> からはずして独立した記載 <1228> とし、乾熱滅菌だけではなく、種々の脱パイロジェン法に関して解説する予定です。いくつかの項目に関しては、すでに USP Pharmacopeial Forum の HP に案が掲載されていますので、ご興味のある方は、参考文献の 5) をご覧ください。
また、<1228.X> に関しては、内容が固まり次第、本欄でのご紹介もしていく予定です。
参考文献
- 高岡文, (2011) GMP 要求を満たすためのエンドトキシン不活化の必要性と実施について:防菌防黴, 39, 47-56.
- Gao, B., Wang, Y., Tsan, M. F., (2006) The heat sensitivity of cytokine-inducing effect of lipopolysaccharide. J. Leukoc. Biol., 80, 359-366.
- Niwa, M., Milner, K. C., Ribi, E., Rudbach, J. A., Alteration of Physical, Chemical, and Biological Properties of Endotoxin by Treatment with Mild Alkali, J. Bacteriol., 97, 1069-1077
- LAL users group, (1989) Preparation and Use of Endotoxin Indicators for Depyrogenation Process Studies. J. Parent. Sci. Technol, 43, 109-112
- <1228> Depyrogenation (Introduction) : USP PF, 40(2)/2014
<1228.1> Depyrogenation by Dry Heat : USP PF, 40(3)/2014
<1228.3> Depyrogenation by Filteration : USP PF, 41(5)/2015
<1228.5> Endotoxin Indicators for Depyrogenation : USP PF, 41(5)/2015
関連記事