【連載】なるほど !! ELISA -基礎とコツ- 「第2回 ELISA の操作法とそのポイント(前編)」
本記事は、和光純薬時報 Vol.85 No.3(2017年7月号)において、若林克己著「ELISA A to Z」をもとに株式会社シバヤギで編集し掲載いただいたものです。

市販キットを使用した場合の一般的な ELISA 操作法のポイントをご紹介します。キットメーカーにより推奨方法が異なります。実際には使用キットの取扱説明書に従って操作して下さい。
ポイント①;測定前のチェック
納品時のチェックポイント
- 製品の状態を確認しましょう。輸送温度が適切だったかどうか、損傷がないかなど、異常の有無を確認しましょう。
冷蔵保管品の場合のチェックポイント
- 冷蔵庫の温度設定(製品指定温度)を確認しましょう。試薬は凍結厳禁の場合があります。
- 冷蔵庫内で吹き出し口から直接冷気が当たる位置での保管は避けましょう。凍結する可能性があります。
- 冷蔵庫の温度が低過ぎるとキット構成品の濃縮洗浄液中の塩が析出することがあります。
- 上下逆さまに置いたり、横向きに置いたりしないようにしましょう。
*プレートに保存安定液が充填されているものがあります。上下逆さまに保管すると抗体固相面に気泡が接触してしまいます。
実験室・機器のチェックポイント
- 反応温度が一定に調節できる実験室を選びましょう。
- エアコンやストーブ、恒温槽、オートクレーブ、パソコンなど熱源が近くに無いこと。
- 空気の流れが小さいこと(風速 0.4m/sec 以下を推奨します)。
- 湿度が 30% 以上あることを推奨。
- 直射日光が当たらないこと。
- ピペットは定期的に校正を行いましょう。
- 自動洗浄機、プレートリーダーなどメンテナンスされた機器、器具を使用しましょう。
ポイント②;ピペット(プランジャー型について)
ピペット操作について
ELISA 測定でピペットを使用する場面は、標準溶液の調製、試薬溶液の希釈調製、標準溶液や検体、試薬溶液を 96 ウェルプレートに分注するところです。これらの作業で再現性良く分注するために、手慣れたピペットのご使用をお薦めします。プッシュボタンを一定の力で押せるピペットをお薦めします。
ピペット選択について
96 ウェルプレートへの分注量は 5μL、10μL、50μL、100μL などさまざまです。5μL 分注する時は最大 10μLのピペットを、50μL 分注する時は最大 100μL のピペットを選択するなど適切なピペットを使用しましょう。
96 ウェル全てに分注する際には連続分注器のご使用をお薦めします。また、メンテナンスされた電動ピペットもお薦めです。
ポイント③;プレートへの分注
分注前の準備
- 96 ウェルプレートのアドレスを作成しましょう。どのウェルに何を入れるかを確認しましょう。
- 96 ウェルプレートのシールは室温に戻してから剥がしましょう。
- ストリップタイプのプレートの場合は外れてしまった時のためにストリップの端に油性ペンで No. を書きましょう。
- キットの全試薬の室温化が必要な場合は室温に戻してから使用するようにしましょう(1 時間半〜 2 時間必要)。特に緩衝液、洗浄液は重要です。
各標準溶液の分注時
- 0 濃度(Blank)、一番薄い濃度の標準溶液から分注しましょう。連続分注時も薄い濃度のウェルから分注することをお薦めします。
- 20 分前後で 1 プレート全てに分注できるようにしましょう。高感度タイプでは特にプレートの乾燥に注意しましょう。
- 連続分注時を除きチップは 1 ウェル毎に交換することをお薦めします。
- 検体の希釈が必要な時は事前に希釈したものを用意しておきましょう。
- 標準溶液、検体、第二抗体の入れ忘れに注意しましょう。
- 泡を立てないように分注しましょう。
96 ウェルプレートに分注する際にプレートのズレが気になる方へ。100 円ショップで販売している玄関マットなどのスベリ止めをプレートの下に敷き操作をすると便利です。
ポイント④;チップ使用法
チップ使用法のポイントに 2 つの方法があります。どちらか一方に統一して使用しましょう。
プレウェッティング法
- 新しいチップをセットした後、採取する溶液を第一ストップ(プランジャーが最初に止まる所)の範囲で 1 〜 2 回吸い上げ、放出する「プレウェッティング」を行った後、溶液を満たします。
- チップの先端を容器の内壁に軽くタッチし先端の外側についている溶液を除去し取り出します(タッチ&ゴー)(図1)。
- チップの先端をウェルの内壁から少し離し、溶液を排出します。この時プッシュボタンを最後まで押し、溶液を完全に排出します(ブローアウト)。
- ウェルの内壁でタッチ&ゴーを行ってピペットを抜き出し、チップを交換します。この時チップ先端で内壁を擦らないように注意しましょう。
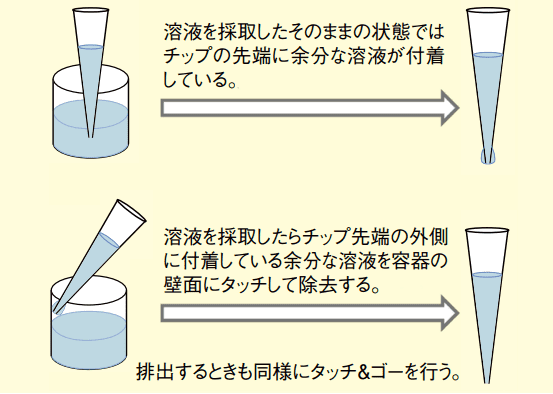
共洗い法
この方法は緩衝液などが既にウェルやチューブに入っている場合に適用できます。微量な検体、微量な各標準溶液の分注作業時などにお薦めします。
- 新しいチップをセットし、第一ストップまでプッシュボタンを押し下げ、採取する溶液を静かに吸い上げます。
- 容器の内壁でタッチ&ゴーを行いピペットを取り出します。
- 緩衝液などが既に入っているウェルにチップの先端を入れて溶液を放出し、第一ストップの範囲内で 1 〜 2 回プッシュボタンを上下して「共洗い」します。最後にブローアウトします。
- ウェルの内壁でタッチ&ゴーを行いピペットを抜き出し、チップを交換します。この時、チップの先を 96 ウェルプレートの内壁に擦らないように分注しましょう。
Q&A
Q:なぜ1検体1ウェルで測定してはいけないのでしょうか。
A:アッセイの操作法から考えると...
1ウェルでの測定結果をサポートする側面的データがないこと。もし測定操作に誤りやピペッティングの誤差があったとしても比較検討することができません。同一実験群の他の試料とかけ離れた結果でなければ一応測定操作に間違いはなかっただろうと推定することになりますが、本当にそれで良いのかと言う疑問が残ります。二重、三重測定ならばそれぞれの測定値がまとまっていれば測定操作に間違いがなかったと判定することができます。
それでは二重測定でも2つの測定値がかけ離れているときはどうするかと言うことなのですが、二重測定の場合にはどちらが異常なのか正しいのか判らないのです。従って、同一実験群に属する他の試料との比較で考えることになります。三重測定ならば他の2つからかけ離れている測定値は棄却することもできます。厳密に言えば棄却検定をした方が良いのですが試料数が少ないときには棄却することは難しくなります。特に二重測定では棄却検定のしようがありません。あまり変な値でなければ棄却しないで平均値を求める方が無難でしょう。
統計学的に考えると...
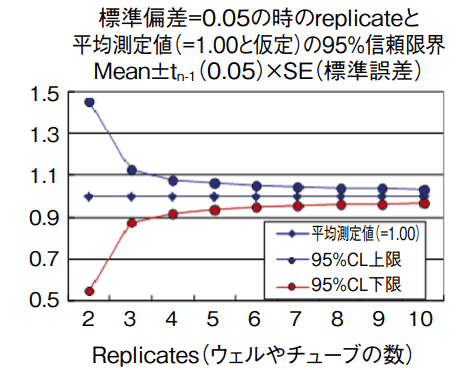
1ウェルの場合は自由度がゼロになります。したがって統計学的には信頼度はゼロです。二重、三重測定ならば平均値と標準誤差が計算できますので、測定値の95%信頼限界が判定できます。平均値の分布の形を示す標準誤差は試料数の平方根に反比例します。したがってレプリケートの数が多ければ平均値の信頼限界は狭くなり信用度は上がります。一方、標本の分布の形を示す標準偏差は試料数に関係なくほぼ一定なのですが、その信頼度は試料数に依存します。
次のグラフ(図2)は平均測定値を1、標準偏差を0. 05(つまり相対標準偏差あるいは変動係数を5%)と仮定した時、測定の繰り返し、即ちウェルの数と求められた平均値の95%信頼区間を示したものです。シングルアッセイは論外ですが、二重アッセイでの平均値の信頼区間は上下約50%となります。三重測定で区間は上下10%強です。二重測定は最低限行うようにしましょう。
次回は、「第3回 ELISA の操作法とそのポイント(中編)」の予定です。










