【連載】〈LC/MS分析 −測定原理から様々な分野での活用例−〉第3回 LC-MS/MSを用いた医薬品不純物としてのニトロソアミン類の測定
本記事は、和光純薬時報 Vol.92 No.2(2024年4月号)において、株式会社 エービー・サイエックス 事業戦略推進本部 テクニカルマーケティング 建田 潮様に執筆いただいたものです。
背景
ニトロソアミン(N-ニトロソアミン)類は、R2N-N=Oの化学構造を持つ有機化合物のグループであり、ほとんどの化合物が変異原性や発がん性を持つことが知られている1)。これらの化合物については環境影響や食物における影響などが知られていたが、医薬品においては2018年にバルサルタン原薬においてN-ニトロソジメチルアミン(NDMA)およびN-ニトロソジエチルアミン(NDEA)の混入が発見され2)、その後日本国内でもサルタン系医薬品、ラニチジン、ニザチジン、メトホルミンなどから検出され自主回収されている。そのため厚生労働省から、令和3年10月に混入リスクに関する自主点検を行う指導がありその中にはニトロソアミン類の測定が含まれている3)。また、欧州や米国をはじめ世界各国においても検査に関する通達がなされており、その中でLC-MS/MS(液体クロマトグラフィー-タンデム型質量分析計)も測定機器として挙げられている1, 4)。
医薬品におけるニトロソアミン類の定量
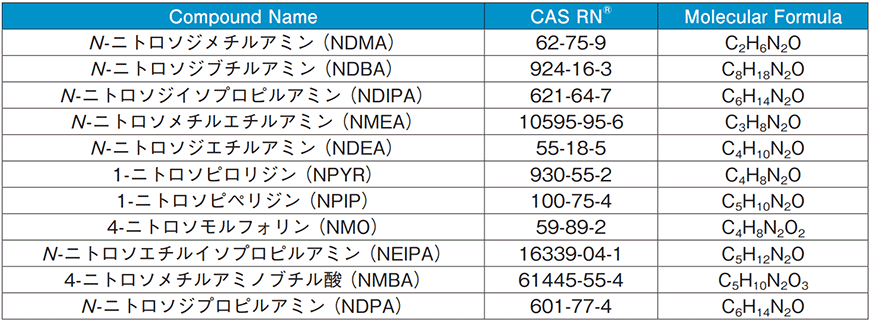
ニトロソアミンは、2級および3級のアミンと亜硝酸塩が存在することで生成される、窒素上の水素がニトロソ基に置換された構造を持つ有機化合物のグループである。サルタン類の医薬品では、当初これらが持つトリアゾール環と亜硝酸塩が反応することでニトロソアミン類が生成されると考えられていた1)。サルタン類の医薬品から検出された化合物はNDMAやNDEAのような化合物(Table 1)であり、液体クロマトグラフィー法、ガスクロマトグラフィー法、質量分析法などで測定できることが各種通達で示されている1, 3-4)。これら化合物は分子量が小さいものが多く、LC-MS/MSで測定する際にはエレクトロスプレーイオン化法(ESI)よりも大気圧化学イオン化法(APCI)のほうが適しているものが多い。
-
Table 1.測定対象となるニトロソアミン類
また、高選択なデータを得るために、四重極型の質量分離部を二つ持つLC-MS/MSで測定する場合、一つ目の質量分離部でプリカーサーイオンを選択、二つ目でプロダクトイオンを選択し、組成と構造両面でフィルタリングできるMRM (Multiple Reaction Monitoring)という測定モードが使用される。テルミサルタン製剤中の8種のニトロソアミン類を、四重極型のLC-MS/MSであるSCIEX Triple Quad™ 5500+ LC-MS/MS System−QTRAP® Readyによって測定した例を示す(Fig.1)5)。
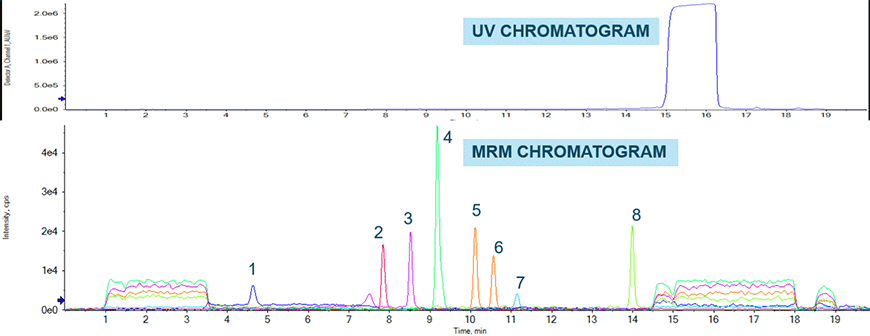
Fig.1 テルミサルタン中のニトロソアミン類の測定
1. NDMA 2. NMBA 3. NDEA 4. NEIPA 5. NDIPA 6. NDPA 7. NMPA 8. NDBA
医薬品や原薬中のニトロソアミン類を定量する際は、分析上の注意点として、大量に含まれるそれらが測定対象のイオン化に影響をしないようにピーク分離をする。また、分子量の小さい化合物を測定する際に共通する点として、バックグラウンドの低減のため移動相などには純度の高い溶媒を使用することが求められる。分析試料についての注意点として、それらマトリクス中に2/3級のアミンを持つ化合物が含まれる場合に、分析系内でニトロソアミン類が生成される可能性も考慮に入れる必要がある。
当初はトリアゾール環をもつサルタン系の医薬品からの検出であったが、その後ピオグリダゾン原薬をはじめ、ラニチジン、ニザチジン、メトホルミンなどその構造を持たない医薬品からも検出された1)。基本的には四重極型のLC-MS/MSでの検出が可能となっているが、対象となる化合物の増加などにより、より選択性の高い方法として、飛行時間型の質量分離部をもちより高分離、高精度な質量分析が可能なQ-TOF型の装置などを用いた高分解能定量も注目を集めている。メトホルミン製剤中の9種のニトロソアミン類の、X500B QTOFシステムを用いた定量分析の例を示す(Fig.2)6)。
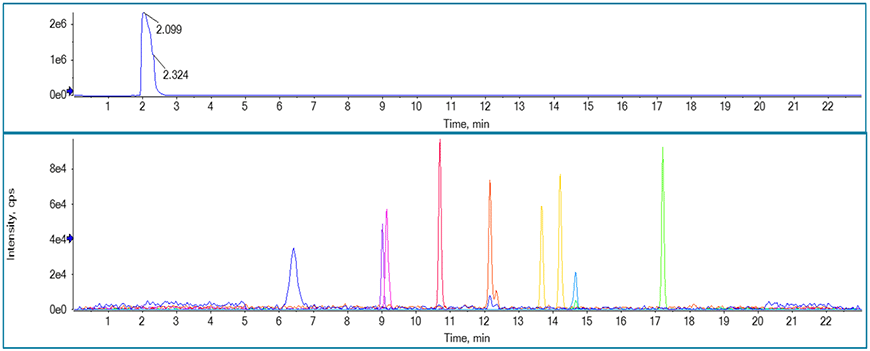
Fig.2 メトホルミン製剤中のニトロソアミン類の測定
左から順にNDMA ; NMO ; NMBA ; NDEA ; NEIPA ; NDIPA ; NDPA ; NMPA ; NDBA
四重極では整数値のm/zでしか分離できないのに対し、Q-TOF型では小数点第二位以下での分離が可能であり、よりバックグラウンドの低いクロマトグラムが得られている。また、FDAは2020年7月に、NDMAとDMFが共溶出し、定量結果が真値より高くなる可能性があることが記載された論文を発表している7)。四重極型ではこれら二つを質量で分離することはできず、クロマトグラムでの分離が必要となるが、Q-TOF型などの高い質量分離能での測定が可能な装置を用いることで、NDMAとDMFを質量分離した上での測定が可能である(Fig.3)6)。
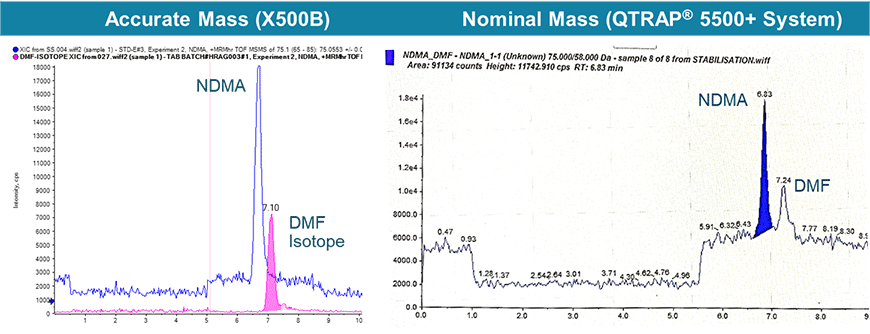
Fig.3 NDMAとDMFの高分解能装置での分離
感度の良い装置を使用し、注入するサンプル中の医薬品の量を減らすことは測定の安定性を上げるうえで重要である。メトホルミン製剤中の10種のニトロソアミン類を、SCIEX 7500システムで測定した例を示す (Table 2)8)。
-
Table 2.超高感度LC-MS/MSを用いたニトロソアミン類の測定
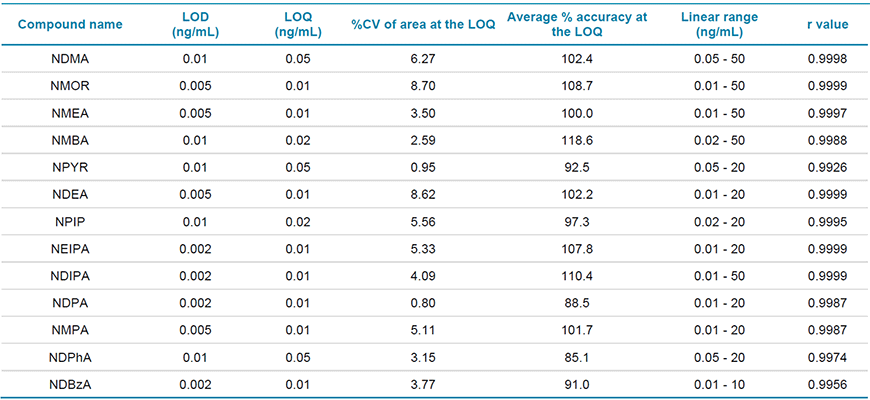
この装置では、NDMAについて溶液中濃度0.01 ng/mLを検出下限値として測定できており、他の装置のおよそ10倍以上の感度で測定できている。これを用いることにより、サンプルの注入量を1/10にすることができ、装置の安定した使用が可能となる。
原薬のニトロソアミン化物の測定
前述したように、ほとんどのR2N-N=Oの化学構造を持つ有機化合物は程度の差はあるが変異原性や発がん性を持つ。そのため近年では原薬中のアミンにニトロソ基が付加した化合物の測定が取りざたされるようになってきている。これらはニトロソアミン原薬関連不純物と呼ばれ、各国で基準値の策定などが進んでいる9, 10)。いくつかの医薬品がニトロソ基を持った構造を図示する(Fig.4)。
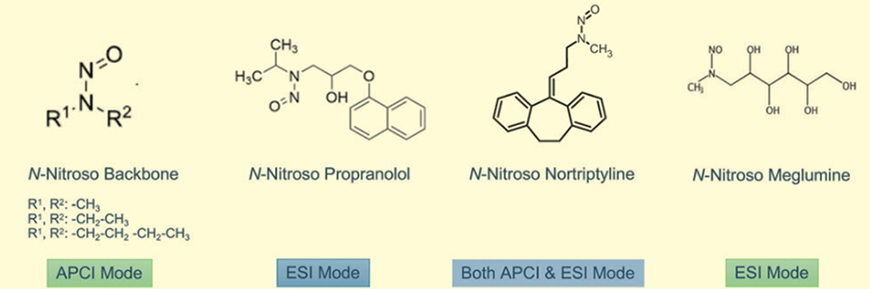
Fig.4 ニトロソアミン原薬関連不純物の構造の一例
これらは、前述したNDMAなどと異なり、もともとの原薬の構造によってはLC-MS/MSでのイオン化がAPCI法ではなくESI法のほうが適している場合もある。また、溶解性などについても原薬由来の性質によることも多くなるため、抽出などの処理においては注意が必要となる。模式的な例として、QTRAP 6500+ システムを用いたニトロソプロプラノロールの測定事例を示す(Fig.5)。
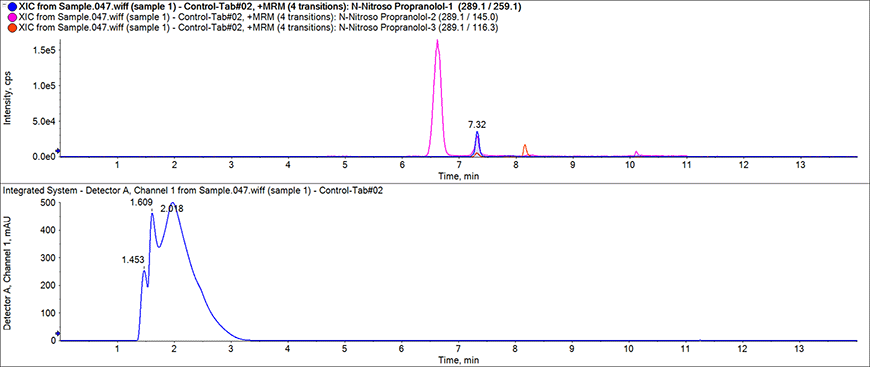
Fig.5 N-ニトロソプロプラノロールの測定例
図中に示した3つのプロダクトイオンについてMRMトランジションを組み測定を行ったところ、保持時間が6.6分、7.3分、8.2分にそれぞれピークがあらわれた。7.3分のみ、すべてのMRMトランジションのピークが重なっていることから、このピークがN-ニトロソプロプラノロール由来のピークであることが確認できた。しかしながら、6.6分、8.2分のそれぞれのピークが何らかのニトロソ化不純物である可能性を捨てることはできない。今後はこのようなピークについての同定/定量が可能な高分解能型の装置での分析が必要となることが予測される。
まとめ
ニトロソアミン類の測定における、現時点でのLC-MS/MSの有用性を示した。発がん性や変異原性を持つ場合の多いこれら化合物については、今後より広範な化合物の測定が必要になる。そのため、定性/定量分析の両面が可能なLC-MS/MSでの分析が必要とされる場面も増えていくと思われる。
参考文献
- Nitrosamines EMEA-H-A5(3)-1490-Assessment report (2020).
- 厚生労働省 平成30年度第8回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会 資料
- 令和3年10月8日 薬生薬審発1008第1号 薬生安発1008第1号 薬生監麻発1008第1号 医薬品におけるニトロソアミン類の混入リスクに関する自主点検について
- Information about Nitrosamine Impurities in Medications
(https://www.fda.gov/drugs/drug-safety-and-availability/information-about-nitrosamine-impurities-medications#updates) - Choudhary, S. et al. : Quantification of genotoxic nitrosamines in a telmisartan drug product.
- Choudhary, S. et al. : Analysis of nitrosamine impurities in a metformin drug substance and drug product.
- Yang, J. et al. : AAPS J., 22 (4), 89 (2020).
- Steed, J. et al. : Enhanced sensitivity for nitrosamine analysis in a metformin active pharmaceutical ingredient (API).
- Recommended Acceptable Intake Limits for Nitrosamine Drug Substance-Related Impurities (NDSRIs) (2023).
(https://www.fda.gov/regulatory-information/search-fda-guidance-documents/updated-information-recommended-acceptable-intake-limits-nitrosamine-drug-substance-related) - Questions and answers for marketing authorisation holders/applicants on the CHMP Opinion for the Article 5 (3)of Regulation (EC) No 726/2004 referral on nitrosamine impurities in human medicinal products (2024).




