【テクニカルレポート】創薬の安全性試験におけるヒトiPS 細胞由来心筋細胞を用いた 評価の重要性
本記事は、和光純薬時報 Vol.89 No.2(2021年4月号)において、富士フイルム株式会社 バイオサイエンス&エンジニアリング研究所 森村 馨様に執筆いただいたものです。
安全性薬理試験のガイドライン
現在、医薬品開発において実施すべき安全性試験は、その実施時期とともに ICH ※ 1 で定めた国際ガイドラインに規定されている1)。
安全性試験の中でも、安全性薬理試験は生命維持機能に関わる心血管系、中枢神経系及び呼吸器の安全性を評価する極めて重要な試験であり、ヒト臨床試験の前に行われるべき試験として ICH S7A/S7B で規定されている2)。ICH S7A には、安全性薬理試験の一般原則と推奨事項が記載されており、ICH S7B は、特に被験物質の心室再分極延長を評価するための非臨床試験の進め方について述べられている3)。
実際の医薬品開発における安全性薬理試験の進め方
実際の医薬品開発においては、ICH S7A/S7B に従い、探索早期ではスクリーニング試験として、培養細胞を用いたhERG 試験※ 2 を実施し、臨床試験手前の探索後期では化合物の見極めとして、大動物(イヌやサルなど)を用いたテレメトリー試験※ 3 を実施している。
hERG 試験は、心電図におけるQT間隔の延長に関わるIKr チャネルの阻害作用を評価する試験である。電流の阻害のみを見るため結果が明瞭であり、自動で測定できる機器も普及している。
しかしながら、心室筋の活動電位には IKr チャネル以外にも様々なイオンチャネルが関与しており、hERG 試験の結果と臨床結果が一致しないケースも報告されている4)。その為、hERG 試験の結果だけで判断してしまうと、有用な医薬品候補を開発初期に除外してしまう可能性やヒトでのQT 間隔延長リスクを正確に評価できない可能性が示唆されている。
実際に、hERG 試験では陰性だったものの、大動物のテレメトリー試験で心電図QT 間隔の延長や心臓の収縮・弛緩などへの影響が見られ、医薬品開発が中止となることがある。テレメトリー試験はhERG試験に比べて必要な化合物量も多く、この段階での開発中止は時間とコストの大幅なロスになり得る。
このような開発後期の医薬品開発中止を避けるため、hERG 試験とテレメトリー試験を繋ぐ様々なフォローアップ試験が実施されている。その代表例として、IKrチャネル以外の心室筋の活動電位に関わるNa チャネルや、Ca チャネルのイオンチャネル阻害試験、摘出心臓を用いたAPD 試験※ 4 やランゲンドルフ灌流心試験※ 5 などを実施し、統合的なリスク評価をしている。非臨床試験間または、臨床−非臨床試験間で結果が異なる場合は、ICH のガイドライン上でもフォローアップ試験を推奨しており、フォローアップ試験は統合的リスク評価を構成する重要な要素となる。
しかし、複数のイオンチャネルに対する阻害評価は、コストが増加する一方、複数チャネルへの複合作用による臨床での影響までは評価できていない。また、摘出した組織を用いた試験(APD 試験やランゲンドルフ灌流心試験)は実験手技の熟練を要し、スループットも低いことが課題となっている。
以上のことから、早期に臨床予測性が高く統合的なリスク評価が可能な細胞(in vitro )試験系が求められている。
ヒトiPS細胞由来心筋細胞を用いたQT 間隔延長評価
そのような背景から、2013 年12 月に、日本製薬工業協会を母体としたヒトiPS 細胞応用安全性評価コンソーシアム(以後CSAHiと記載)※ 6 が発足した。発足以来CSAHi では、医薬品の安全性で特に問題となる心臓、肝臓、神経について、ヒトiPS 細胞由来分化細胞を用いた各種安全性評価技術開発とその応用可能性を検証し、実用化に向けた活動を行ってきた。
特にヒトiPS 細胞由来心筋細胞 (以後iPS 心筋と記載) を用いた心毒性評価系の構築が推し進められてきた。その中でもMEA ※ 7 を用いた培養iPS 心筋の細胞外電位波形の評価系は高精度でリスク予測ができる系として確立されつつある。MEA 評価系は、iPS 心筋に存在する様々なイオンチャネルの電気活動を複合した波形で取得するため、QT 間隔の評価だけでなく、動物実験でしか検出できなかった致死性不整脈(TdP ※ 8)の原因となるEAD(early afterdepolarization:早期後脱分極)も検出できる。実際、日本国内で行ったバリデーション試験において、MEA 評価系の臨床予測精度は83% となっており、hERG 試験(72%)に比べ、精度が向上していることが分かっている5,6)(下図;iPS 心筋評価の臨床予測率)。その一方、使用するiPS心筋の種類によって、イオンチャネルの発現が大きく異なることが報告されていることから7)、iPS 心筋の種類及びロットの選択はMEA を用いた心毒性評価の予測精度を向上する上で重要であると考えている。
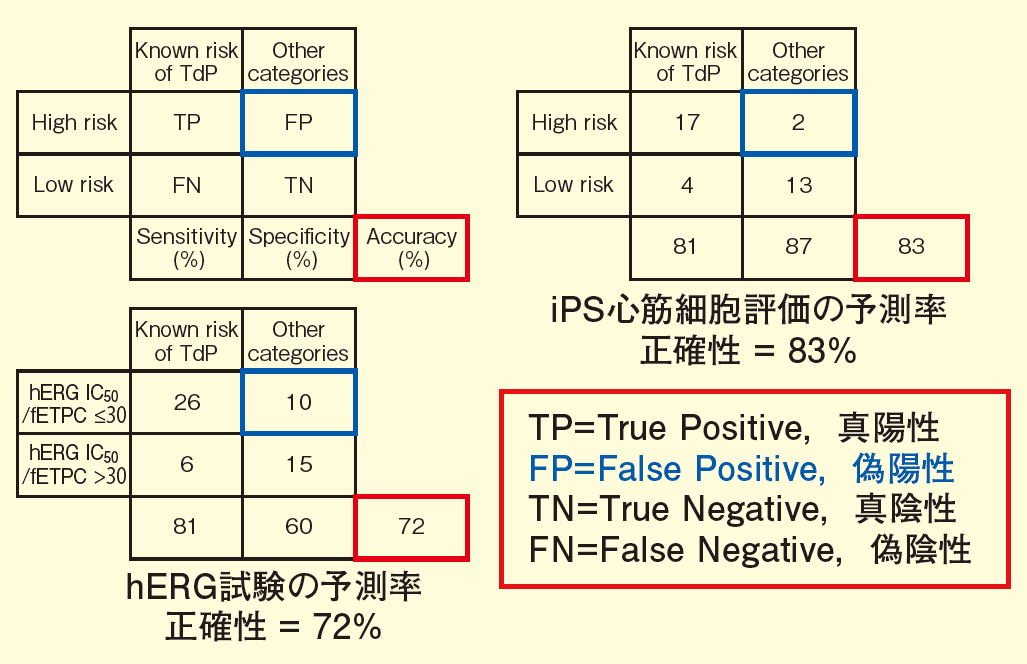
iPS 心筋評価の臨床予測率6)
iPS 心筋を用いた心毒性評価は、CSAHiの活動だけではなく、国立医薬品食品衛生研究所を母体とするJiCSA ※ 9、FDAが母体のCiPA ※ 10 などと協力して国際的バリデーション試験が実施されてきた。これらの活動が実を結び、2020 年10 月にiPS 心筋の利用などが記載された ICH E14/S7B のQ&A案が公開された。
ガイドラインの案文にはフォローアップ試験の項目にiPS 心筋を用いたMEA 評価系も記載されている8)。今後、ICH E14/S7B のQ&A が最終化され、iPS 心筋を用いた心毒性評価の実用化が促進されると考えられる。
今後の展望
現在、iPS 心筋を用いた心毒性評価の研究は更に進んでおり、今まで動物実験でしか評価ができなかった、収縮・弛緩系の評価系構築も進められている。収縮・弛緩系の評価についても、QT 評価と同様に国内外でバリデーション試験が実施されることが予想され、iPS 心筋を用いた収縮・弛緩系の評価が可能になれば、現況のフォローアップ試験で実施されているランゲンドルフ灌流心試験の代替としてさらなる活用が期待できる(下図;安全性薬理試験のフロー)。
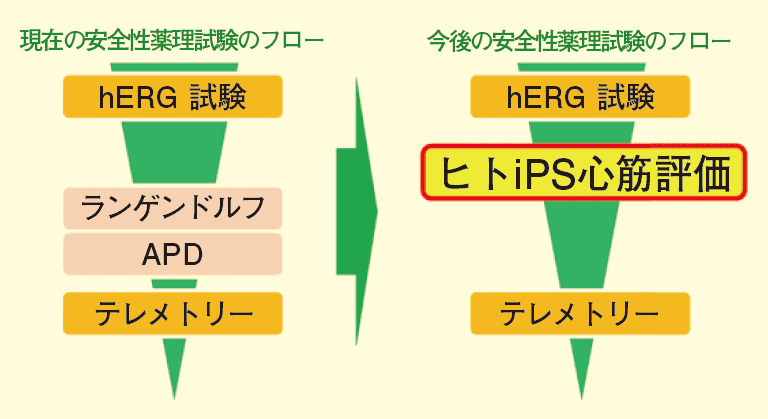
安全性薬理試験のフロー
まずはスタート地点に立ったiPS 心筋を用いた安全性評価であるが、今後は様々な薬剤の開発に利用され、これまでhERG試験の偽陽性判定により除外されていた薬剤の救済や、hERG 以外のチャネルによる心毒性リスクを提示できれば、医薬品開発の成功確立の向上に貢献できるであろう。iPS 心筋を用いた評価の実績が積まれていくことで、動物実験の削減や評価効率化に繋がり、より良い医薬品が早く世に送り出されることを期待したい。
参考文献
- ICH-M3「医薬品の臨床試験のための非臨床安全性試験の実施時期についてのガイドライン」,医薬審第1019 号,2000.12.27 改正.
- ICH-S7A「安全性薬理試験ガイドライン」,医薬審発第902 号,2001 年.
- ICH-S7B「ヒト用医薬品の心室再分極遅延(QT間隔延長)の潜在的可能性に関する非臨床的評価」,薬食審査 発 1023 第4 号,2009 年.
- Gintant, G. : Pharmacol, Ther., 129 (2), 109 (2011). DOI: 10.1016/j.pharmthera.2010.08.008
- Nozaki, Y. et al. : Regul. Toxicol. Pharmacol., 88, 238 (2017). DOI: 10.1016/j.yrtph.2017.06.006
- Ando, H. et al. : J. Pharmacol. Toxicol. Methods, 84, 111 (2017). DOI: 10.1016/j.vascn.2016.12.003
- Kodama, M. et al. : J. Pharmacol. Sci., 140 (4), 325 (2019). DOI: 10.1016/j.jphs.2019.06.006
- Gintant, G. et al. : Regul. Toxicol. Pharmacol., 117, 104756 (2020). DOI: 10.1016/j.yrtph.2020.104756
キーワード
※1. ICH(International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use): 医薬品規制調和国際会議
医薬品規制当局と製薬業界の代表者が協働して、医薬品規制に関するガイドラインを科学的・技術的な観点から作成する国際会議のこと。ここで決まったガイドラインは、世界の標準的な指針となる。
※2. hERG(human ether-a-go-go-related gene)試験
心筋細胞に存在するカリウムチャネルの1つであるhERG チャネルに対して医薬品候補化合物の阻害作用を確認する試験。hERG チャネルが化合物に阻害されるとQT 間隔が延長し、不整脈が起きる可能性が高くなる。
※3. テレメトリー試験
イヌやサルなどの大動物に送信機を埋め込み、医薬品候補化合物が心臓へ与える影響を測定する。近年、ジャケットを被せて測定する非侵襲な方法や、ミニブタを用いる検討なども進められている。
※4. APD(Action Potential Duration)試験
活動電位持続時間の延長を検出する試験。モルモットなど動物から摘出した乳頭筋標本を用いた試験が広く行われている。
※5. ランゲンドルフ灌流心試験
モルモットなどの動物から摘出した心臓を用い、QT 間隔延長だけでなく伝搬や収縮・弛緩など、心臓への様々な影響を総合的に評価する実験方法。
※6. CSAHi(Consortium for Safety Assessment using Human iPS Cells)
ヒトiPS 細胞由来分化心筋・肝臓・神経細胞を用いた各種安全性評価技術について、新規医薬品開発への応用可能性を実験的に検証し、将来的展望も含め実用に向け世の中に提言することを目的とした組織。2021年1 月29 日現在、国内外の47 の企業・機関が加盟している。
※7. MEA(Microelectrode array)
微小電極アレイシステム法。アレイ状に配置された電子センサ上に細胞を培養したり、組織を置くことで、細胞外電位を測定する。
※8. TdP(Torsades de Pointes)
重症型不整脈の一例であり、突然死の原因となる特徴的な多型性心室頻脈。心電図上でねじれながら振動するように見えることから名付けられた。市場から医薬品が回収される理由の一つ。
※9. JiCSA(Japan iPS Cardiac Safety Assessment)
ヒトiPS 細胞由来心筋細胞を医薬品の安全性評価に応用することを目的に、産・官・学で構成されたオールジャパン体制の研究グループ。
※10. CiPA(Comprehensive in vitro Proarrhythmia Assay)
米国FDA(食品医薬品局)を中心に組織された国際コンソーシアムで、ヒトiPS 心筋細胞などを含めた統合的な催不整脈リスク予測法の確立を目指している。




