【テクニカルレポート】細胞懸濁保存液セルストア®S及び細胞洗浄保存液セルストア®W を用いたヒト脂肪由来間葉系幹細胞の保存例
本記事は、和光純薬時報 Vol.88 No.3(2020年7月号)において、株式会社大塚製薬工場 研究開発センター 鳴門研究所 藤田 泰毅様に執筆いただいたものです。
はじめに
幹細胞治療においては、細胞を懸濁・保存するために、しばしば生理食塩液が用いられているが、細胞生存率の維持や細胞の沈殿の抑制の観点から必ずしも理想的な溶液ではない 1)。
我々は、タンパク質や細胞膜の安定化剤、凍害防止剤としての効果が知られているトレハロースに着目し、ヒト脂肪由来間葉系幹細胞(hADSCs)の 5℃及び 25℃保存においても有効であることを見出した 1)(特許取得済み)。
また、細胞の保存中に細胞は沈降し濃度の均一性が失われるが、血漿増量剤として臨床使用されているデキストラン40 を細胞保存液に添加することにより、細胞保存液の粘度と比重を上昇させ、細胞沈降を抑制することが可能である 1)。
これらの成分濃度について検討を行い、細胞懸濁保存液として3% トレハロース及び 5% デキストラン添加乳酸リンゲル液であるセルストア®S を、細胞洗浄保存液として3% トレハロース添加乳酸リンゲル液であるセルストア®W を開発した 1)(研究用試薬として富士フイルム和光純薬株式会社より販売)。以下に、使用例を記載する。
細胞特性の保存
使用例1.hADSCsの細胞生存率
培養した hADSCs を Trypsin/EDTAを用いて剥離し、セルストア®S、セルストア®W、乳酸リンゲル液もしくは市販の冷蔵用保存液に 5×105 cells/mLの濃度で懸濁し細胞低吸着遠沈管(ステムフル®、住友ベークライト株式会社)に分注した。5℃または 25℃の温度条件で静置し、経時的にトリパンブルー染色により細胞生存率を測定した。いずれの温度においても、24 時間保存後の細胞生存率は、セルストア®S、セルストア®W ともに 90% 以上であった(図 1)。
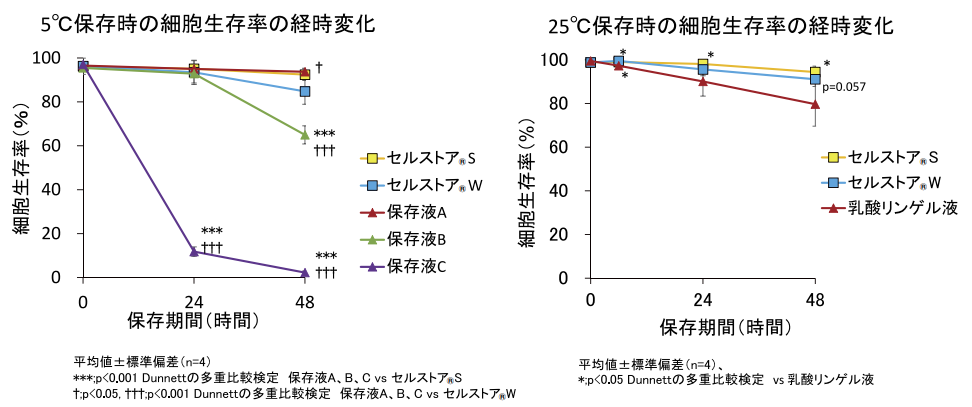
図1.5℃あるいは 25℃保存時の細胞生存率の経時変化
セルストア®S における細胞生存率は、5℃保存後 48 時間において保存液 B 及び C に比して有意に高く、保存液 A と同様な値であり、25℃保存後 6 時間から 48 時間まで乳酸リンゲル液に比して有意に高かった。セルストア®W における細胞生存率は、5℃、24 時間において保存液 C に比して有意に高く、保存液 A 及び B と同様な値であり、25℃において乳酸リンゲル液に比して 6 時間で有意に高く、48 時間で高い傾向があった。
使用例2.hADSCsのコロニー形成率
hADSCs をセルストア®S またはセルストア®W に懸濁し、懸濁直後あるいは 5℃または 25℃で 24 時間保存後に再播種し、コロニー形成率を評価した。いずれの条件においても、24 時間保存後のコロニー形成率は、懸濁直後のコロニー形成率(約 20%)に対し有意な差は認められず、hADSCsの増殖能は保存されていると考えられた(図 2)。
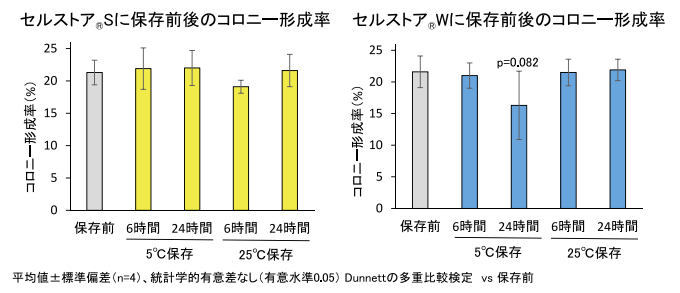
図2.コロニー形成率の確認
使用例3.hADSCsの細胞表面抗原陽性率
hADSCs をセルストア®S またはセルストア®W で懸濁し、懸濁直後あるいは 5℃または 25℃で 24 時間保存後に細胞表面マーカーの陽性率を評価した。保存前後において、間葉系幹細胞の陰性マーカー(CD14 及び CD45)は5%以下、陽性マーカー(CD73、CD90及び CD105)は 90%以上であった 1)。
使用例4.hADSCsの脂肪分化能ならびに骨分化能
hADSCs をセルストア®S またはセルストア®W で懸濁し、懸濁直後あるいは 5℃または 25℃で 24 時間保存後に、脂肪細胞あるいは骨芽細胞への分化誘導を行ったところ、それぞれオイルレッド染色による油滴の確認により脂肪分化能が、アルカリホスファターゼ染色及びアリザリンレッド S 染色による石灰化の確認により骨分化能が保存されていることを確認した 1)。
細胞濃度の均一性維持
hADSCs をセルストア®S あるいは生理食塩液に 1.5×105 cells/mL の濃度で懸濁し 100mL を血液バッグに入れスタンドに吊るし、1 時間静置した後に、輸血セットから 3.3mL/min の速度で排出させ、5mL ずつ細胞低吸着遠沈管に回収した。最悪のケースを想定して、1 時間静置後に攪拌はせず、滴下が半分終了した 10 本目の回収後にバッグを手で揉み攪拌した。血液バッグからの排出ライン中の細胞濃度は、生理食塩液に比してセルストア®Sでは、より安定することを確認した 1)(図 3)。
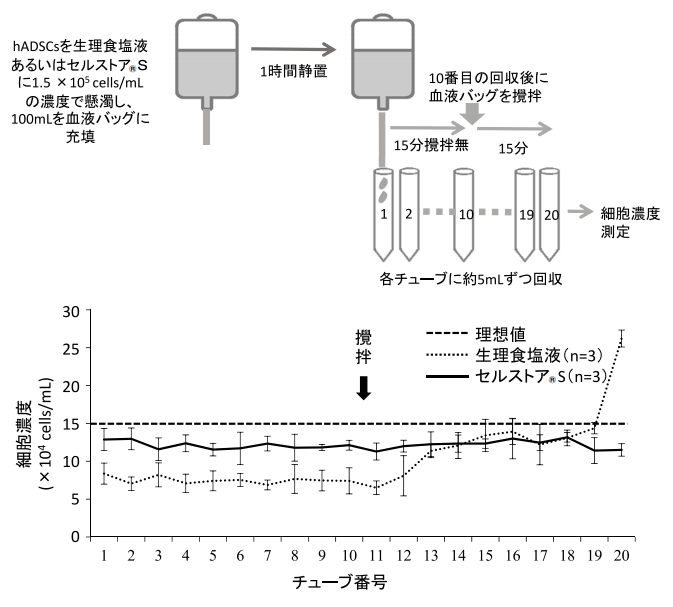
図3.血液バッグから排出される細胞濃度の経時変化
各チューブの細胞濃度について、平均値±標準偏差を示した。結語
セルストア®S及びセルストア®Wは、5℃または 25℃の温度条件で少なくとも 24 時間、hADSCs の細胞特性を保持した。また、セルストア®S は、少なくとも 1 時間、細胞濃度の均一性を維持した。ただし、保存可能時間は、使用する細胞の種類や状態、保存条件によって異なるため、使用する細胞での確認試験が必要となる。
本品は、間葉系幹細胞等の基礎研究に貢献するとともに、再生医療等製品への応用につながるものと期待している。
参考文献
- Fujita, Y, et al. : Regen, Ther., 14, 95 (2020). doi: 10.1016/j.reth.2019.10.004




