【特別講座】NAD(P)非依存な固定化不斉酸化触媒「SanCat-Super」について
本記事は、OrganicSquare No.59 (2017年3月号)において、サンヨー食品株式会社 開発本部開発部 永岡 宏行様に執筆いただいたものです。
はじめに
エンドウ豆由来ヘム蛋白質による"NAD(P)非依存な不斉酸化反応(SanCat-R:5g、WAKO-No.351-34213)"は、論文報告済となっており、1)以前の本総説(Wako Organic Square 44, 22 (2013))で紹介済である。2) 今回は更に、該当ヘム蛋白質が、蛍光菌由来 HasA(Heme-Acquisition system A)であることを突止め、それを多孔質セラミック担体(トヨナイト200:東洋電化工業製)3)へ吸着固定して、新たに"有機溶媒耐性・デラセミ化反応"を賦与する固定化触媒「SanCat-Super」に発展させたので紹介する。
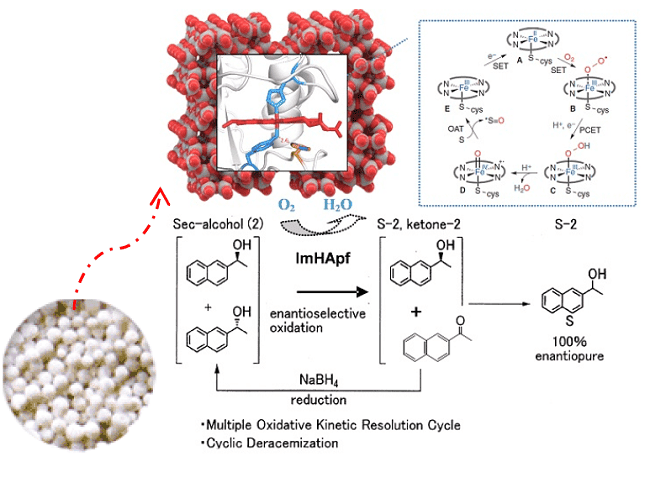
図1. SanCat-Superのイメージ
NAD(P) 非依存不斉酸化触媒-蛍光菌 HasA の調整
近年、ヘム蛋白質-チトクローム P450(反応活性種:Fe2+ ↔ Fe3+ with O2)の有するヒドロキシ化・エポキシ化・脱メチル化反応が報告されており、ヘム模倣型酸化反応-有機遷移金属触媒についても鋭意、研究されている。4)
化学工業において、"遷移金属による酸素駆動式酸化反応"は安全・コスト・簡便の点で期待が高い。しかし、酸化剤-過酸化水素水(H2O2)と還元剤-NAD(P)は不可欠といった課題もある。SanCat 不斉酸化の優位な点は、"過酸化水素水(H2O2)"と"NAD(P)"が不要、(固定によって)有機溶媒耐性とデラセミ化反応が可能な点にある。
更に、蛍光菌 HasA(200 mg~300 mg)の製造方法は、ベクター構築(pET28a-HASApf)後に BL21(DE3) 大腸菌体内に挿入、TL 培地(4L)中で培養(24h)後に菌体の超音波破砕→His-Tag 精製と平易である。また、該当変異菌体をグリセロールストックして何度も再利用することにより、HasA 生産コストは大幅に、低減化できる。
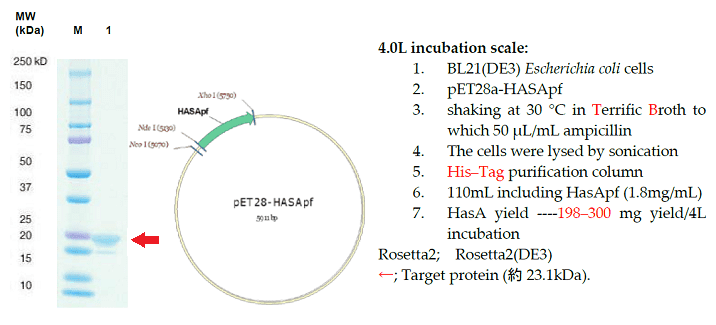
図2. SanCatの調整
ヘム蛋白質(ヘム鉄)の生理機能
遷移元素(鉄など)は複数の酸化数状態が可能、酸素配位による活性酸素種の再合成(反応活性種)が働き、例えば、チトクローム P450 のヘム鉄は、外来性カルボン酸が二酸化酸素と水に分解・無毒化に機能を持つことが知られている。ヘモグロビンのヘム鉄は、肺で酸素を受取り末梢まで運ぶ機能を持つ。
病原菌(緑膿菌や結核菌)由来 HasA「ヘム獲得タンパク質:Heme-Acquisition system A(分子量 21kDa)」は、「ヘムを奪い取る蛋白質」として知られるが、今回、HasA ヘム鉄もチトクローム P450 と同様に、酸素配位(酸化型ヘム低スピンg=2.8, 2.22, 1.72 のシグナル消失)する現象を突止め、蛍光菌 HasA も反応活性種と報告した。5)
以下、SanCatと菌本体、菌由来酵素、そして有機金属錯体との比較(メリット〇、デメリット×、基質特異的に高△)を表1にて整理する。
表1.SanCat の既存法との比較
| コスト | 補酵素 | 専門知識 | 菌培地 | 反応溶媒 | 立体選択性 | 後処理 | |
| 菌、組換え菌 | 低〇 | 不要〇 | 要× | 必要× | 緩衝液〇 | 高〇 | 滅菌× |
| 菌由来酵素 | 高× | 要× | 不要〇 | 不要〇 | 緩衝液〇 | 高〇 | 廃棄〇 |
| 有機金属錯体 | 高× | 不要〇 | 高× | 不要〇 | 有機溶媒/H2 圧× | 特異的-高△ | 重金属× |
| SanCat | 低〇 | 不要〇 | 不要〇 | 不要〇 | 緩衝液〇 | 高〇 | 廃棄〇 |
SanCat 使用例と比活性(Turnover 数、unit)
SanCat-Super(0.5 mg~6 mg)の不斉酸化反応は、試験管(18mm×15 mL)に撹拌子を入れ、1)フタ開放系にて、3)50mMグリシン NaOH 溶媒中(pH9.0、4mL)、4)基質溶液(40,000ppm、15μL(1.2 mM))を添加後、40℃で撹拌(700rpm)にて反応させる。反応後、SanCat-Super は濾過又は遠心にて分離できる。又、ヘキサン(又はジエチルエーテル)抽出後、基質 (40,000ppm、15µL(1.2mM))添加しても反応は進行する(有機溶媒耐性)。水素化ホウ素ナトリウム添加により、ワンポット・デラセミ化も進行する(図1)。6)

図3. SanCatの利用例
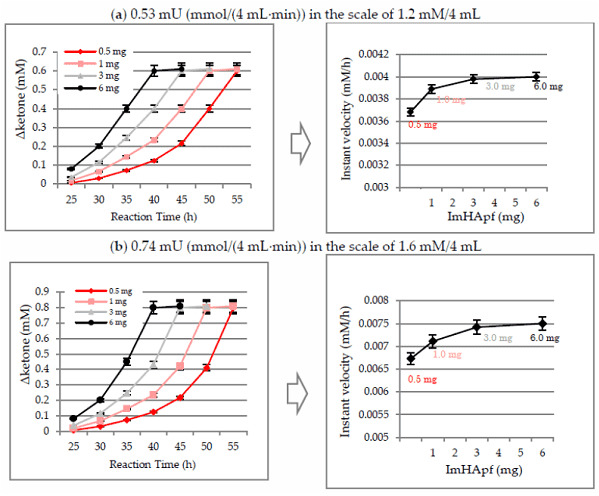
図4. SanCatによる比活性(Turnover数、unit)
固定化方法と HPLC 測定例
50mL -遠心管中に蛍光菌 HasApf(2.25 mg・4.5 mg・9.0 mg・18 mg/10mL-リン酸緩衝液(pH9.0))と多孔質セラミック担体(トヨナイト200:1.0g)を入れ、24 時間振とうさせて、その吸着性を調べた。吸着率は、ポータブル FT-IR システム(ATR 測定)・PANORAMA ソフトウェア(データ解析、検量線)を用いて作成した。6)
図 5 より、凡そ 16mg(0.0016µM)/gの HasApf が固定化されており、図 4 より、固定化酵素 0.5mg(0.0004µM)に対して、基質濃度 0.8mM(R 体のみ)に対して好適に作用することより、反応効率(Turnover)は凡そ 2 × 106、従って、比活性は 0.74 ± 0.03 mU/(mg·min) にあった。6) 尚、鏡像体過剰率 (ee) は、Daicel Chiralcel OB-H column (S-/R-isomer/ product ketone = 7.8 /8.8/11.6 min) 、HPLC LC-10A system (Shimadzu)、移動相(n-hexane/IPA = 9/1), 流速(1.0 mL/min)、温度30 °C、検出器 UV 254 nm. の条件で行える。1)
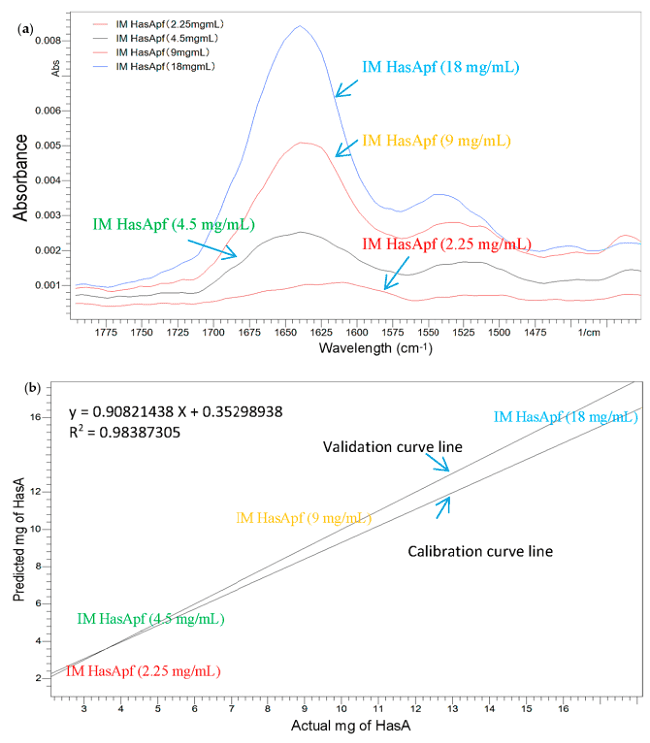
図5. SanCat変換のHPLC測定例
おわりに
光学活性体の比率は、医農薬分野、特に医薬品において 34%と上昇しており、ラセミスイッチ医薬品の動向を加えると、簡便で環境・安全・コストに配慮できる効率的な製造法の確立が求められている。酵素などの生体触媒反応は、水中で本来の機能を発揮するものであり、環境との調和を目指した有機合成化学の今後の展開にもますます重要な役割を担ってゆくものと期待できる。7)
今回、提案する SanCat-Super は、ヘム蛋白質内ヘム鉄の活性酸素再合成系(蛍光菌 HasA)を反応素子としており、ヘム不斉酸化反応といった類稀なヘテロ酵素触媒となっている。最後に、水条件下で光学異性体を分割合成する SanCat ヘム鉄の低環境負荷・安全・低コストな酸化反応が、益々、持続可能社会の構築に寄与することを期待したい。
参考文献
- a) Nagaoka, H. et al.: Biosci. Biotechnol. Biochem., 63, 1991 (1999). b) Nagaoka, H. et al.: Biosci. Biotechnol. Biochem., 64, 781 (2000). c) Nagaoka, H. et al.: Biosci. Biotechnol. Biochem., 65, 634 (2001). d) Nagaoka, H. Biotechnol. Prog., 19, 1149 (2003). e) Nagaoka, H. Biotechnol. Prog., 20, 128 (2004). f) Nagaoka, H. Biotechnol. Prog., 28, 953 (2012).
- Nagaoka, H.: Wako Organic Square 44, 22 (2013).
- Kamori, M. et al.: J. Mol. Catal. B Enzym., 9, 269 (2000).
- a) Nagaoka, H.: RSC Adv., 4, 16333 (2014). b) Nagaoka, H.: ACS Catal., 4, 553 (2014). c) Nagaoka, H.: Dalton Trans., 44, 13384 (2015).
- Nagaoka, H.: Catalysts., 6, 38 (2016).
- Nagaoka, H.: Biomolecules., 4, 41 (2016).
- 和光純薬時報 Vol.71(No.4), 1(2003).




