【連載】Talking of LAL「第12話 β-グルカン(2)」
本記事は、和光純薬時報 Vol.61 No.3(1993年7月号)において、和光純薬工業 土谷 正和が執筆したものです。
第12話 β-グルカン(2)
(1→3)-β-D-グルカンと LAL の反応に関して、その構造、濃度依存性、反応 kinetics 等、様々なアプローチの方法があると思います。構造に関しては、13C-NMR を用いた研究で、1 重らせん構造の状態では 3 重らせん構造の時より、100 倍も LAL 中のβ-グルカン感受性因子(G 因子)活性化能が高いことが報告されています1)。
濃度依存性に関しては、100~1000 ng/mL に反応の至適濃度があり、高濃度では LAL の活性化が起こらないことが報告されています2)。また、筆者らは、トキシノメーター ET-201(和光純薬)を用いた LAL と(1→3)-β-D-グルカンの反応 kinetics について報告しております3)。
今回は、このLAL と(1→3)-β-D-グルカンの反応 kinetcis について考えてみたいと思います。
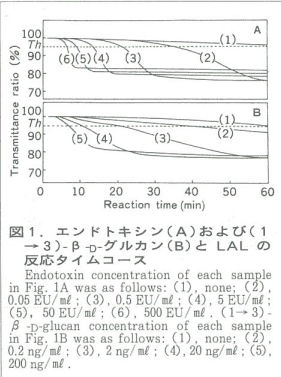
筆者らは、LAL の活性化における反応タイムコースを解析することにより、エンドトキシンとβ-D-グルカンが異なった反応を示すことを明らかにしました。すなわち、LAL とエンドトキシンの反応タイムコースは反応のラグが長く、ゲル化に伴う濁度変化が急激に起こるのに対し、LAL と(1→3)-β-D-グルカンの反応はラグが短いが、濁度変化は緩やかであるという特徴が認められたのです(図 1)。
そして、エンドトキシンと(1→3)-β-D-グルカンの混合物では両者の特徴が現れ、ラグが短く、途中から急激な濁度変化が起こりました。このように、エンドトキシンと(1→3)-β-D-グルカンの LAL に対する反応様式が異なることは、LAL 中に、C 因子(エンドトキシン感受性因子)系と G 因子系という異なった活性化経路があることとも関連していると思われます。
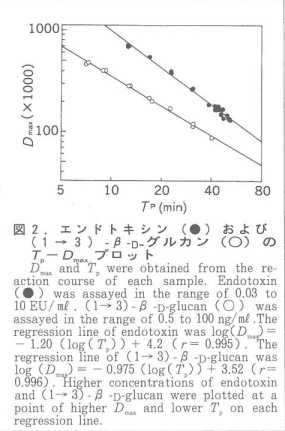
この違いを数値として扱うために、濁度変化の微分係数に着目しました。微分係数を算出するソフトウェアは、当社の ME 研究室で作ってもらいました。こうして解析した微分係数の最大値を Dmax とし、Dmax が得られるまでの反応時間を Tp として、これらをプロットすると、エンドトキシンと(1→3)-β-D-グルカンは異なった直線上にプロットされました(図2)。
筆者らは、この方法を Tp-Dmax プロットと名づけ、エンドトキシンとβ-グルカンの判別に利用しようとしたのですが、測定終了後に解析が必要であり、定量性・汎用性に問題があったため、実用化は見送りました。
しかし、反応タイムコースを見慣れてくると、Tp-Dmax プロットを行わなくても、LAL を活性化している主な物質がエンドトキシンかβ-グルカンかを見分けることができるようになります。この意味で、比濁時間分析法によって反応タイムコースを観察することにも意義があると思われます。このような情報は、ゲル化転倒法やエンドポイント合成基質法では得ることができないからです。
エンドトキシンと LAL の反応に比べると、(1→3)-β-D-グルカンと LAL の反応は、まだまだ研究の余地がありそうです。特に、複数の種類の結合や糖を持つ物質については、興味が持たれます。
次回は、少し趣を変えて「カブトガニ」の話をしたいと考えています。
参考文献
- Saito, H. et al. : Carbohydr. Res., 217, 181 (1991).
- Kakinuma, A. et al. : Biochem. Biophys. Res. Commun., 101, 434 (1981).
- Tsuchiya, M. et al. : Chem. Pharm. Bull., 38, 2523 (1990).
関連記事