【テクニカルレポート】iCell® ヘパトサイトを用いた胆汁酸排泄評価
本記事は、和光純薬時報 Vol.89 No.1(2021年1月号)において、崇城大学 生物生命学部 石田 誠一様に執筆いただいたものです。
ヒトiPS 細胞(hiPSC)の確立から10 年以上が経ち、様々な応用例が報告されている。hiPSC からヘパトサイトへの分化誘導については、Duncanのグループからの分化誘導法1)が基礎となり、様々な報告がされてきている。ヒトヘパトサイトについては、医薬品の代謝研究や安全性評価に多用されており国内の需要も多い一方で、ヒト肝臓由来の凍結肝細胞は資源を海外に頼っているため供給面での不安や倫理面からの問題も孕んでいる。
そのため、hiPSC などの幹細胞に由来するヘパトサイトの細胞資源としての期待は大きい。しかしながら、hiPSC に限らず、種々のヘパトサイトの分化誘導プロトコル2)はヒト発生における肝臓の形成過程3)を模倣しているが、in vitro の分化誘導系では新生児期の肝臓におけるヘパトサイトの活性を有するにとどまっているとされ、ヒト凍結肝細胞を越える細胞資源としての活用が進んでいない。
そのような中、我々は、iCell® ヘパトサイトが均質なヘパトサイト様細胞を供給できることに注目し、医薬品安全性評価への応用性を1)長期培養、2)薬物代謝酵素誘導性、3)胆汁排泄、4)脂肪蓄積の観点から検討した。その中で、iCell® ヘパトサイトを長期培養(図1)することで、毛細胆管様構造が形成されることを見いだした(図2A)。
培養方法は図1 に示すように、iCell® ヘパトサイトの融解・播種のプロトコルに従い細胞の培養を開始し5 日間の馴化培養の後、培地を長期培養用の培地に置き換え28 日間、培地交換をしつつ細胞を培養維持する。その後、マトリゲルを重層してサンドイッチ培養を開始するとともに、培地をCDI 社のMaintenance Medium に交換して毛細胆管を促すという比較的平易なもので、再現性も高い。
毛細胆管様構造を形成したiCell® ヘパトサイトについて、胆汁排泄を担う代表的なトランスポーターであるMRP2(Multidrug Resistance-associated Protein 2、ABCC2)とBSEP(Bile Salt Export Pump、ABCB11)の局在を免疫組織染色で確認すると、毛細胆管様構造に存在することが確認された(図2B、C)。毛細胆管様構造は、iCell® ヘパトサイトの培養面の全領域にほぼ均等に拡がっており、iCell® ヘパトサイトの細胞集団としての均質性が活かされていると考えられる。
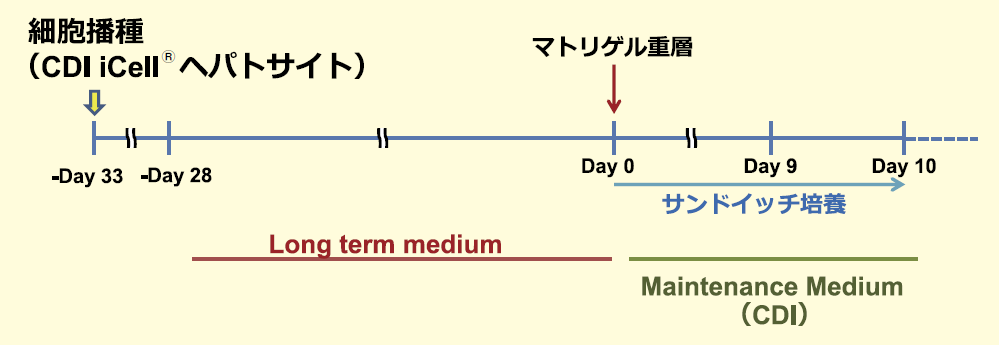
図1. iCell® ヘパトサイトを用いた胆管形成の培養プロトコル
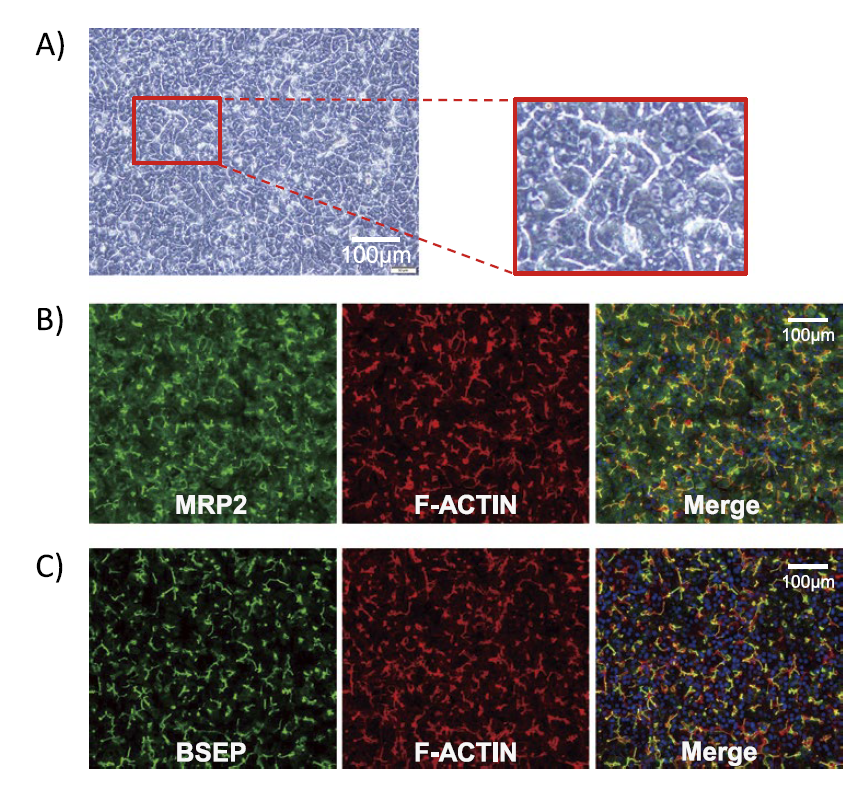
図2. A) iCell® ヘパトサイトで形成された毛細胆管様構造(位相差顕微鏡像)
B) MRP-2 の免疫組織染色
C) BSEP の免疫組織染色
このようにして形成された毛細胆管の胆汁排泄能をモデル蛍光基質FD(Fluorescein Diacetate)とTauro-nor THCA 24DBDを用いて検証した。FD はMRP2 の基質、Tauro-nor THCA 24DBD はBSEP の基質として知られている(図3A)。その結果、それぞれの基質が、iCell® ヘパトサイトに形成された毛細胆管様構造に特異的に排泄、蓄積することが見られ(図3B、C)、この排泄、蓄積はそれぞれのトランスポーターの特異的阻害剤で阻害された(data not shown)ことから、免疫組織染色で毛細胆管様構造に局在が確認されたMRP2、BSEP がそれぞれトランスポーターとして機能していることが確認された。
さらに、サンドイッチ培養開始後からの胆汁排泄能の維持期間を検討すると、16 日目でもほぼ同様の胆汁排泄能を維持していることが認められ(図3B、C)、iCell® ヘパトサイトを用いることで胆汁酸排泄が長期間にわたり評価できることが判明した。
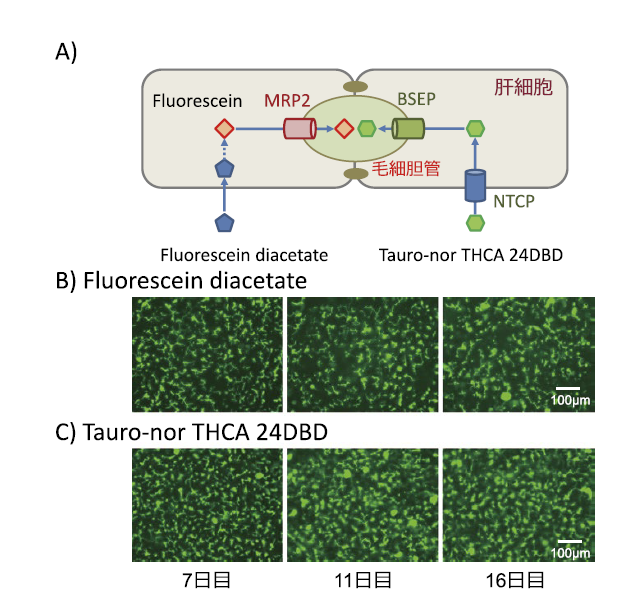
図3. A) Fluorescein diacetate とTauro-nor THCA 24DBD の取り込み・排泄機構
B) Fluorescein diacetate の毛細胆管様構造への排泄とその経日変化
C) Tauro-nor THCA 24DBD の毛細胆管様構造への排泄とその経日変化
以上の結果から、我々はiCell® ヘパトサイトを長期培養し、サンドイッチ培養と組み合わせることで、細胞培養面に均質に毛細胆管様構造を形成する培養法を確立できたと考えている。形成された毛細胆管様構造には胆汁排泄に関わるトランスポーターが適切に配向し機能しており、その活性が長期にわたることも確認できた。さらに、毛細胆管形成に重要なタイトジャンクションを破壊し毛細胆管様構造に蓄積された成分を定量することで、化合物の胆汁排泄を定量的に扱えることを確認している(未発表データ)。
医薬品開発の臨床試験で未だに薬物性肝障害により開発が中止になる例が散見されている。また、医薬品として認可後の市場撤退の理由としても薬物性肝障害が問題となっている。薬物性肝障害の主たる原因として、胆汁うっ滞型と胆汁うっ滞と肝細胞障害の複合型が知られている4)。重度肝障害への進展予後の予測はHy's Law という経験則に基づいて行われる5)が、基準となる数値は胆汁うっ滞と関連が深い。そのため、本稿で紹介したiCell®ヘパトサイトを用いた胆汁排泄能を有する培養系は、医薬品候補化合物の in vitro で胆汁うっ滞を予測する評価系として有用な手法となると考え、開発を進めている。
肝臓の胎児性マーカーであるAFP(alpha-fetoprotein)と成人肝マーカーであるalbumin の発現を定量的PCRで測定すると、培養初期ではAFP の発現が高いが長期培養するに従いAFP の発現は減少し、albumin の発現が上昇してくることから、細胞の成熟化が進行していることが予想される。長期培養することで毛細胆管様構造が形成されるメカニズムについても興味が持たれるところである。
iCell®ヘパトサイトを用いた胆管形成は均質性が高いので、毛細胆管形成の分子機構解明にも有用なツールとなると考えている。ヒトヘパトサイトは、接着性、非接着性や薬物代謝酵素の誘導性の有無などとともに毛細胆管形成によって品質評価がなされている。このような品質評価項目の基礎になる分子機構は未だに解明されておらず、本系での解析により、より安定的な毛細胆管形成が可能になることで薬物性肝障害のin vitro 評価系開発への貢献も期待される。
参考文献
- Si-Tayeb, K., Noto, F. K., Nagaoka, M., Li, J., Battle, M. A., Duris, C., North, P. E., Dalton, S. and Duncan, S. A. : Hepatology , 51, 297 (2010). DOI: 10.1002/hep.23354
- Yamaguchi, T., Matsuzaki, J., Katsuda, T., Saito, Y., Saito, H. and Ochiya, T. : Inflamm. Regen ., 39, 13 (2019). DOI: 10.1186/s41232-019-0102-4
- Si-Tayeb, K., Lemaigre, F. P. and Duncan, S. A. : Dev. Cell , 18, 175 (2010). DOI: 10.1016/j.devcel.2010.01.011
- 厚生労働省:重篤副作用疾患別対応マニュアル 薬物性肝障害(2008).
https://www.mhlw.go.jp/topics/2006/11/dl/tp1122-1i01.pdf - Temple, R. : Pharmacoepidemiol. Drug Saf ., 15, 241 (2006). DOI: 10.1002/pds.1211




