【テクニカルレポート】生物由来原料基準に適合した間葉系幹細胞用無血清培地
本記事は、和光純薬時報 Vol.88 No.2(2020年4月号)において、富士フイルム和光純薬 ライフサイエンス研究所 髙垣 謙太郎が執筆したものです。
間葉系幹細胞を用いた再生医療等製品
世界中で間葉系幹細胞を細胞医薬に用いるという動きが活発になっています。
2014 年に薬事法が薬機法へ変わったことにより、再生医療等製品を開発する環境が整いました。以降、テムセル、ステミラックという 2 つの間葉系幹細胞を主成分とする再生医療等製品が承認を受けました。これに続けと、間葉系幹細胞を主成分とする ADR-001、Multistem といった製品の開発も進められています。欧州では、Alofisel という製品が承認を受けましたが、開発を行った TiGenix社は武田薬品工業株式会社の子会社となり、間もなく日本国内で開発が進むと予想されます。
血清を用いた培養の問題点
細胞を医薬品にするにあたって、培養によって細胞数を増やすという工程が必要です。間葉系幹細胞の培養には、D-MEM やα-MEM といった基本培地に、10% 程度の血清を添加したものを用いることが一般的で、先述のテムセルやステミラックもそれぞれウシ血清あるいはヒト血清を用いて培養されています。
血清はさまざまな細胞の増殖を助ける万能因子ですが、いくつかの問題を抱えています。一つ目として、ドナー由来の感染症に関する懸念があります。牛海綿状脳症(BSE)が世に知られるようになって以降、生物に由来する原料の取扱いは厳しさを増しました。日本でも、生物由来原料に起因する細菌・ウイルスなどに感染する可能性を排除するため「生物由来原料基準(生原基)」が設けられました。特にウシ血清に関しては、原料として用いることのできる原産国が規定されるなど、さまざまな制限があります。
二つ目は、血清ロット間差です。血清がどのような成分で構成されているのか、血清中のどのような成分が細胞増殖に関与しているのかなどは完全に解明されておらず、細胞培養におけるブラックボックスになっています。このブラックボックスに起因する血清のロット間差は、培養工程を安定化させるうえで大きな障害になっています。実際に血清を用いて、得られた細胞が基準を満たすかどうかを判断するロットチェックには多大な労力を要しますし、仮に良い血清ロットが得られたとして、確保できる同一ロットの本数には限りがあります。今使っているロットがなくなったとき、再び良い血清に巡り合えるかどうかも悩ましい問題でしょう。
無血清培地の優位性
血清が持つ安全性と安定性に関する問題を解決するために、無血清培地を用いた培養は非常に有効な方法であると考えられます。厳密に管理された、糖質、タンパク質、アミノ酸、脂質、ビタミン、微量元素などを毎回決まった量比で混合して作製する無血清培地は、ロット間差が最小化されており、細胞の安定的な培養に寄与します。もちろん、開発初期の基礎研究においても、血清ロットの違いにより実験結果が左右されないというのは大きなメリットになります。
無血清で細胞が増殖できるのか不安に感じる方も多いと思いますが、無血清培地は細胞の増殖を促進する因子を的確に増強することができるため、血清添加した基礎培地を用いるより細胞の増殖が活発です。まとまった数の細胞が短時間で得られるため、実験スケジュールが組みやすくなるというメリットもあるでしょう。
PRIME-XV MSC Expansion XSFM を生原基に適合させるための当社の取組み
当社で取扱う PRIME-XV MSC Expansion XSFM は、同じ富士フイルムグループの FUJIFILM Irvine Scientific社が開発した、間葉系幹細胞の拡大培養に特化した無血清培地で、国内外で高い評価をいただいています。しかし、一部に生原基を満たさない原料を用いているため、国内で間葉系幹細胞を用いた再生医療等製品の開発を検討されている方々に、基礎研究以外の用途には推奨しづらい部分がありました。
私たちは、2018 年に PRIME-XV MSC Expansion XSFM の成分を見直すことにより、生原基を満たした MSC Expansion XSFM B を開発し、(独)医薬品医療機器総合機構より再生医療等製品材料適格性確認書を取得しました(薬機審長発第 0305006 号)。
MSC Expansion XSFM Bを用いた間葉系幹細胞培養
MSC Expansion XSFM B で培養した間葉系幹細胞は、一般的に用いられる 10%ウシ血清を含んだα-MEM で培養した細胞より速く増殖します(図 1)。MSC Expansion XSFM B で培養した間葉系幹細胞の表面抗原は、CD90 陽性、CD105 陽性、CD45 陰性で(図 2)、脂肪、骨、軟骨の三方向に分化していることを確認しています(図 3)。これらの形質は、継代を経ても安定しています。
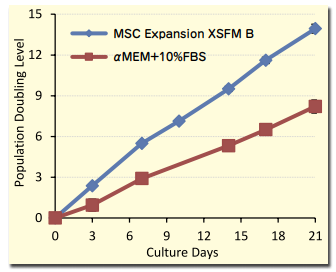
図1.MSC Expansion XSFM B で培養した細胞の増殖速度
骨髄由来の間葉系幹細胞を、MSC Expansion XSFM B あるいは 10% ウシ血清を含むα-MEM で 21 日間培養した際の増殖曲線を示す。MSC Expansion XSFM B で培養した細胞は、血清含有培地で培養した場合に比べて増殖が速い。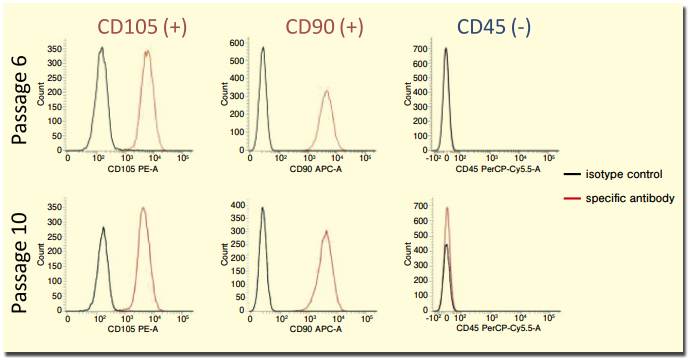
図2.MSC Expansion XSFM B で培養した細胞の表面抗原
MSC Expansion XSFM B で培養した 6 継代目及び 10 継代目の細胞を、フローサイトメトリーで解析した結果を示す。いずれの時点においても、CD105 及び CD90 が陽性、CD45 が陰性であった。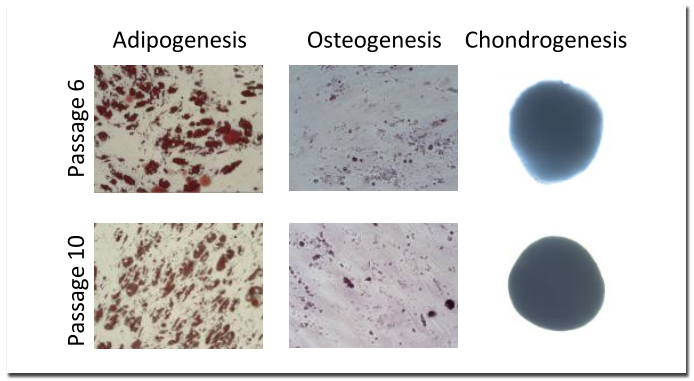
図3.MSC Expansion XSFM B で培養した細胞の分化
MSC Expansion XSFM B で培養した 6 継代目及び 10 継代目の細胞を、脂肪、骨、軟骨へ分化させた結果を示す。それぞれ、Oil Red O、Alizarin Red、Alcian Blue にて染色している。いずれの時点においても、脂肪、骨、軟骨に分化させることができた。MSC Expansion XSFM B は、間葉系幹細胞を用いた再生医療等製品の開発に、安心してご利用いただけると確信しています。また現在、生原基に対応しつつ、MSC Expansion XSFM Bよりもさらに増殖能を高めた、MSC Expansion XSFM MDF の開発も進めています。
当社は、お客様のご要望にあわせたカスタマイズにも柔軟に対応させていただきます。将来的に、FDA の監査を定期的に受けた FUJIFILM Irvine Scientific 社の GMP 準拠工場にて培地を製造することも可能です。研究から薬事開発まで、さまざまなステージでサポートさせていただきます。
当社は、FUJIFILM Irvine Scientific社製品の日本における販売に加えて培地の開発・改良も行っています。




