【テクニカルレポート】イオンペアー試薬と分離の関係
本記事は、和光純薬時報 Vol.69 No.2(2001年4月号)において、和光純薬工業 大阪研究所 上森 仁志が執筆したものです。
逆相クロマトグラフィーにおいて、イオンペアークロマト法は、分析対象となる化合物の適応範囲を中性化合物だけでなく、酸性・塩基性化合物などのイオン性化合物へも拡大した手法として評価され日常分析に広く応用されている。
塩基性化合物の分析には、酸性移動相条件下に直鎖型アルキルスルホン酸 Na 塩の添加が効果的である。この直鎖型アルキルスルホン酸 Na 塩としては、1-ペンタンスルホン酸 Na、1-ヘキサンスルホン酸 Na(SHS)、1-ヘプタンスルホン酸ナトリウム(SHpS)、1-オクタンスルホン酸 Na(SOS)等が分析目的に応じて使い分けられている。
しかし、実際に分析条件を設定する場合には、"どのタイプを選択肢、どの程度の量を添加したらよいのか、また、その時の pH はどのくらいが適切か"迷うものである。
今回、HP プロテインシークエンサーの測定条件を参考として、20 種類の PTH-アミノ酸をグラジエント分析法により約 20 分で分析することを目的として検討を行った結果より、イオンペアー試薬の種類と添加量の関係について考察した。
PTH-アミノ酸には中性アミノ酸以外に 2 種類の酸性アミノ酸(グルタミン酸、アスパラギン酸)と 3 種類の塩基性アミノ酸(ヒスチジン、アルギニン、リジン)が含まれている。中性アミノ酸の分離のバランスは、グラジエントの初期と最終の有機溶媒濃度(この場合は種類も変えてあるが)で決定され、酸性アミノ酸は pH の調整により、塩基性アミノ酸はイオンペアー試薬の添加により保持時間の調節が可能となる。
イオンペアー試薬に SHS を使った場合と SOS を使った場合の添加量と保持の関係を図 1. に示した。中性アミノ酸はイオンペアー試薬の影響を受けないが、塩基性アミノ酸は言うまでもなく酸性アミノ酸の保持にまで影響を与えている。
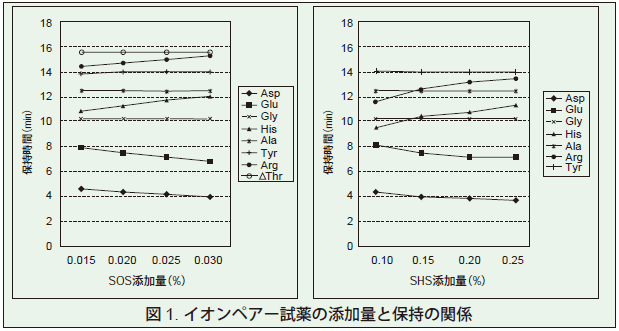
この保持変化曲線から至適添加量が推定され、この場合は、SHS で 0.20 %、SOS で 0.025 %となった。クロマトグラムを図 2. に示したが、SHS と SOS は炭素にして 2 つしか違わないにもかかわらず、その効果は約 10 倍以上となり、しかも SHS のアルギニンに対する添加効果は限界であり、SOS 0.025 %添加時と同一分離パターンを得ることはできなかった。なお、SHpS を使用した場合は、0.10 %の添加量でほぼ同一分離パターンを示した。
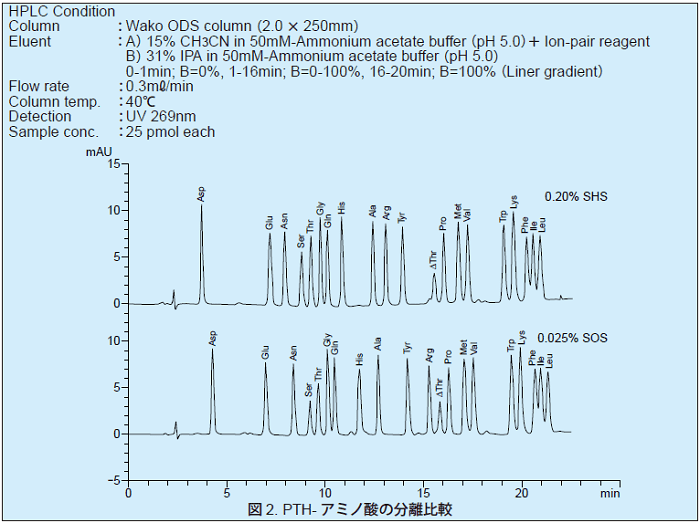
移動相の pH は、最初に溶出する酸性アミノ酸の保持調整から 5.0 に設定し、塩濃度は、10 mM から 100 mM 検討範囲において保持時間に影響を与えなかったため 50 mM に設定した。分離パターンは異なるものの SHS、SHpS、SOS とも当初の目的を達成した。しかし、SOS の場合は移動相への添加量が少ないために、初期平衡化に時間を要するという欠点を有していた。
以上、PTH-アミノ酸分析を例に、イオンペアー試薬と分離の関係について説明したが、一般的な条件決定法として、筆者らの経験から、塩濃度は 20 ~ 50 mM、pH は充てん剤が安定的にしようできる 3 ~ 5 に設定し、イオンペアー試薬の種類は SOS から、添加量は 0.05 ~ 0.1 %から検討を開始されることをお勧めする。
得られたクロマトグラムをもとに、4 点位の添加量、種類の変更検討で最適分離条件が設定可能になるものと推定する。




