【テクニカルレポート】反応性代謝物検出のための Presep® XenoScreen™ 96well Plate を用いた試料前処理について
本記事は、和光純薬時報 Vol.84 No.2(2016年4月号)において、和光純薬工業 試薬化成品研究所 須藤 勇紀が執筆したものです。
医薬品は通常、動物実験や臨床試験を経て有効性と安全性が確認された後に、当局に承認された物質のみが製造・販売されます。臨床試験、上市後に発症する副作用は全副作用の約 80 %を占めますが、それら副作用は薬理作用から予測が可能であり、通常、用量を減量することにより回避することが可能です1)。
一方で特異体質性薬物毒性(IDT : Idiosyncratic drug toxicity)と呼ばれ、動物実験や臨床試験では発見されることがほとんどなく、医薬品として上市後に多くの患者に使用されて初めて発現する重篤な副作用があります1)。 IDTの発生についてはいくつかの仮説が提唱されていますがその中でも医薬品の反応性代謝物が大きな要因のひとつであると考えられ、その評価が重要とされています2, 3)。
1.トラッピング試験について
トラッピング試験は肝ミクロソームなどの酵素源を医薬品候補化合物とトラッピング試薬共存下でインキュベーションし、生成した反応性代謝物をトラッピング試薬付加体として捕捉し、LC/MSなどにより測定する方法です4, 5)。 一般にトラッピング試薬としてグルタチオン(GSH)がよく使用されます6, 7)。しかし、グルタチオンエチルエステル体(GSHEE)の方が検出感度良く分析できるとの報告もあり8, 9)、さらにグルタチオンエチルエステル安定同位体置換体(GSHEE-d5)を併用することで選択性を向上させることができます4, 10)。
今回、トラッピング試験に必要なBuffer類やGSHEEとGSHEE-d5が1つのチューブに小分けされた迅速分析が可能なキットXenoScreen™ GSH-EE に合わせて、試料前処理用プレート Presep® XenoScreen™ 96well Plateの使用例を紹介します。
2.実験方法について
反応性代謝物の発生が既知の薬物クロザピン11)を対象にQ1 Scanモードによる分析を行いました。実験フローを図1に示します。被験薬物溶液は1 mmol/ℓ となるように調液します。前処理では96well plate用の吸引マニホールドを用いて減圧下で処理しました。LC/MS条件を表1に示します。

図1.実験フロー
表1. LC/MS条件
-
機器 Prominence LC-20A (島津製作所) カラム Wakopak® Ultra C18-3 φ2.0 mm x 50 mm 移動相A 0.05 % ぎ酸水溶液 移動相B 0.05 % ぎ酸 - アセトニトリル溶液 グラジエント条件 0 min. (A : B = 98 : 2)→10 min. (10 : 90)→15 min. (10 : 90)→15.01 min. (98 : 2)→20 min. (98 : 2) 流量 0.2 mL/min. カラム温度 40 ℃ 注入量 5 µL -
機器 3200 QTRAP (SCIEX社) イオン化 ESI positive 測定モード Q1 Scan Curtain gas 20 Ion Spray Voltage 5500 Temperature 300 Ion Source gas 1 70 Ion Source gas 2 60
3.結果
TICクロマトグラムの比較を図2に示します。保持時間 5.2 分付近にブランク溶液と被験薬物溶液とのピークに違いがあることが分かります。
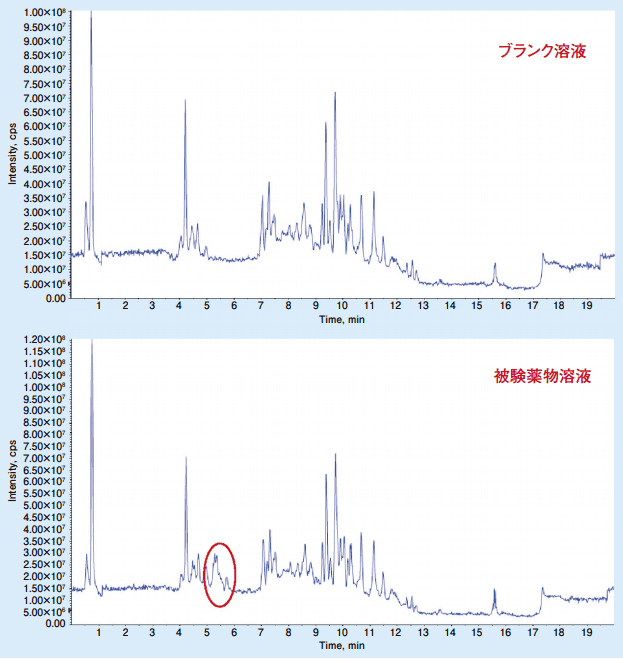
図2.TICクロマトグラムの比較
保持時間 5.2 分のMSスペクトルを図3に示します。クロザピンの代謝物 + GSHEE 及び GSHEE-d5の付加体は H 体が m/z : 660、D 体が m/z : 665 で検出されるとの報告11)がありますのでこの結果は一致します。
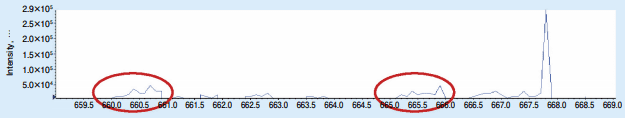
図3.保持時間5.2分のMSスペクトル
このようにPresep® XenoScreen™ 96well Plate を利用して反応性代謝物を検出することができます。
次に参考データとして反応性代謝物11)が既知であるアセトアミノフェン、オメプラゾール、ジクロフェナク、チクロピジンをSIMモードで分析しました。薬物4種類のSIMクロマトグラムを図4に示します。 クロザピンと同様に m/z 差 5 の反応性代謝物 + GSHEE 及び GSHEE-d5 の付加体ピークを確認することができました。
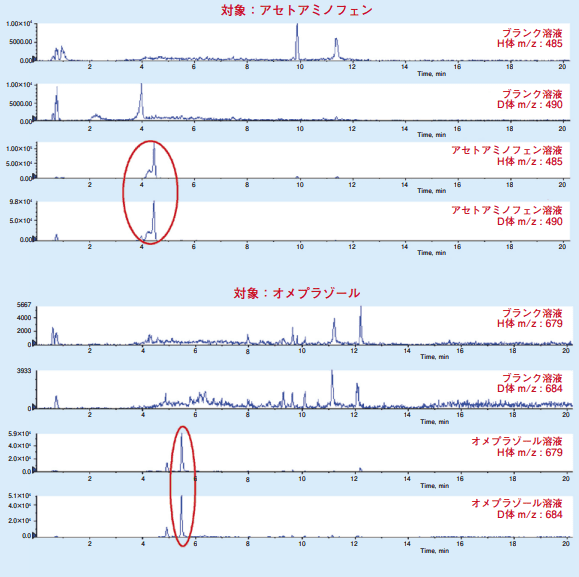
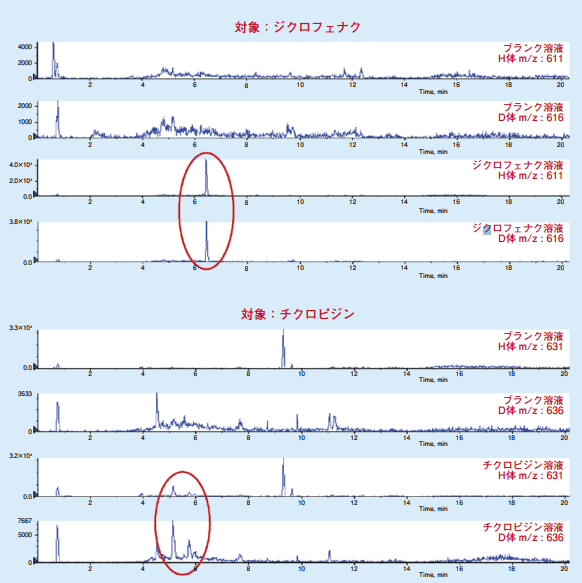
図4.薬物4種類のSIMクロマトグラム
今回の検討結果が反応性代謝物の分析に貢献できれば幸いです。
参考文献
- 山田久陽 他:日本薬理学雑誌、127(6), 473 (2006).
- 大江知之:日本薬理学雑誌, 134(6), 338 (2009).
- Naito, S et al. : J. Toxicol. Sci., 32(4), 329 (2007).
- 山岡俊和:和光純薬時報, 84(1), 5 (2016).
- Ramirez-Molina, C. et al. : Rapid Commun. Mass Spectrom., 23(22), 3501 (2009).
- Yan, Z. et al. : Anal. Chem., 76(23), 6835 (2004).
- Mutlib, A. et al. : Rapid Commun. Mass Spectrom., 19(23), 3482 (2005).
- Soglia, J. R. et al. : J. Pharm. Biomed. Anal., 36(1), 105 (2004).
- Wen, B. et al. : J. Mass Spectrom., 44(1), 90 (2009).
- Yamaoka, T. et al. : J. Pharmacol. Toxicol. Methods, 76, 83 (2015).
- 山岡俊知:特願 2011-113846, 国際公開番号 WO2012/160798.




