【連載】幹細胞由来EV~治療、診断、化粧品への展開~「第3回 細胞外小胞を利用した治療の実現をサポートする富士フイルム和光純薬の取り組み」
本記事は、和光純薬時報 Vol.91 No.1(2023年1月号)において、弊社 生産プロセス開発部 西部 隆宏に執筆いただいたものです。
はじめに
細胞外小胞 (Extracellular vesicle/EV) は、エクソソームやマイクロベシクルといった細胞から分泌される脂質二重膜の小胞体の総称である1)。近年、間葉系幹細胞(Mesenchymal stem cell : MSC)など一部の細胞に由来するEVが治療に有用である可能性が示されてきており2)、それに伴い、EVを利用した治療用製剤、EV製剤の利用に関連した技術開発も活発化している。
本稿では富士フイルム和光純薬が有するEVの産生、精製、保存、品質管理の一連の生産工程に係る技術や製品について紹介する。
MSC由来EVの産生に最適化した培地
近年、種々の細胞に由来するEVの治療応用が試みられているが、その中でも特にMSCに由来するEVの研究開発が注目されており、実際に2022年時点ではEVを用いた臨床試験の6割以上がMSC由来EVを利用したものである3)。一方、MSC由来EVを得るために使用される培養液は古典的な基礎培地がほとんどであり、いまだに最適化された培養液の条件は定められていない。
MSC由来EVの製造においては、MSCをウシ胎児血清 (FBS) を含む基礎培地といった血清培地で増殖させた後、FBSを含まない無血清培地やEVを除去したFBSを含む血清培地に置き換えてEVを培養上清中に産生させる、2段階の工程が使用されている場合が多い。当社では、これらそれぞれの工程に最適化した培地を開発した。
MSCの増殖においては、MSCを高品質の状態で効率的に増殖させる培地として、MSCulture™培地を開発した (コードNo. 133-19331, 132-19345)。本培地はFBSを添加して使用する基礎培地であるが、αMEMなど従来の基礎培地に比べると細胞増殖の効率が非常に高く、また増殖したMSCが産生するEVの生物活性も向上することを確認している (図1)。
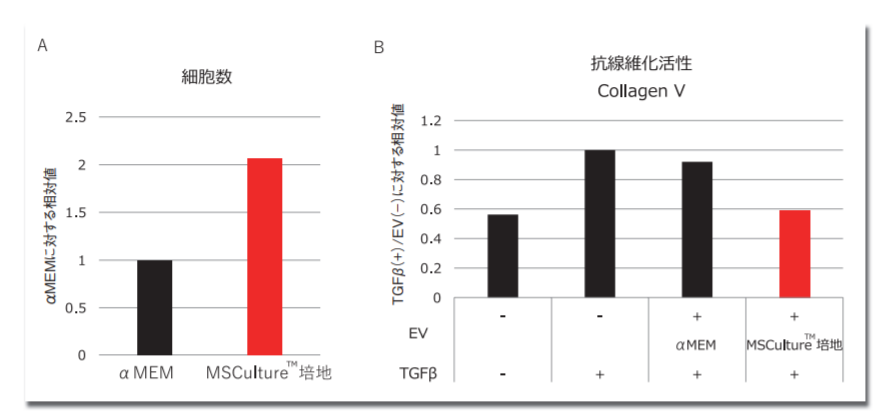
A) αMEM及びMSCulture™培地でMSCを増殖させた際の細胞数の比較
αMEM及びMSCulture™培地はそれぞれ15% FBSを添加して使用している。
B) 各培地で増殖させたMSCからEV-Up™培地を用いて得たEVの抗線維化活性を比較した結果。
また当社では、MSC増殖後のEV産生ステップでの使用に最適化したEV産生専用無血清培地、EV-Up™培地を開発した (コードNo. 053-09451, 298-84001)。本培地はEVの産生量を向上させるだけではなく、生物活性も大幅に向上することを抗線維化活性により確認している4) (図2)。
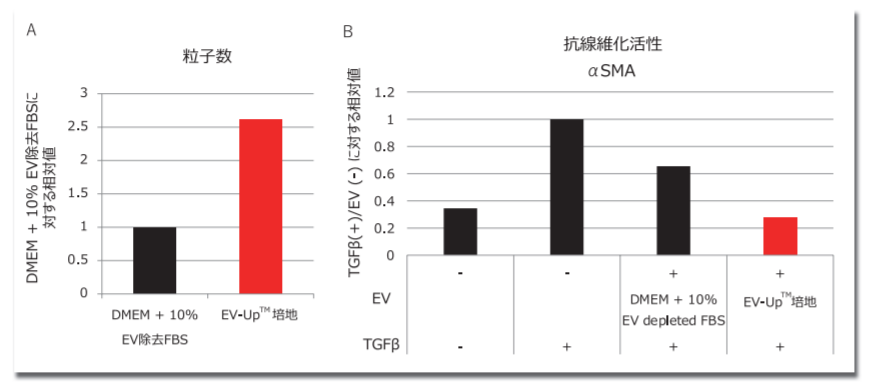
A) MSCを血清培地で拡大した後にEV除去FBSを含むDMEMあるいはEV-Up™培地に置換して得た培養上清から取得されたエクソソームの粒子数をナノ粒子トラッキング解析により測定した結果
B) Aの各条件で得たEVの生物活性を抗線維化活性評価で比較した結果
MSCulture™培地とEV-Up™培地を組み合わせた培養により高品質のMSC由来EVを効率的に取得することが可能になる。MSC由来EVの治療応用を目的とした研究を実施する際には是非ともこれらの培地を検討していただきたい。
独自のEV精製技術、PSアフィニティー法を利用したEV精製技術
EV産生後の培養上清からEVを精製する工程に利用できる技術として、当社は現金沢大学医学部華山教授との共同研究により、独自のEV精製方法、PSアフィニティー法を開発し5)、本技術を利用した研究用のEV精製試薬、MagCapture™ Exosome Isolation Kit PS Ver. 2(コードNo. 290-84103)を上市している。PSアフィニティー法はホスファチジルセリン(Phosphatidylserine : PS) に特異的に結合するTim4タンパク質を利用したEVのアフィニティー精製手法であり、MSC由来EVにおいては培養上清からの回収率が約80%という優れた精製手法である。PSアフィニティー法により精製したEVが優れた生物活性を有していることもin vitroでの抗線維化活性評価、抗炎症活性評価により確認している6) (図3)。
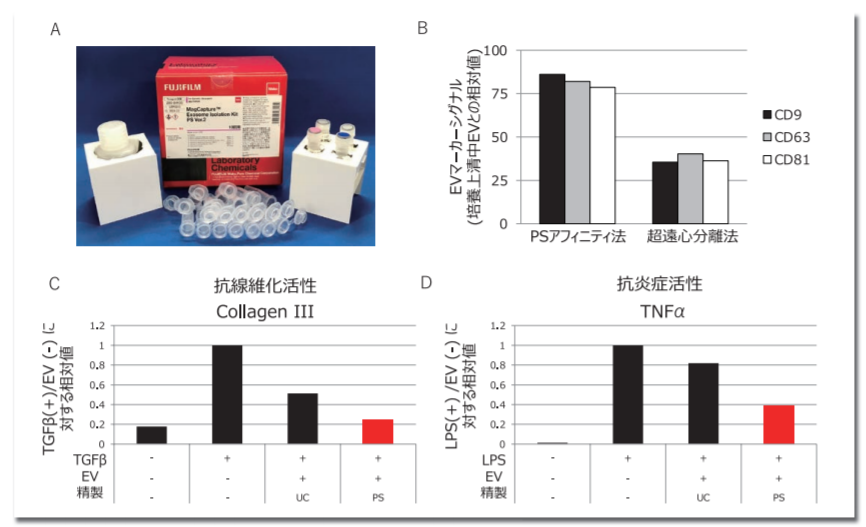
A) PSアフィニティー法を利用したEV精製の研究用試薬、MagCapture™ Exosome Isolation Kit PS Ver. 2。
B) PSアフィニティー法、超遠心分離法それぞれの手法で精製したMSC由来EVの回収率をELISAで定量した結果。検出には抗CD9抗体、抗CD63抗体、抗CD81抗体を使用。グラフは培養上清中のEVマーカー量との相対値。ELISAはPS Capture™ Exosome ELISA Kit (Streptavidin HRP) [コードNo. 298-80601]を使用した。
C) 線維芽細胞へのTGFβ刺激で誘導した線維化関連遺伝子発現の上昇をMSC由来EVが抑制する効果を定量PCRにより解析した結果。
D) PBMC由来単球へのLPS刺激で誘導した炎症関連遺伝子発現の上昇をMSC由来EVが抑制する効果を定量PCRにより解析した結果。
UC:超遠心分離法、PS:PSアフィニティー法
現在我々は、このPSアフィニティー法をEV製剤の製造に利用できるよう、Tim4タンパク質を固定化したアフィニティーカラムを用いた大量精製技術を開発中であり、リッタースケールの培養上清からのEVのアフィニティーカラム精製が現実味を帯びてきた段階である。
精製したEVの保存安定性を向上させる技術
精製したEVは保存チューブなどの器材に著しく吸着するため、取り扱う際にはEVの非特異的な吸着を抑制できる成分を添加することが好ましい。以前より我々はこのEVの非特異的な吸着を問題視しており、EVを取り扱う際の吸着抑制試薬、EV-Save™細胞外小胞ブロッキング試薬 (コードNo. 058-09261) の使用を推奨している。このEV-Save™細胞外小胞ブロッキング試薬は、EVの吸着抑制のみならず、凍結保存時の安定性を向上させることも確認している(図4)。
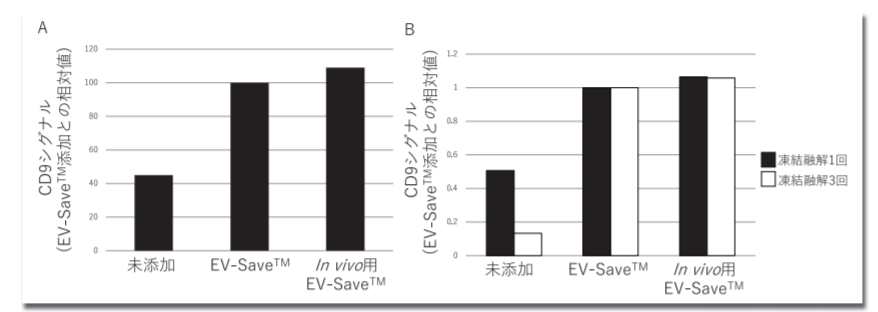
A) PSアフィニティー法で精製したCOLO201細胞由来EVにEV-Save™及びin vivo用EV-Save™を添加して16時間冷蔵保管した後、サンプルチューブ内のEVマーカー量をPS Capture™ Exosome ELISA Kit (Streptavidin HRP)により測定した結果。
B) EV-Save™及びin vivo用EV-Save™を添加したCOLO201細胞由来EVを1回もしくは3回凍結融解し、その後サンプルチューブ内のEVマーカー量をPS Capture™ Exosome ELISA Kit (Streptavidin HRP) により測定した結果。
そして当社はEV製剤の製造においてもEVの吸着抑制や凍結保存時の安定性の向上が重要になると考え、医薬品添加剤として既に使用実績がある成分のみで構成したEV保存液も開発した (in vivo用 EV-Save™細胞外小胞ブロッキング試薬,コードNo. 050-09461 ; 図4)。現状では本製品はin vivo実験用の研究用試薬として販売している状況であるが、医療分野での利用を想定した成分を用いていることからEV製剤の研究開発の際には是非とも利用していただきたい。
EVの製造工程管理や品質管理に利用できるELISA技術
EVの治療応用においてはEVの製造技術のみならず品質管理技術の確立も重要であり、その中でもEVマーカーを定性的、定量的に解析する技術はEVの質や量を評価する上で非常に重要である。当社ではEVマーカーの定性・定量解析が可能なELISA製品を開発し、キットを上市している。CD9、CD63、CD81といったEVマーカーに対する抗体を用いたサンドイッチELISAのCD-Captureシリーズキットや、Tim4タンパク質を固相化したプレートでEVを捕捉し、任意のEVマーカーに対する抗体で検出するPS Capture ELISAなど目的に合わせたパターンでの検出が可能であり、当社の技術開発においても有用なツールとなっている (図3B、図4の実験で使用)。これらのキットをEV製造工程でのモニタリングや精製EVの品質管理などに是非活用していただきたい。
最後に
MSC由来EVを中心にEVの治療応用への期待が高まる中、EVの製造技術や評価技術の最適化や標準化が大きな課題となっている。当社はこれまでにEV生産の一連工程に関連する技術を研究用試薬として上市しているが、今後は実際のEV製剤の製造や品質管理を担う部材への適応を進め、EV治療という全く新たな医療の実現に貢献していきたいと考えている。
参考文献
- Colombo, M. et al . : Annu. Rev. Cell Dev. Biol., 30, 255 (2014).
- Phinney, D. G. and Pittenger, M. F. : Stem Cells, 35 (4), 851 (2017).
- Rezaie, J. et al. : Cell Commun. Signal., 20(1), 145 (2022).
- 丸谷祐樹、山根昌之 : 和光純薬時報, 89 (4), 8 (2021).
- Nakai, W. et al . : Sci. Rep., 6, 33935 (2016).
- 山根昌之、石止貴将 : 和光純薬時報, 88 (4), 10 (2020).




