抗体薬物複合体 (ADC) 研究試薬
抗体薬物複合体 (ADC) は標的分子に対する抗体に抗がん剤などの薬物 (ペイロード) を結合させたバイオ医薬品です。従来の抗がん剤と比較して標的への特異性が高く、副作用の低減が期待できることから注目されているモダリティです。 ADCの研究開発においては、標的へ特異的に結合する抗体の取得と有効なペイロードおよび結合に用いるリンカーの選定が重要です。当社では、ADCの研究開発において抗体の産生や精製に必要な試薬や各種ペイロードおよびリンカーをラインアップしています。DNA免疫法を用いた抗体の作製受託サービスやADC合成・評価サービスなどADCの研究開発をサポートする受託サービスも展開しています。
製品ラインアップ
学術コンテンツ
抗体薬物複合体 (ADC) とは?
抗体薬物複合体 (ADC: Antibody-Drug Conjugate) は標的分子に対する抗体に抗がん剤などの薬物 (ペイロード) を結合させたバイオ医薬品です。従来の抗がん剤と比較して標的への特異性が高いことから、高い治療効果と副作用の低減が期待でき、注目されているモダリティの一つです。これまでに卵巣がん1)や乳がん2)、急性骨髄性白血病3)をはじめとした様々ながんに対するADCが開発されています。

ADCの構成要素
(1) 抗体
特定の抗原に対して特異的に結合する抗体を使用することで、その抗原が発現している標的細胞に薬物を作用させることができます。抗原は標的細胞に選択的に発現しているものを選択します。一般的には免疫原性を回避するためキメラ化やヒト化などの改変が加えられたモノクローナル抗体が使用されており、完全ヒト抗体の開発も進んでいます。また近年では、抗体の親和性や安定性を向上させるために抗体の修飾や変異導入が行われており、より高性能な抗体を作製するための技術開発が行われています。
ADCの開発では抗原に高い特異性を有する抗体の取得が必要ですが、標的となるタンパク質の多くは細胞膜表面上に発現する膜タンパク質であり、その複雑な立体構造から抗体の取得が難しいと言われています。当社のDNA免疫法はこのような膜タンパク質に対する抗体の取得において有用な技術です。
DNA免疫法
DNA免疫法は⽬的タンパク質の遺伝⼦を組み込んだ発現ベクターを動物に導入し、動物の体内で目的タンパク質を発現させることで抗体を作製する技術です。従来のタンパク質やペプチドを用いた免疫法と比較して、(1) 抗原タンパク質・ペプチドの調製が不要、(2) 抗原のコンタミネーションのリスクがない、(3) 抗原が変性しない、(4) ターゲット抗原の改変が容易といった利点があります。
抗原を動物体内で発現させるため、抗原のネイティブフォームを認識する抗体が取得しやすいのも大きな特長です。複数回膜貫通型の膜タンパク質に対しても抗体取得の成功率は77.3% (51/66件、マウス・ラット、~2024年3月末までの実績) と高く、さらに中和活性を有する抗体も得ることができます。
当社ではDNA免疫法を用いたモノクローナル抗体作製の受託サービスを提供しています。
(2) ペイロード
抗体が認識した標的に対して細胞傷害活性を有する化合物 (薬物)です。DNAに直接結合し複製を阻害するものや、DNAの構造変化に必要なトポイソメラーゼの活性を阻害するもの、微小管 (チューブリン) の重合を阻害するものなどがあり、これらの作用で標的細胞にダメージを与えたり、アポトーシスを誘導したりします。なおADCの特性上、ペイロードにもリンカーが結合できる部位が必要となります。
(3) リンカー
抗体とペイロードをつなぐ役割を担います。ADCに使用されるリンカーは切断可能なものとそうでないものに大別されますが、ほとんどのADCでは切断可能なリンカーが採用されています。リンカーの切断様式は酵素による切断をはじめ、酸性環境による切断や還元による切断などがあります。リンカーの選択は、体内での安定性やペイロードの放出に影響を与えます。
ADCの作用機序
ADCが標的抗原 (多くは細胞膜上の標的タンパク質) に結合すると、エンドサイトーシスによって細胞内に取り込まれます。取り込まれたADCは初期エンドソームから後期エンドソームに移行し、最終的にエンドソームとリソソームが融合します。切断式のリンカーを使用している場合、リソソーム内でADCのリンカーが切断され、ペイロードが放出されます。ペイロードは標的分子 (DNAやトポイソメラーゼ、チューブリンなど) に結合し、アポトーシスの誘導などを引き起こし、細胞傷害作用を発揮します4-5)。このような直接的な細胞傷害作用に加えて、ペイロードの一部は標的細胞の外に拡散し、近隣の細胞も傷害します (バイスタンダー効果)。これにより標的細胞の周辺に存在する細胞も攻撃することができます6-7)。
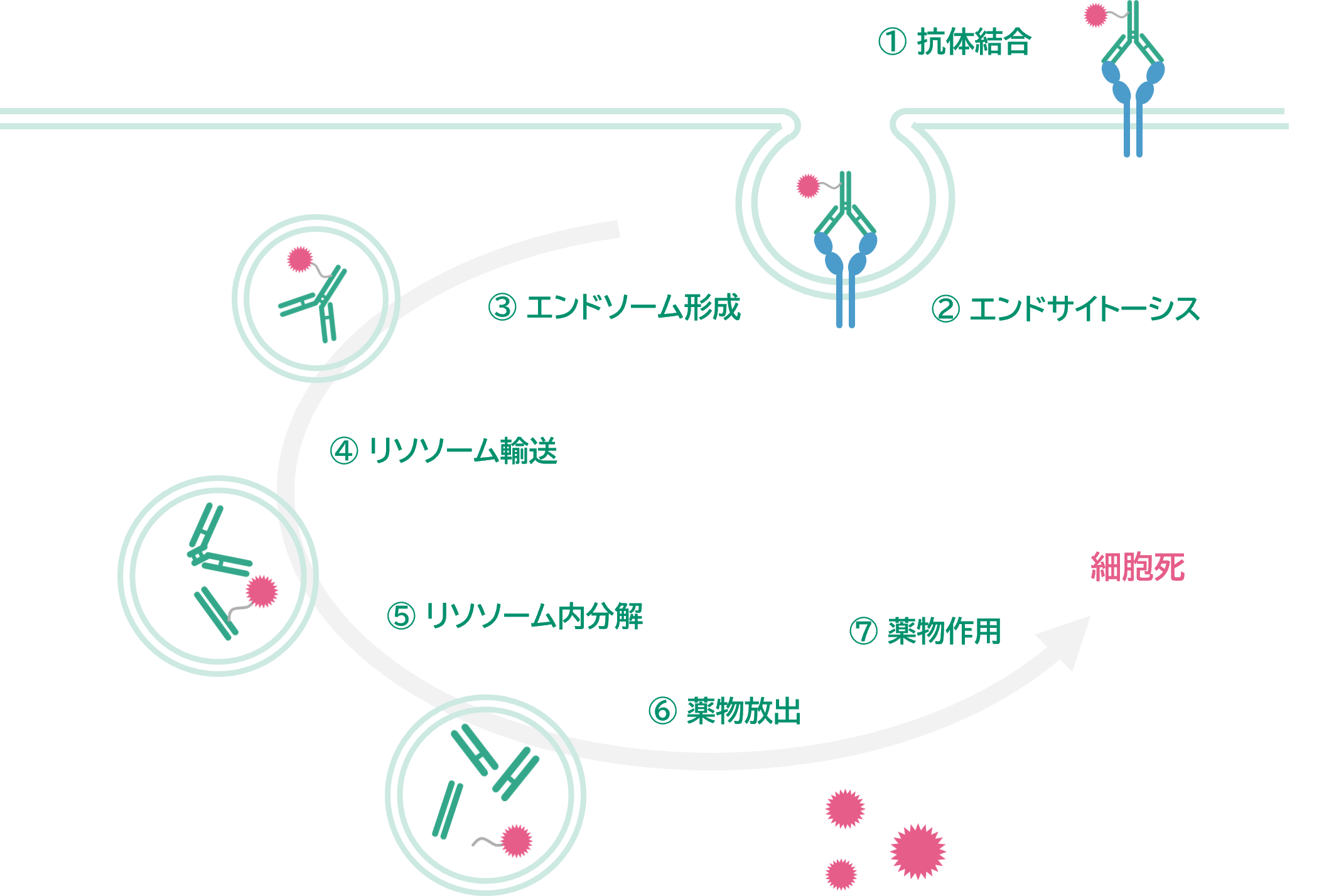
図1 ADCの作用機序
文献8)を元に作成
ADC開発の流れ (例)
1
抗体作製・修飾
ADC作製の第一歩はモノクローナル抗体の作製です。標的抗原 (主に膜タンパク質) に特異的なモノクローナル抗体を取得するのはもちろん、目的に応じてキメラ化やヒト化などを行います。また生体内での安定性を高めたり、抗原への結合能を維持したままペイロードを結合させるための修飾を行う場合もあります。
| 当社提供の製品・サービス | 概要 |
|---|---|
| ウサギモノクローナル抗体作製受託 (DNA免疫) | DNA免疫法により、従来法では難しかった膜タンパク質などの抗体も高い確率で作製可能。中和活性を持つ抗体も取得可能。 |
| マウス・ラットモノクローナル抗体作製受託 (DNA免疫) | |
| 培地/平衡塩類 (バイオ医薬) | 抗体の産生に使用される培地および平衡塩をラインアップ。 |
| 抗体標識/改変試薬 | 抗体の糖鎖を改変したり、ペプチドを付加する試薬をラインアップ。 |
| AIによる抗体の高機能化受託 | レボルカ社が開発した人工知能による予測を組み込んだ最新のタンパク質工学技術、aiProtein® を利用し、抗原結合性への影響を最小限に、抗体の発現量・安定性などの複数の特性値をバランスよく同時に向上。 |
| ヒトキメラ化/ヒト化抗体受託 | マウス、ラット、ウサギ、その他各種動物の抗体について、抗体遺伝子のキメラ化、ヒト化を実施。 |
2
ペイロード・リンカーの選定
ペイロードは標的となる細胞 (がん細胞) への有効性やオフターゲット効果の程度を考慮して選択します。これまでに微小管重合阻害剤やトポイソメラーゼ阻害剤などが使用されています9-10)。 リンカーもADCの安全性や有効性に影響する重要な要素と考えられています。切断可能なものとそうでないもののいずれかを選択しますが、ADCの多くは切断可能なものです。
| 当社提供の製品・サービス | 概要 |
|---|---|
| ペイロード/リンカー | ADCの研究開発に有用なMedChemExpress社のペイロードやリンカーをラインアップ。 |
3
抗体-ペイロードの結合
抗体とペイロードをリンカーを介して結合させます。この段階で、結合部位の選択と薬物抗体比 (DAR: Drug-to-Antibody Ratio) の最適化が必要です。また目的の部位だけに結合させることはADCの均一性と安定性を高めるために重要です11)。
| 当社提供の製品・サービス | 概要 |
|---|---|
| ADC作製試薬 | 酵素切断型リンカーとペイロード (MMAE/PNU) をIgGに付加できるキット。 |
| ADC合成受託 | お客様よりご提供いただいた抗体、リンカー-ペイロード※を使用してADCを合成するサービス。当社取り扱いの70種類以上のリンカー/ペイロードも利用可能。 ※本サービスではリンカーとペイロードの結合は承っておりません。MedChemExpress社のリンカー-ペイロード (外部サイトへ移動) などをご利用ください。 |
4
ADCの精製
精製により未反応のペイロードやリンカー、未結合の抗体、さらには副生成物や凝集体などの不純物を除去します。精製工程はADCの純度と均一性を確保するために不可欠です。主な精製方法としては、タンジェンシャルフローろ過 (TFF) を用いた限外ろ過/透析ろ過 (UF/DF)に加え、サイズ排除クロマトグラフィー (SEC)、疎水性相互作用クロマトグラフィー (HIC)、イオン交換クロマトグラフィー (IEC)、ヒドロキシアパタイトクロマトグラフィー、膜クロマトグラフィーなどのクロマトグラフィーによる精製法が用いられ12)、それぞれ分子量や親和性、電荷の違いを利用して目的物の分離が行われます。
| 当社提供の製品・サービス | 概要 |
|---|---|
| 抗体精製試薬 | 抗体精製のクロマトグラフィーに必要な充填剤やカラムをラインアップ。 |
5
ADCの特性評価
取得したADCの性能 (有効性や安全性) を評価し、医薬品候補として有用かを判定します。考慮すべき項目は血中安定性や取込み効率、標的細胞に対する活性、薬物動態、交差反応性、毒性など多岐に渡ります。また品質評価においては、薬物抗体比 (DAR) や遊離薬物関連不純物 (FDRI) 含有量、純度などが重要な評価項目です13)。
<品質評価項目の例>
- DAR:
- 抗体に結合する薬剤の平均数を示し、ADCの有効性と密接に関連しています。薬剤結合が不十分な場合は抗腫瘍効果が低下しますが、 一方でDARが高すぎると安全性や安定性、さらには薬物動態にリスクが生じる可能性があります14-16)。
- FDRI:
- 未結合の遊離薬物および関連不純物を指し、これらが製品中に残留すると標的への選択性を欠き、副作用リスクが高まります。遊離薬物 は強い細胞毒性を有するため、製造プロセスのモニタリングから製品放出試験、安定性試験に至るまで、製品のライフサイクル全体でFDRI 含有量を厳格に管理することが必要です13)。
| 当社提供の製品・サービス | 概要 |
|---|---|
| 抗体分析試薬 | 抗体分析に使用される酵素などをラインアップ。 |
| ADC評価受託 | ADCの有効性 (抗がん活性、がん細胞内のペイロード定量) や血中安定性、交差反応性、薬物抗体比 (DAR) などの特性評価を実施します。標準的な試験から、ICH-Q6B ガイドラインの試験方法に基づいた抗体・ADCの特性解析まで、ご要望に応じてカスタム可能です。ADC合成受託と合わせてご依頼することも可能です。 |
参考文献
- Moore, K.N. et al.: N. Engl. J. Med., 389(23), 2162(2013).
Mirvetuximab soravtansine in FRα-positive, platinum-resistant ovarian cancer - Amiri-Kordestani, L. et al.: Clin. Cancer Res., 20,4436(2014).
FDA approval: ado-trastuzumab emtansine for the treatment of patients with HER2-positive metastatic breast cancer - Sievers E.L. et al.: J. Clin. Oncol., 19(13), 3244(2001).
Efficacy and safety of gemtuzumab ozogamicin in patients with CD33-positive acute myeloid leukemia in first relapse - Birrer, M.J. et al.: J. Natl. Cancer Inst., 111(6),538(2019).
Antibody-Drug Conjugate-Based Therapeutics: State of the Science - Phuna, Z.X. et al.: Life Sci., 347,122676(2024).
Antibody-drug conjugates: Principles and opportunities - Giugliano, F. et al.: Curr. Oncol. Rep., 24(7),809(2022).
Bystander effect of antibody-drug conjugates: fact or fiction? - Li, F. et al.: Cancer Res., 76(9),2710(2016).
Intracellular Released Payload Influences Potency and Bystander-Killing Effects of Antibody-Drug Conjugates in Preclinical Models - Biteghe, F. et al.: Oncotarget, 11(38), 3531(2020).
Advances in epidermal growth factor receptor specific immunotherapy: lessons to be learned from armed antibodies - Dumontet, C. et al.: Nat. Rev. Drug Discov., 22(8),641(2023).
Antibody-drug conjugates come of age in oncology - Colombo, R. et al.: Cancer Discov., 14, 2089(2024).
The Journey of Antibody-Drug Conjugates: Lessons Learned from 40 Years of Development - Dong, W. et al.: ChemMedChem., 19(17), e202400109(2024).
The Evolution of Antibody-Drug Conjugates: Toward Accurate DAR and Multi-specificity - Matsuda, Y. et al.: J. Sep. Sci., 45(1),27(2022).
Current approaches for the purification of antibody-drug conjugates - Song, W. et al.: Anal. Chem., 97(18),9748(2025).
Simultaneous Analysis of the Drug-to-Antibody Ratio, Free-Drug-Related Impurities, and Purity of Antibody-Drug Conjugates Based on Size Exclusion Chromatography - Xu, K. et al.: Bioanalysis, 5(9), 1057(2013).
Characterization of the drug-to-antibody ratio distribution for antibody-drug conjugates in plasma/serum - Sun, X. et al.: Bioconjugate Chem., 28(5), 1371(2017).
Effects of Drug-Antibody Ratio on Pharmacokinetics, Biodistribution, Efficacy, and Tolerability of Antibody-Maytansinoid Conjugates - Guo, J. et al.: Bioconjugate Chem., 27(3), 604(2016).
Characterization and Higher-Order Structure Assessment of an Interchain Cysteine-Based ADC: Impact of Drug Loading and Distribution on the Mechanism of Aggregation



