MagCapture (TM) Exosome Isolation Kit PS Ver.2
MagCapture (TM) Exosome Isolation Kit PS Ver.2
- 遺伝子研究用
-
for Genetic Research
- 製造元 :
- 富士フイルム和光純薬(株)
- 保存条件 :
- 冷蔵 (氷冷輸送)
- 適用法令 :
- 優先評価物質
- GHS :
-
- 構造式
- ラベル
- 荷姿
ドキュメント
キットコンポーネント
2回用
| Biotin Capture Magnetic Beads | 120 μL |
|---|---|
| Biotin-labeled Exosome Capture | 20 μL |
| Exosome Immobilizing/Washing Buffer (10x) | 5 mL |
| Exosome Binding Enhancer (500x) | 300 μL |
| Exosome Elution Buffer (10x) | 300 μL |
| Reaction Tubes | 4本 |
10回用
| Biotin Capture Magnetic Beads | 600 μL |
|---|---|
| Biotin-labeled Exosome Capture | 100 μL |
| Exosome Immobilizing/Washing Buffer (10x) | 25 mL |
| Exosome Binding Enhancer (500x) | 1,500 μL |
| Exosome Elution Buffer (10x) | 1,500 μL |
| Reaction Tubes | 22本 |
製品概要

MagCapture™ Exosome Isolation Kit PS Ver.2は細胞培養上清、血清、血漿などのサンプルからエクソソームをはじめとする細胞外小胞 (EV) を高純度かつ簡便に単離・精製できるキットです。EVの膜表面に存在するホスファチジルセリン (PS) とカルシウム依存的に結合するTim4タンパク質を応用することで、キレート剤によるインタクトなEVの単離・精製を実現しました。
特長
- 新規アフィニティー法 (PSアフィニティー法) によりEVを単離・精製
- 従来の超遠心分離法よりも高純度なEVを高い収量で回収
- ダメージの少ないインタクトなEVが取得でき、さまざまなアプリケーションに利用可能
- 磁気ビーズによる簡便操作で、多検体処理と高い実験再現性を実現
サンプル
- 細胞培養上清
- 血清
- 血漿 (ヘパリン、EDTA、くえん酸)
- 尿
- 唾液 など
※ 脳脊髄液などからEVを単離した報告もあります。
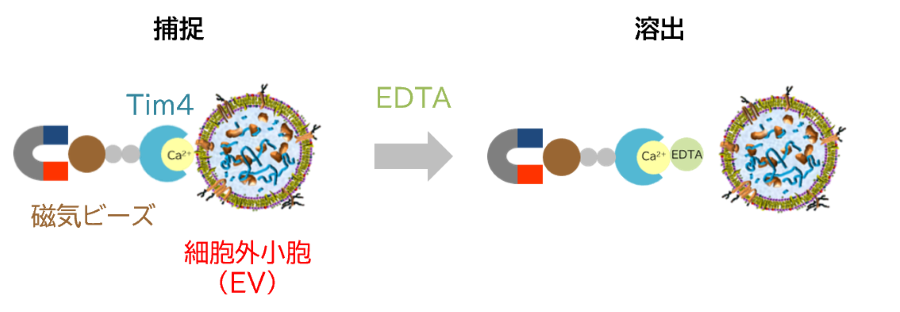
原理
PSアフィニティー法は、金沢大学 ナノ生命科学研究所の華山教授と共同で開発したEVの表面に存在するホスファチジルセリン (PS) と特異的に結合するTim4タンパク質を利用した独自のEV単離手法です1)。PS-Tim4結合の高い特異性とキレート剤によるマイルドな溶出で高純度なEVをインタクトな状態で単離できます。
ライセンスについて
本製品は研究用途でご使用ください。営利・商業目的にご使用される場合には、当社 () までお問い合わせください。
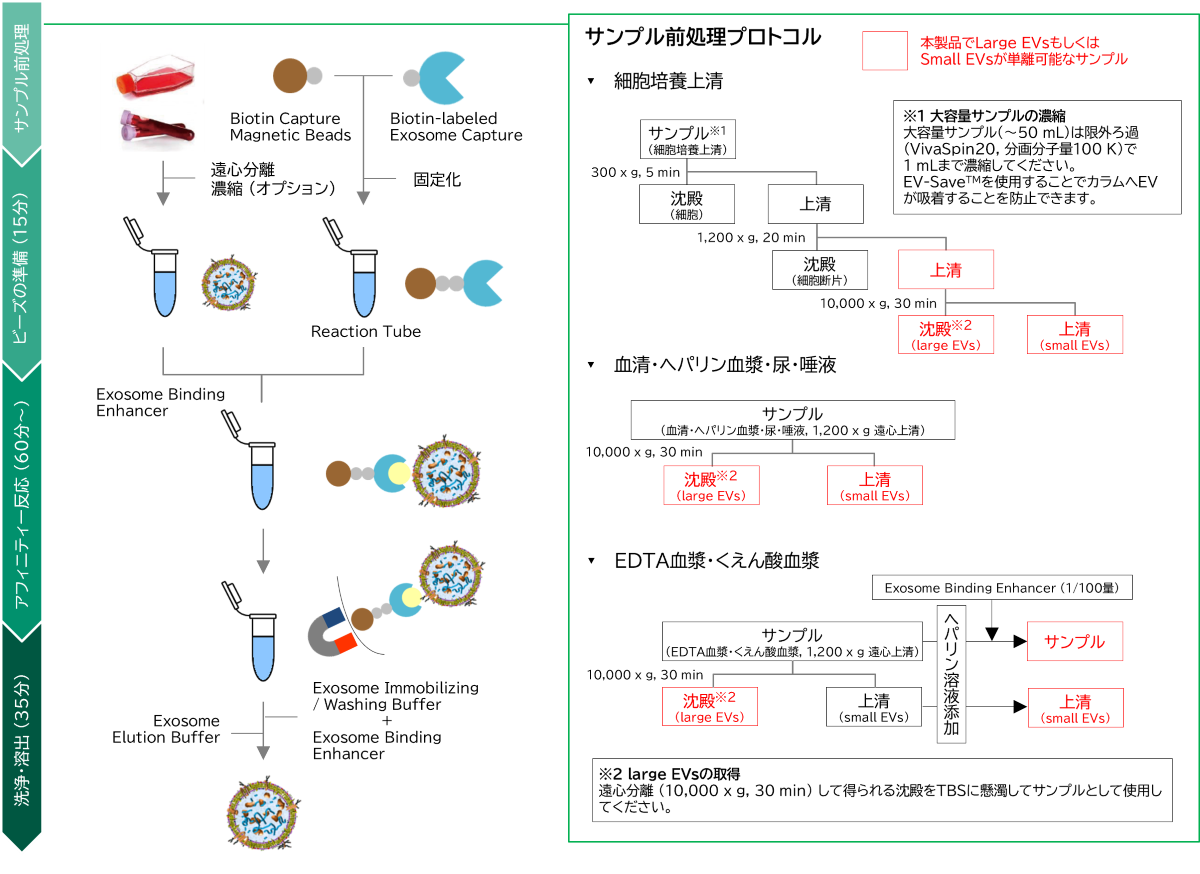
プロトコル
以下はプロトコルの概要です。詳細なプロトコルは本ページの「添付文書」をご覧ください。
エクソソームの単離/抽出/精製キット:
MagCapture™ Exosome Isolation Kit PS Ver.2
(Youtube, 7:48)
データ
従来手法との比較
プロテオミクス解析によるヒト血漿由来EVのタンパク質同定数およびEV Enrichment Scoreの比較
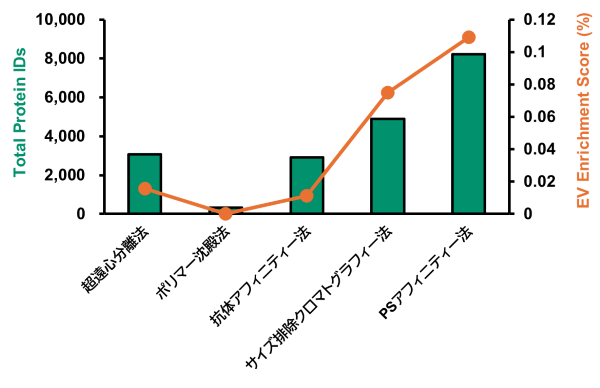
ヒト血漿200 μLから各手法でEVを単離し、LC/MS Orbitrap Fusion Lumos with FAIMS Pro (DIA、120分) を用いてプロテオミクス解析を行った。EVの純度は同定した全タンパク質の総量における、EVマーカータンパク質の総量の割合 (EES: EV Enrichment Score、以下式参照) で比較した。

[結果]
本製品は、他の手法と比較してタンパク質の同定数が多かった。
またEESも高く、高純度なEVが単離できていることが示唆された。
サイズ排除クロマトグラフィーとの回収率比較
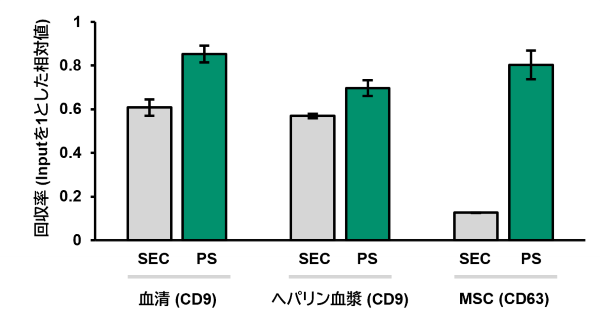
骨髄由来MSC (BMMSC) の細胞培養上清およびヒト血清、ヘパリン血漿から本製品 (PS) もしくはサイズ排除クロマトグラフィー (SEC) でEVを単離・精製した。EVの回収量はCD9-もしくはCD63-Capture ヒトエクソソームELISAキット(ストレプトアビジンHRP)で測定した。
[結果]
本製品はSECよりも高いEV回収率を示した。
超遠心分離法で単離したEVとの抗炎症活性比較新潟大学大学院 医歯薬総合研究科 消化器内科学分野 寺井先生、土屋先生との共同研究 (所属はデータ提供当時)
IFN-γで刺激した脂肪由来MSC (ADMSC) を、サプリメントを添加したEV産生培地 EV-Up™ MSC EV産生用基礎培地, AF (コードNo. 053-09451) で培養した。その後、細胞培養上清から本製品もしくは超遠心分離法でEVを単離・精製した。単離したEVをマウス由来初代培養単球に添加し、炎症マーカーであるTNF-α (M1マーカー) と抗炎症マーカーであるCD206 (M2マーカー) の発現量をリアルタイムPCRで測定した。
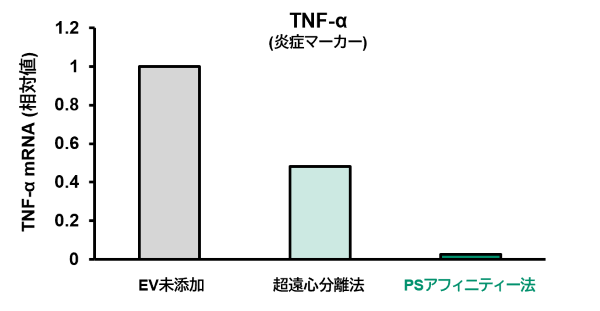
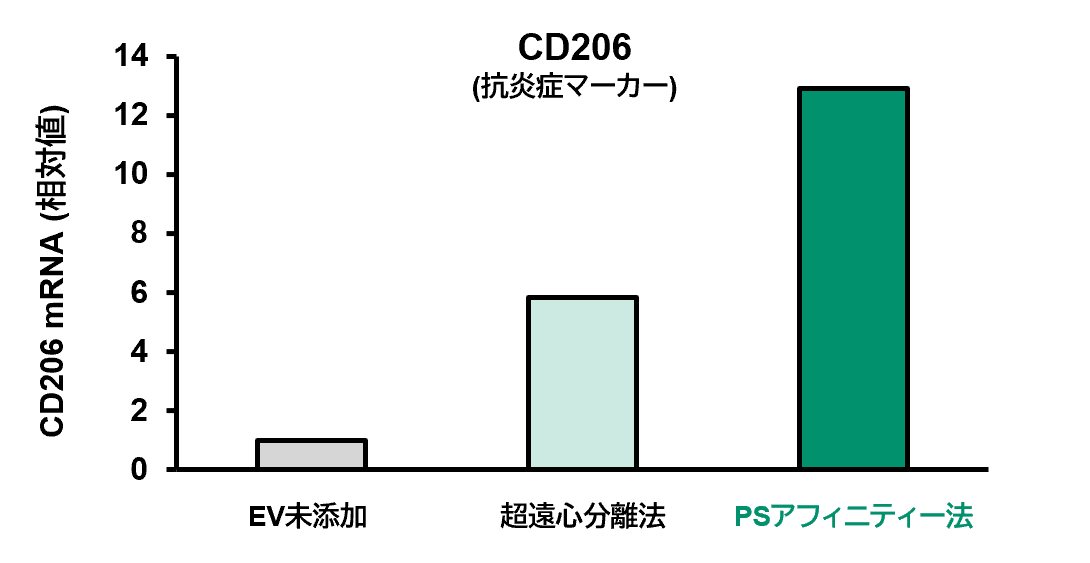
[結果]
本製品 (PSアフィニティー法) を用いることで、超遠心分離法よりも抗炎症活性の高いEVが得られた。
各サンプルからのEV単離・精製
血清・血漿
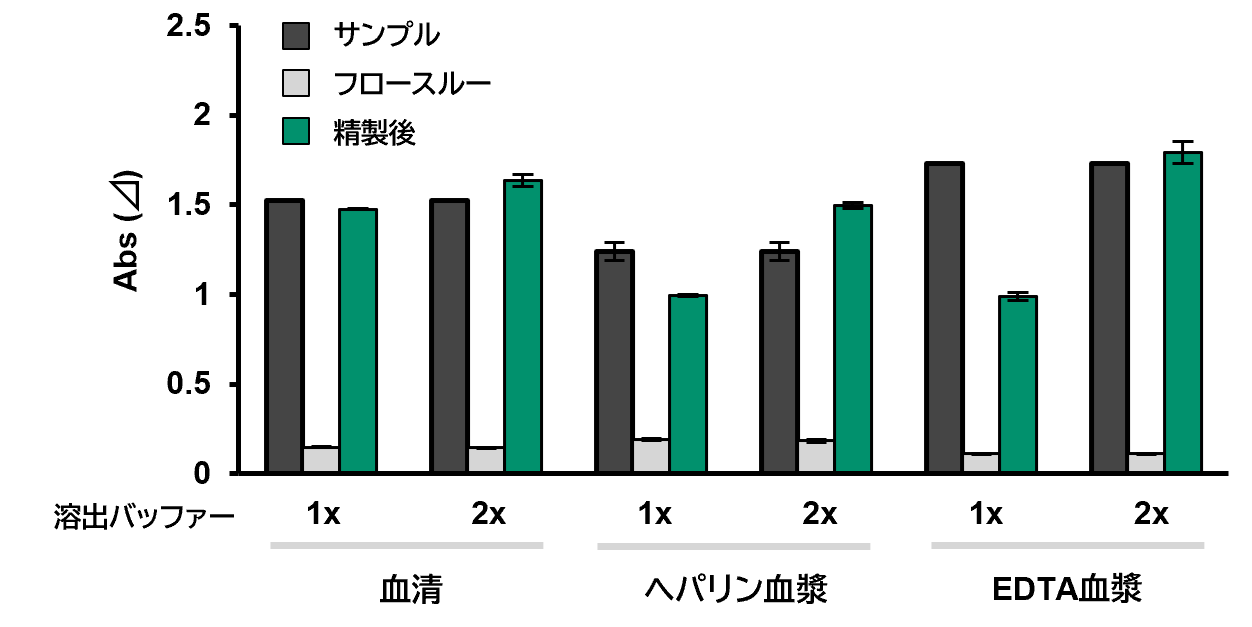
各種ヒト血液サンプルから本製品でEVを単離・精製した。EVの回収量はPS Capture™ エクソソームELISAキット(ストレプトアビジンHRP) (コードNo. 298-80601) で測定した。なお溶出バッファーは2種類の濃度 (1xおよび2x) で検討した。
[結果]
本製品によってヒト血清、血漿サンプルから高効率でEVを回収できた。
特に血漿サンプルは高濃度 (2x) の溶出バッファーを使用することで回収率が向上した。
細胞培養上清
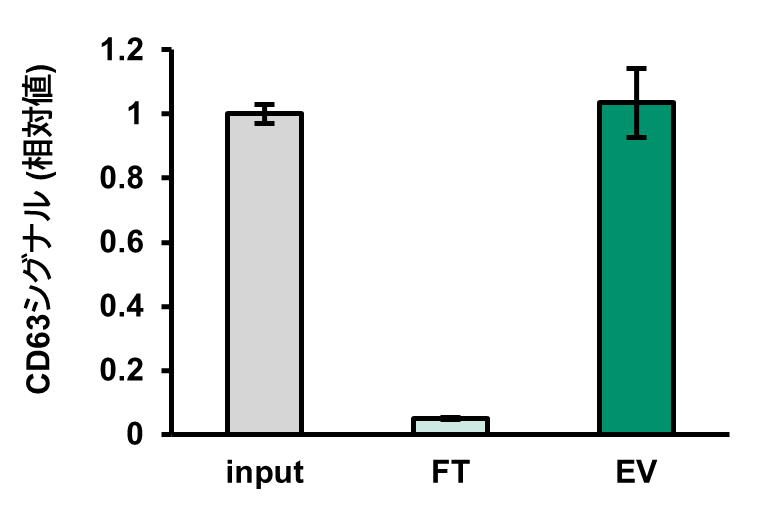
HEK293
HEK293を10% FBS含有D-MEM培地で増殖後、サプリメントを添加したEV産生培地 EV-Up™ MSC EV産生用基礎培地, AF (コードNo. 053-09451) で3日間培養した。その後、細胞培養上清から本製品でEVを単離・精製した。Input、フロースルー (FT)、単離後のEV溶液 (EV) 中のCD63シグナルを、CD63-Capture ヒトエクソソームELISAキット(ストレプトアビジンHRP) (コードNo. 290-83601)で測定し、EVの回収率を比較した。
[結果]
MagCapture™ Exosome Isolation Kit PS Ver.2は高いEV回収率を示した。
COLO201
COLO201細胞培養上清から本製品を用いてEVの単離・精製を行った。単離したEVもしくは同量の溶出バッファー (50 μL) を、あらかじめ播種したヒト正常線維芽細胞へ添加し、48時間経過時点での細胞形態変化を測定した。
-
精製EV
(0.7x107 particles)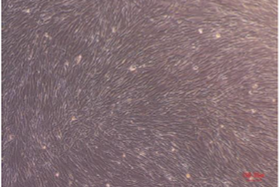
-
溶出バッファーのみ
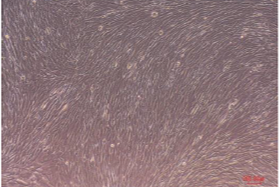
-
無処理
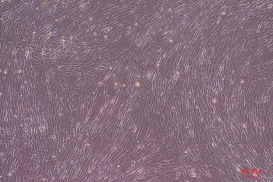
[結果]
本製品で単離・精製したEVや溶出バッファーを添加しても、細胞の形態変化や顕著な細胞死はほとんど観察されなかった。
溶出したEVはそのまま細胞添加に使用できることが示唆された。
※ 溶出バッファー中にはEDTAが含まれています。EDTAが影響を与える場合には、限外ろ過などによるバッファー交換が必要です。
参考文献
- Nakai, W. et al.: Sci. Rep., 6(1), 1(2016).
A novel affinity-based method for the isolation of highly purified extracellular vesicles
FAQ
PSアフィニティー法について
- 本製品の原理はどのようなものですか。
- エクソソームをはじめとする細胞外小胞 (EV: Extracellular Vesicle) の膜表面に存在するホスファチジルセリン (PS) と 金属イオン依存的にPSに結合する Tim4というタンパク質を利用してエクソソームなどの細胞外小胞を単離する手法です。
- どのような細胞外小胞が精製できますか。
- ホスファチジルセリンを脂質膜表面に露出しているエクソソームやマイクロベジクルを精製することができます。
- エクソソームとマイクロベジクルを別々に精製できますか。
- エクソソームとマイクロベシクルは大きさで明確に区別できないため完全に分けることはできませんが、 本製品では各々の主要な画分を得るために以下の簡便な分離方法を推奨しています。
エクソソームを始めとする粒子径が小さい細胞外小胞 (small EVs) を単離・精製する場合は、 10,000 x gで遠心分離した上清をサンプルとして使用してください。
マイクロベシクルを含む粒子径が大きい細胞外小胞 (large EVs) を精製する場合は、 まず 1,200 x gで遠心分離した上清を回収し、それを 10,000 x g で遠心分離して得られる沈殿をTBSに懸濁してサンプルとしてご使用ください。
また、両方を一緒に精製する場合は、1,200 x gで遠心分離した上清をサンプルとしてご使用ください。
- PSアフィニティー法ではEV以外も単離されるのでしょうか。
- エンベロープを持つウイルスを回収してくることがわかっています。エンベロープ型のウイルスの膜表面にもホスファチジルセリンが露出しているため、エンベロープ型ウイルスが混入しているサンプルでは、両方回収されます。そのためPSアフィニティー法はエンベロープ型ウイルスの回収に応用できる可能性があり、実際に
PSアフィニティー法を用いたウイルス精製の報告がございます2)。
なおウイルスを分離したい場合は、PSアフィニティー法で回収後、ウイルスに特異的な抗体を用いたアフィニティー精製を行う必要があります。これはPSアフィニティー法に限らず、エンベロープ上に存在するCD63などのEVマーカータンパク質に対する抗体を使った精製法でも同様のことが言えます。
<参考文献>
2) M. Santiana, et al.: Cell Host Microbe, 24, 208(2018).
- 全てのEVがPSを露出していますか。
- 全てのEVがPSを露出していることを示す知見は得られていませんが、下記論文において、クライオ電子顕微鏡解析および免疫金コロイド粒子を用いた活性化血小板由来EVの表現型解析が報告されています3)。本論文では、活性化血小板由来のEVの約75%がPSを表面に露出していることが報告されています。
3) Brisson, A. R., et al.: Platelets, 28(3), 263(2017).
当社の検討ではPSアフィニティー法による精製の前後で、試料に含まれるEV数をNTA法やELISA法を用いて比較すると、ほとんどの細胞や体液サンプルで、ほぼ90%以上のEVが回収されていることが確認されています。特にPSアフィニティー法で精製したEVでは、超遠心分離法やサイズ排除クロマトグラフィー法に比べて、低アニオン性EVの割合が高く、高アニオン性EVの割合が低いことが判明しました。
- 他のEV単離手法と比較した場合のPSアフィニティー法のメリットは何ですか。
- 超遠心分離法
高純度なEVを簡便に再現性良く高効率で回収することができます。また、超遠心分離法では沈殿しにくいようなサンプルからもEVを回収できることを確認しています。回収されるEVの純度も高く、超遠心分離法と密度勾配遠心法を組み合わせた場合と同等レベルの高純度なEVを回収することができます。さらにPSアフィニティー法では、同一原理でリッタースケールの細胞培養上清やサンプルを96検体同時処理が可能です。
ポリマー沈殿法
ポリマー沈殿法より回収効率が高く、高純度のEVが取得できます。
抗体アフィニティー法
抗体アフィニティー法は、EV表面抗原に対する抗体を用いているため変性剤による溶出や酸性条件下でEVを解離させて回収する必要があります。PSアフィニティー法は、中性条件下でキレート剤を用いて溶出するため、インタクトなEVを回収することができます。またビーズに非特異吸着したタンパク質の混入が少なく、より高純度なEVを回収でき、回収効率が高いことも確認しています。さらにPSアフィニティー法は膜脂質成分をターゲットとしているため、1種類のEV表面マーカータンパク質をターゲットとした抗体アフィニティー法より、広い範囲のEVを回収できると考えられます。
サンプルについて
- どのようなサンプルから精製できますか。
- 細胞培養上清、血清、血漿 (ヘパリン、EDTA、くえん酸)、尿、糞便から回収した実績があります。またユーザーより、脳脊髄液や唾液からのEV精製実績が報告されています。乳由来のEVは、乳中に含まれるアネキシンⅤがEV表面のPSに結合し、Tim4との結合を阻害する可能性があります。
- どのような動物種から単離できますか。
- ヒト、マウス、ラット、イヌ、サルなどから単離した実績があります。
- 精製に用いるサンプルの最低量はどのくらいですか。
- 安定的にビーズとサンプルを混合するために、ローテーターを用いて反応を行う場合は 500 μL 以上、チューブミキサーを用いて反応を行う場合は 100 μL 以上のサンプルを用いてください。 これより少ない量のサンプルを用いる場合は TBS を加えて最低量以上としてから Exosome Capture 固定化ビーズと反応させてください。また、フィルアップに用いるTBS には、EV-Save™ 細胞外小胞ブロッキング試薬 (コードNo. 058-09261) の添加を推奨します。
- 多量のサンプルから回収できますか。
- 本製品を使用する場合、細胞培養上清15 mL程度であれば濃縮せずに単離・精製が可能です。また濃縮などを行うことで50 mLまでのサンプルに対応できます。その場合、遠心分離前処理済みの細胞培養上清50 mLを1 mLまで限外ろ過濃縮してください (推奨フィルター: ザルトリウス社Vivaspin20、分画分子量100 K、メーカーコード: VS2041)。無血清培地だけではなく10%FBS添加培地にも対応できます。血清サンプルは濃縮できないため、使用できるのは1 mLまでです。 なお当社ではPSアフィニティー法を用いた細胞培養上清からのEV大量精製カラムとしてMassivEV™ EV Purification Column PSも販売しております。
- 限外濾過濃縮で分画分子量100K が推奨されていますが、10K は使用できませんか。
- 当社にて100 K、300 K、1,000 Kの限外濾過フィルターを比較し、濃縮時間および濃縮できたEV量の結果から100 Kを推奨しています。より小さな10 Kや30 Kも使用可能だと思われますが、濃縮時間が長くなる可能性があります。また、アルブミンを含む培地の場合、アルブミンが濃縮されるため、回収効率が低下する可能性があります。
- 血漿 (EDTA、くえん酸) サンプルにおけるヘパリン濃度の推奨はありますか。
- 当社では終濃度5 mUとなるようにヘパリンを添加しています。未添加でも5倍以上希釈すれば測定可能ですが、希釈時に凝集が見られることがあるので、ヘパリン添加を推奨します。
収量について
- 1回あたりのEVの取得量はどれくらいですか。
- サンプルの種類や量により大きく異なりますが、モネンシンナトリウムでEV分泌を亢進させた K562細胞培養上清 5 mLを 1 mLに濃縮してから精製操作を行った場合に、1回の精製操作でタンパク質量にして約30 μg/mL程度 (BCA 法で測定)、粒子数にして 1-2 x 1010 particles/mLの粒子が取得できています。また正常ヒトプール血清1 mLから1回の精製操作でタンパク質量にして約34 μg/mL程度、粒子数にして5 x 109 particles/mL程度の粒子が回収できています。
- EVの最大収量はどれくらいですか。
- 1アッセイの最大収量は約1-5×1010 particlesです。
- 1個のBiotin Capture Magnetic Beadsに結合するBiotin-labeled Exosome Captureも1個でしょうか。また、一つのExosome Capture固定化ビーズに捕捉されるEV数はいくつでしょうか。
- 1個のBiotin Capture Magnetic Beadsに対して複数のBiotin-labeled Exosome Captureが結合します。したがって1つのExosome Capture固定化ビーズに対して複数のEVが捕捉されます。
キット構成・操作について
- 溶出液の組成は何ですか。
- 1 mmol/Lのキレート剤、塩を含むPBSベースの溶液です。溶出液が以降の解析を阻害する場合は、限外ろ過 (ザルトリウス社 VivaSpin500、分画分子量100 K、メーカーコード: VS0141) もしくはゲルろ過により、適切なバッファーに置換してください。
- 本製品の操作で、特に慎重に行った方が良い操作は何ですか。
- Exosome Capture固定化ビーズとサンプルを反応させた後の洗浄ステップ最終段階で、洗浄液をしっかりと除去することです。完全に除去したことを確認後、溶出操作に入ってください。また溶出ステップでビーズに溶出液を加えた後、ビーズが凝集していないか確認しながらしっかりと懸濁してください。
- 実験操作を翌日まで持ち越せるステップはありますか。
- Exosome Capture固定化ビーズとサンプルを反応させるステップは終夜で反応させても問題ありません。反応時は冷蔵を推奨します。
- Exosome Capture を固定化した使用後の磁気ビーズのリサイクルは可能ですか。
- 可能です。サンプル中に残存するEVを再回収するため、使用した磁気ビーズを4回まで再生利用可能です。バッファー類も十分量同梱されていますので、同一サンプルからの繰り返し抽出やコンタミネーションしないケースであれば、最大50回 (10回用キットの場合) 使用可能な仕様となっています。またReaction Tubeもキット添付のWashing Bufferなどで洗浄すれば再利用可能です。 容量が1 mL 以上のサンプルから回収を行う場合や濃縮サンプルから回収する場合におすすめいたします。
- Exosome Capture 固定化磁気ビーズの保存は可能ですか。
- 可能です。EVを溶出した後のExosome Capture固定化ビーズを再利用する場合は、別途調製したTBSを用いて冷蔵保存し、できるだけ早くご使用ください。
アプリケーションについて
- 精製した細胞外小胞は、どういった解析に使用できますか。
- インタクトな細胞外小胞が得られますので、あらゆる解析に利用できます。
<解析例>
・タンパク質解析:タンパク質電気泳動、ウエスタンブロッティング、プロテオミクス解析、フローサイトメトリー、ELISA など
・核酸解析:qPCR、マイクロアレイ、次世代シークエンスなど
粒子解析:電子顕微鏡解析、Nanoparticle Tracking ・Analysis (NTA)など
・機能解析:in vitro、in vivo での投与実験など
- 各アプリケーションに必要なEVの量はどれくらいですか。
- 当社での実績を以下に記載します。
実験 サンプル量 (例) 電子顕微鏡解析 2-4 x 1010 particles/mL マイクロアレイ解析 COLO201: 4.6 x 1010 particles TIG3: 1.7 x 1010 particles iPSC: 1.9 x 109 particles プロテオミクス解析 精製EV 約1 μg (Nakai, W. et al.: Sci. Rep., 6(1), 1(2016)) ウエスタンブロッティング 溶出液100 μL の内、15 μLを使用
- 精製したEVの保存はどうすれば良いですか。
- EV-Save™ 細胞外小胞ブロッキング試薬を添加し、冷蔵または冷凍での保存を推奨しています。また、長期間保存する場合は-80℃で保管してください。EV-Save™細胞外小胞ブロッキング試薬を添加した状態で12ヶ月保管可能であることを確認しています。ただし、本製品はポリマーを含むため、プロテオミクス解析に使用する場合には、EV-Save™を除去する工程が必要です。
- 単離したEVはそのまま細胞への添加実験に使用できますか。
- 本製品の溶出バッファーは細胞毒性が低く、in vitro やin vivo の投与実験が可能です。ただし、溶出バッファー中のEDTAが問題となる場合はバッファー交換が必要となります。
トラブルシューティング
- 細胞培養上清から上手く精製できません。どのようにすれば良いですか。
- ポジティブコントロールをご用意ください。ポジティブコントロールは、HEK293など任意の細胞を培養していただき、細胞培養上清を必要量調製し、本製品を用いてEVを単離することで得られます。また培地中のEV量が少ない可能性があります。培養スケールを大きくしたり、培養条件を見直したりすることをご検討ください。
- 回収効率を向上させる方法はありますか。
- サンプルによっては通常プロトコルより Biotin-labeled Exosome Capture の固定化量を減少させることで回収効率が向上する場合があります。 通常プロトコルで回収効率が低いサンプルについては、Biotin-labeled Exosome Captureの添加量を減らして下さい (例 : 10 μL → 2-5 μL)。
- 本製品で精製したEVサンプルの総タンパク質量が他の単離手法と比較して少ないのは何が原因ですか。
- 他の手法で回収したEVサンプル中には、多くの不純物が混入しているため、総タンパク質量が多くなります。一方、本製品で精製したEVサンプルの総タンパク質量は少ないですが、サンプルの純度が高いため、実際に得られるEV量は他の単離手法と比較して同等以上と考えています。
- 磁気ビーズがマグネットスタンドに集まりません。原因として考えられることはありますか。
- サンプル中のキレート剤として働く成分 (くえん酸など) によって磁気ビーズの構成成分である鉄が酸化してしまい、吸着能が低下している可能性があります。
概要・使用例
| 概要 | 本キットは、細胞培養上清、血清、血漿などのサンプルから高純度な細胞外小胞をアフィニティー法によって簡便に精製できます。細胞外小胞の膜表面に存在するホスファチジルセリン(PS)にカルシウム依存的に結合する物質を応用しているため、キレート剤によりインタクトな状態で細胞外小胞を精製ビーズから溶出できます。 【特長】 (1)新規アフィニティー法(PSアフィニティー法)により高純度な細胞外小胞が取得可能 (2)従来の超遠心分離法よりも高い収量で高純度なエクソソームが取得可能 (3)インタクトな細胞外小胞が取得でき、様々なアプリケーションに利用可能 (4)磁気ビーズによる簡便操作 (5)超遠心分離が不要 |
|---|---|
| 構成 | ・2回用 1) Biotin Capture Magnetic Beads 120 μL×1本 2) Biotin-labeled Exosome Capture 20 μL×1本 3) Exosome Immobilizing/Washing Buffer(10x) 5 mL×1本 4) Exosome Binding Enhancer(500x) 300 μL×1本 5) Exosome Elution Buffer(10x) 300 μL×1本 6) Reaction Tubes 4本 ・10回用 1) Biotin Capture Magnetic Beads 600 μL×1本 2) Biotin-labeled Exosome Capture 100 μL×1本 3) Exosome Immobilizing/Washing Buffer (10x) 25 mL×1本 4) Exosome Binding Enhancer(500x) 1500 μL×1本 5) Exosome Elution Buffer(10x) 1500 μL×1本 6) Reaction Tubes 22本 |
物性情報
「物性情報」は参考情報でございます。規格値を除き、この製品の性能を保証するものではございません。
本製品の品質及び性能については、本品の製品規格書をご確認ください。
なお目的のご研究に対しましては、予備検討を行う事をお勧めします。
製造元情報
別名一覧
【本サイト掲載情報について】
- 掲載内容は本記事掲載時点の情報です。仕様変更などにより製品内容と実際のイメージが異なる場合があります。
- 製品規格・包装規格の改訂が行われた場合、画像と実際の製品の仕様が異なる場合があります。
- 掲載されている製品について
- 【試薬】
- 試験・研究の目的のみに使用されるものであり、「医薬品」、「食品」、「家庭用品」などとしては使用できません。
- 試験研究用以外にご使用された場合、いかなる保証も致しかねます。試験研究用以外の用途や原料にご使用希望の場合、弊社営業部門にお問合せください。
- 【医薬品原料】
- 製造専用医薬品及び医薬品添加物などを医薬品等の製造原料として製造業者向けに販売しています。製造専用医薬品(製品名に製造専用の表示があるもの)のご購入には、確認書が必要です。
- 表示している希望納入価格は「本体価格のみ」で消費税等は含まれておりません。
- 表示している希望納入価格は本記事掲載時点の価格です。










