DNAエキストラクターR キット
DNA ExtractorR Kit
- 遺伝子研究用
-
for Genetic Research
- 製造元 :
- 富士フイルム和光純薬(株)
- 保存条件 :
- 室温
- 適用法令 :
- 安衛法57条・有害物表示対象物質 有機則第2種 労57-2 優先評価物質 危4-ア(水溶性)-II
- GHS :
-
- 構造式
- ラベル
- 荷姿
|
比較
|
製品コード
|
容量
|
価格
|
在庫 / 納期目安
|
|
|---|---|---|---|---|---|
|
|
|
50回用
|
|
|
ドキュメント
キットコンポーネント
50回用
| よう化ナトリウム溶液 | 26 mL x 1本 |
|---|---|
| N-ラウロイルサルコシン酸ナトリウム溶液 | 1.2 mL x 1本 |
| 洗浄液(A) | 42 mL x 1本 |
| 洗浄液(B) | 40 mL x 2本 |
| グリコーゲン溶液 | 0.1 mL x 1本 |
概要
ワクチン・バイオ医薬品などの残留DNA検査に
生物由来成分に残留する宿主細胞由来のDNAをよう化ナトリウム法*で抽出するキットです。抽出したDNAはqPCRで定量できます。CHO細胞、大腸菌、酵母などホストセル由来DNA量の検査、管理にご使用ください。
本製品でDNAを抽出後、Molecular Devices社のThreshold systemsを使用することで、由来種を問わない総DNAの定量も可能です。
ヒト血清中のウイルスDNAの定量に
ヒト血清中のウイルスDNAの抽出にご使用いただけます。
*よう化ナトリウム法:USP(The United States Pharmacopeia)42-NF37の<509>Residual DNA Testingで紹介されている残留DNA抽出法
特長
- 微量DNA(100-1,000 fg)を高い収率で回収
- チューブ交換不要(チューブ1本で全工程完了)
- スタートから抽出完了まで60-90分間
- 高濃度タンパク質含有サンプル用の前処理プロトコルあり
- 回収後のDNAはqPCR、Threshold Assay(Molecular Devices社)で定量可能
- よう化ナトリウム法採用
よう化ナトリウム法によるDNA抽出の基本原理
- サンプルにカオトロピックイオンであるよう化ナトリウムと界面活性剤を添加し、タンパク質および脂質を可溶化します。
- グリコーゲンを添加したサンプルに2-プロパノールを添加し、DNAをグリコーゲンと共沈させます。
- DNAペレットを回収します。
アプリケーション
CHO由来DNAの添加回収試験
培養上清を用いて、CHO由来DNAの添加回収率を調べた。
方法
- 10 fgから1 ngまでのCHO由来DNAをPANC-1細胞培養上清に添加した。
- 本製品の説明書に記載のプロトコルに従いDNAを抽出した。
・抽出プロトコル: プロトコル #2
・前処理:なし - 抽出したDNAに対してqPCRを行いCq値を測定した。またCHO由来DNAを添加した精製水をDNA抽出処理せずqPCRを行い、Cq値を測定した。これを標準条件とした。
- 標準条件で検量線を作成し、各条件でのDNA回収率を算出した。
サンプル
- 標準条件:CHO由来DNAを添加した精製水(DNA抽出操作なし)
- 培養上清:CHO由来DNAを添加したPANC-1細胞培養上清から本製品で抽出したDNA
使用したqPCR試薬類
- GeneAce SYBR® qPCR Mix α No ROX(ニッポンジーン 製品コード:319-07703)
- Optical Flat 8–Cap Strips for 0.2 mL tube strips/Plates (BIO-RAD社コード:TCS0803)
- Hard-Shell PCR plates 96 well, thin-wall (BIO-RAD社コード:HSP9601)
結果
| 1. 標準条件 | 2. 培養上清 | |||||
|---|---|---|---|---|---|---|
| 添加量(fg) | Cq 1 | Cq 2 | 平均値 | Cq 1 | Cq 2 | 平均値 |
| 0 | ND | |||||
| 10 | ||||||
| 100 | 36.89 | ND | 36.89 | 37.44 | 36.73 | 37.09 |
| 1,000 | 33.44 | 33.91 | 33.68 | 33.94 | 34.09 | 34.01 |
| 10,000 | 30.23 | 30.17 | 30.2 | 30.72 | 30.96 | 30.84 |
| 100,000 | 26.74 | 26.68 | 26.71 | 26.9 | 27.03 | 26.96 |
| 1,000,000 | 23.39 | 23.28 | 23.33 | 23.61 | 23.48 | 23.54 |
-
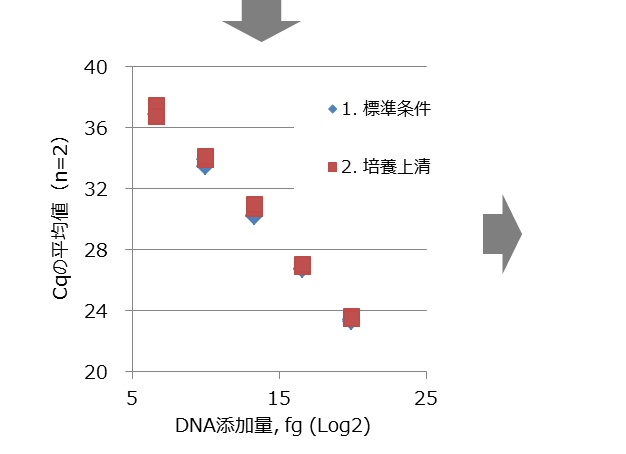
DNA添加量とCqの平均値
1.標準条件 :R2=0.9998
2.培養上清 :R2=0.9982 -
2. 培養上清 添加量(fg) 回収量(fg) 回収率(%) 0 ND 10 100 93 93 1,000 741 74 10,000 6,333 63 100,000 86,703 87 1,000,000 874,502 87
標準条件のCq平均値で検量線を作成し、他の条件のCq平均値からDNA回収率を算出した。
100 fgから1 ngのDNA添加量において、培養上清中のDNAを高い収率で回収できた。
大腸菌由来DNAの添加回収試験
大腸菌 (E.coli) 由来DNAの添加回収率を調べた。
方法
- 10 fgから1 ngまでの大腸菌由来DNAを精製水に添加した。
- 本製品の説明書に記載のプロトコルに従いDNAを抽出した。
・抽出プロトコル: プロトコル #1 - qPCRにより、DNA抽出処理前後のCq値をそれぞれ測定した。
- DNA抽出前のCq平均値で検量線を作成し、DNA抽出後の回収率を算出した。
サンプル
大腸菌由来DNAを添加した精製水
使用したqPCR試薬類
- GeneAce SYBR® qPCR Mix α No ROX(ニッポンジーン 製品コード:319-07703)
- Optical Flat 8–Cap Strips for 0.2 mL tube strips/Plates (BIO-RAD社コード:TCS0803)
- Hard-Shell PCR plates 96 well, thin-wall (BIO-RAD社コード:HSP9601)
結果
-
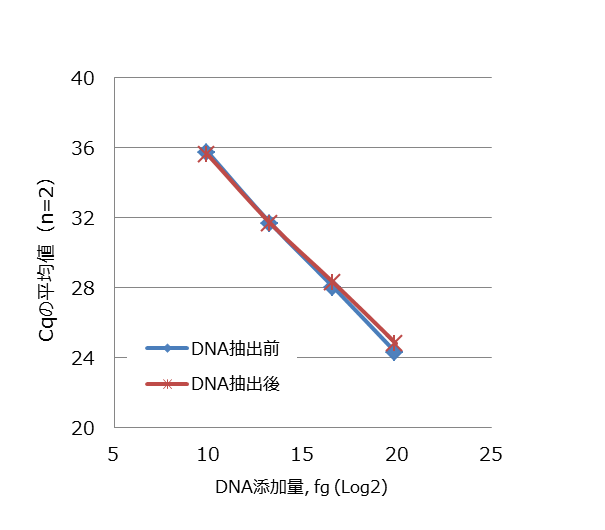
DNA添加量とCqの平均値
DNA抽出前:R2= 0.9995
DNA抽出後:R2= 0.9989 -
大腸菌 添加量(fg) 回収量(fg) 回収率(%) 0 ND - 10 100 1,000 1,031 103 10,000 11,093 111 100,000 85,094 85 1,000,000 703,059 70 DNA抽出前のCq平均値で検量線を作成し、DNA抽出後のCq平均値からDNA回収率を算出した。
1 pgから1 ngのDNA添加量において、大腸菌由来DNAを高い収率で回収できた。
ヒト血清へのDNA添加回収試験
λ/HindⅢ 10~1,000 pgを32Pラベルし、100 μLのヒト血清に添加し、本製品によりDNA抽出を行い、回収率を求めた。
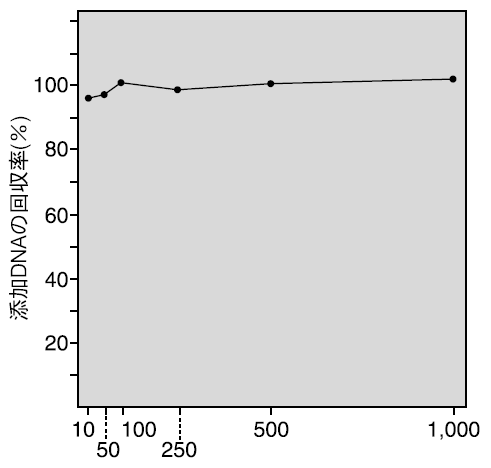
いずれのDNA量においても高い回収率を示した。
PCRによるヒト血清中HBV(B型肝炎ウイルス)の検出
HBV(B型肝炎ウイルス)が含まれるヒト血清を段階的に希釈し、本製品およびフェノール法によりDNA抽出を行った。抽出したDNAに含まれるHBV-DNAをPCRにより増幅し、アガロースゲル電気泳動を行った。
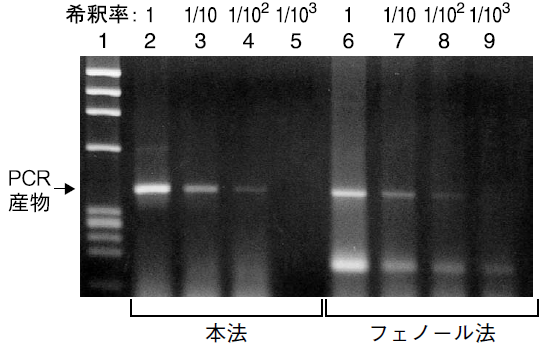
Lane 2-9 :希釈検体
フェノール法よりも本法の方が特異的かつ高感度にHBV-DNAを検出できた。
抗体医薬品への適用性検討
高タンパク質溶液からのDNA抽出
種々の濃度のIgG溶液を用いて、CHO由来DNAの添加回収率を調べた。
方法
- 各種濃度のIgG溶液 (10-100 mg/mL) に、CHO由来DNAを2 pg/mLになるように添加した。
- 本製品の説明書に記載のプロトコルに従いDNAを抽出した。
・抽出プロトコル:プロトコル #2
・サンプル前処理:タンパク質濃度が2 mg/mL以上の場合の前処理プロトコル (Proteinase K処理) 実施 - qPCR法により、抽出したCHO由来DNAの回収率を算出した。
結果
各タンパク質濃度溶液からのCHO由来DNA回収率
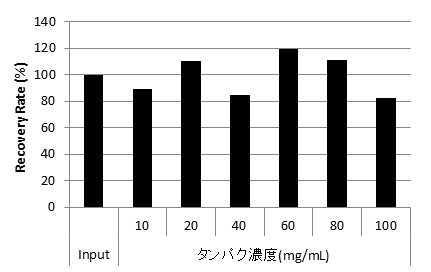
各タンパク質濃度溶液のCq値
| Sample | Input | タンパク濃度 (mg/mL) | |||||
|---|---|---|---|---|---|---|---|
| 10 | 20 | 40 | 60 | 80 | 100 | ||
| Cq | 31.596 | 31.566 | 31.351 | 31.726 | 31.502 | 31.282 | 31.658 |
| 31.599 | 31.608 | 31.774 | 31.787 | - | 31.485 | 31.660 | |
| 31.338 | 31.861 | 31.500 | 31.850 | 31.560 | 31.369 | - | |
| Average Cq | 31.511 | 31.678 | 31.542 | 31.788 | 31.531 | 31.379 | 31.659 |
| Difference of Cq | 0 | -0.167 | 0.136 | -0.246 | 0.257 | 0.152 | -0.280 |
| Power | 1 | 0.891 | 1.099 | 0.843 | 1.195 | 1.111 | 0.824 |
| Recovery Rate (%) | 100 | 89.1 | 109.9 | 84.3 | 119.5 | 111.1 | 82.4 |
100 mg/mLの高濃度タンパク質存在下でも、高い収率でCHO由来DNAを抽出できた。
抗体医薬品模倣溶液からのDNA抽出
抗体医薬品に一般的に使用されるBufferおよび添加物を用いて作製したIgG溶液に対して、CHO由来DNAの添加回収率を調べた。
方法
- 抗体医薬品に用いられる一般的なBuffer組成(表1. ①‐⑥)および、添加物溶液(表2. ①‐⑩)に20 mg/mLのIgGタンパク質を加え、各種の抗体医薬品模倣溶液を作製した。各溶液にCHO由来DNAを20 pg/mLになるように添加した。
- 本製品の説明書に記載のプロトコルに従いDNAを抽出した。
・抽出プロトコル:プロトコル #2
・サンプル前処理:タンパク質濃度が2 mg/mL以上の場合の前処理プロトコル (Proteinase K処理) 実施 - qPCR法により、抽出したCHO由来DNAの回収率を算出した。
-
表1 Buffer組成
No. Buffer組成 ① 10mM PB pH6.0, 0.15M NaCl, 2mM EDTA ② 10mM PB pH7.4, 0.15M NaCl, 2mM EDTA ③ 50mM NaOAc pH5.2, 0.15M NaCl, 2mM EDTA ④ 10mM PB pH6.0, 2mM EDTA ⑤ 10mM PB pH7.4, 2mM EDTA ⑥ 50mM NaOAc pH5.2, 2mM EDTA -
表2 添加物溶液
Buffer: 10mM PB pH6.0, 0.15M NaCl, 2mM EDTA
No. 添加物 (濃度) ① Sucrose (10w/v%) ② Trehalose Dihydrate (10w/v%) ③ D(-)-Mannitol (10w/v%) ④ D(-)-Sorbitol (10w/v%) ⑤ D(+)-Maltose Monohydrate (10w/v%) ⑥ L(+)-Arginine Hydrochloride (1w/v%) ⑦ L‐Histidine (1w/v%) ⑧ Glycine (1w/v%) ⑨ Polyoxyethylene(20) Sorbitan Monooleate (Tween80) (0.5v/v%) ⑩ Polyoxyethylene(20) Sorbitan Monolaurate (Tween20) (0.5v/v%)
結果
各種BufferからのCHO由来DNA回収率
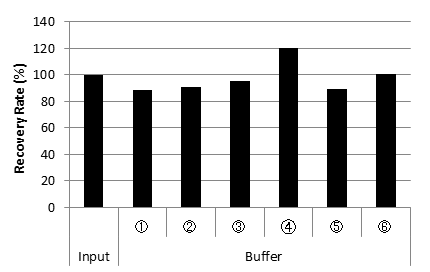
各種BufferのCq値
| Sample | Input | Buffer | |||||
|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | ||
| Cq | 31.473 | 31.693 | 31.544 | 31.218 | 31.058 | 31.595 | 31.181 |
| 31.364 | 31.196 | 30.973 | 31.568 | 31.085 | 31.343 | 31.112 | |
| 31.045 | 31.530 | 31.787 | 31.315 | 30.942 | 31.452 | 31.558 | |
| Average Cq | 31.294 | 31.473 | 31.435 | 31.367 | 31.028 | 31.463 | 31.284 |
| Difference of Cq | 0 | -0.179 | -0.141 | -0.073 | 0.266 | -0.169 | 0.010 |
| Power | 1 | 0.883 | 0.907 | 0.951 | 1.203 | 0.890 | 1.007 |
| Recovery Rate (%) | 100 | 88.3 | 90.7 | 95.1 | 120.3 | 89.0 | 100.7 |
各添加物溶液のCq値
| Sample | Input | 添加物溶液 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
| Cq | 31.473 | 31.826 | 31.327 | 30.907 | 31.143 | 31.071 | 31.525 | - | 31.525 | 31.013 | 31.086 |
| 31.364 | 31.194 | 30.991 | 31.759 | 31.103 | 31.279 | 31.068 | 31.442 | 31.203 | 31.340 | 30.870 | |
| 31.045 | 30.703 | - | 31.009 | - | 30.978 | 31.225 | 31.479 | 30.757 | 31.020 | 31.020 | |
| Average Cq | 31.294 | 31.241 | 31.159 | 31.225 | 31.123 | 31.109 | 31.273 | 31.461 | 31.162 | 31.124 | 30.992 |
| Difference of Cq | 0 | 0.053 | 0.135 | 0.069 | 0.171 | 0.185 | 0.021 | -0.167 | 0.132 | 0.170 | 0.302 |
| Power | 1 | 1.037 | 1.098 | 1.049 | 1.126 | 1.137 | 1.015 | 0.891 | 1.096 | 1.125 | 1.233 |
| Recovery Rate (%) | 100 | 103.7 | 109.8 | 104.9 | 112.6 | 113.7 | 101.5 | 89.1 | 109.6 | 112.5 | 123.3 |
各添加物溶液のCHO由来DNA回収率
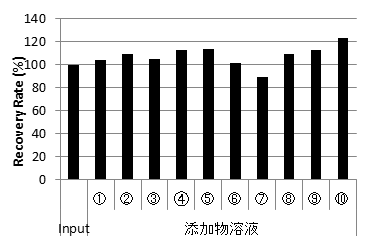
種々のBuffer組成、添加物を含むIgG溶液からでも高い収率でCHO由来DNAを抽出できた。
概要・使用例
| 概要 | <ワクチン・バイオ医薬品などの残留DNA検査に> <ヒト血清中のウイルスDNAの定量に> 宿主由来の残留DNAや血清中DNAをよう化ナトリウム法*で抽出するキットです。抽出したDNAはqPCRで定量できます。CHO細胞、大腸菌、酵母など宿主由来DNA量の検査、血清中のウイルスDNAの定量にご使用ください。 また、本キットでDNAを抽出後、Molecular Devices社のThreshold systemsを使用することで、由来種を問わない総DNAの定量も可能です。 *よう化ナトリウム法:USP(The United States Pharmacopeia)42-NF37の<509>Residual DNA Testingで紹介されている残留DNA抽出法 測定原理よう化ナトリウムと界面活性剤により、試料中のタンパク質および脂質などを可溶化状態にし、そこへイソプロパノールを添加することで、核酸をグリコーゲンと共沈させる。この時カオトロピックイオンのよう化ナトリウムおよび界面活性剤が試料中のタンパク質を始めとした成分の沈殿を妨げるため、DNAが選択的に沈殿する。 和光純薬時報 Vol.60 No.3 p.28(1992)。 [参考文献] ・ Ishizawa, M., Kobayashi, Y., Miyamura, T. and Matsuura, S. : ''Simple procedure of DNA isolation from human serum'', Nucleic Acids Res., 19, 5792(1991) ・ 本法はUSP39-NF34, page 1413/Pharmacopeial Forum. Vol.41(4)に収載された。 ・ Hui Cai, Xuelin Gu, Mary S. Scanlan, and Chris R. Lively,: Development of a quantitative PCR assay for residual mouse DNA and comparison of four sample purification methods for DNA isolation., Journal of Pharmaceutical and Biomedical Analysis, 55, 71-77 (2011). |
|---|---|
| 特長 | -微量DNA(100-1,000 fg)を高い収率で回収 -チューブ交換不要(チューブ1本で全工程完了) -スタートから抽出完了まで60-90分間 -高濃度タンパク質含有サンプル用の前処理プロトコルあり -回収後のDNAはqPCRおよびThreshold Assay(Molecular Devices社)で定量可能 -よう化ナトリウム法採用 -フェノール、クロロホルム不要 |
| 構成 | 構成 1.よう化ナトリウム溶液…26ml 2.N-ラウロイルサルコシン酸ナトリウム溶液…1.2ml 3.洗浄液(A)…42ml 4.洗浄液(B)…40mlx2 5.グリコーゲン溶液…0.1ml |
| 用途 | DNA抽出用キット。 |
| 使用上の注意 | 血液および培養細胞、組織からゲノムDNAを抽出する場合は、DNA Extractor WB Kitをご使用下さい。 キット部材の「よう化ナトリウム溶液」、「N-ラウロイルサルコシン酸ナトリウム溶液」の保存中に結晶が析出した時は、50℃に加温して結晶を溶かしてから使用して下さい。 |
物性情報
「物性情報」は参考情報でございます。規格値を除き、この製品の性能を保証するものではございません。
本製品の品質及び性能については、本品の製品規格書をご確認ください。
なお目的のご研究に対しましては、予備検討を行う事をお勧めします。
製造元情報
別名一覧
- 掲載内容は本記事掲載時点の情報です。仕様変更などにより製品内容と実際のイメージが異なる場合があります。
- 製品規格・包装規格の改訂が行われた場合、画像と実際の製品の仕様が異なる場合があります。
- 掲載されている製品について
- 【試薬】
- 試験・研究の目的のみに使用されるものであり、「医薬品」、「食品」、「家庭用品」などとしては使用できません。
- 試験研究用以外にご使用された場合、いかなる保証も致しかねます。試験研究用以外の用途や原料にご使用希望の場合、弊社営業部門にお問合せください。
- 【医薬品原料】
- 製造専用医薬品及び医薬品添加物などを医薬品等の製造原料として製造業者向けに販売しています。製造専用医薬品(製品名に製造専用の表示があるもの)のご購入には、確認書が必要です。
- 表示している希望納入価格は「本体価格のみ」で消費税等は含まれておりません。
- 表示している希望納入価格は本記事掲載時点の価格です。









