『細胞の』ATP測定試薬 Ver.2
''Cell'' ATP Assay reagent Ver.2
- 製造元 :
- 東洋ビーネット(株)
- 保存条件 :
- 冷凍 (ドライアイス輸送)
- 構造式
- ラベル
- 荷姿
ドキュメント
特長
『細胞の』ATP測定試薬® Ver.2は、細胞数の少ない培養初期から生細胞数の変化をみることができます。細胞溶解成分やATPaseブロッキング試薬を含んだ1液型の発光試薬で、試薬を添加・混和するだけの1ステップで測定が開始できます。試薬の調製や培地の除去、細胞の洗浄は不要で、試薬の添加により細胞中からATPが抽出され、ATP量に比例した発光を生じます。発色法では困難な浮遊細胞も接着細胞と同様に測定できます。また、検体との混和性に優れているため、384ウェルプレート使用時の混和不足により生じる時間経過に伴う発光量のずり上がり現象もなく安定しています。HTSなどの96/384ウェルプレートを用いた多検体測定に適した仕様です。
| ・安定性 ・高感度 ・簡便 ・迅速 ・高溶解力 ・発光安定 ・安全性 |
:-20℃での長期保管が可能 :384ウェルプレートでの二次元培養で10個の細胞から検出 :細胞溶解剤を含んだ一液型で操作は1ステップ(試薬添加・混和 ⇒ 測定) :試薬添加後10分から測定が可能 :細胞溶解不足による時間経過による発光量上昇は生じない :発光が長時間安定(発光半減期 3時間以上) :毒劇物該当物質を含まない |
参考データ
-
室温(23℃)静置安定性試験
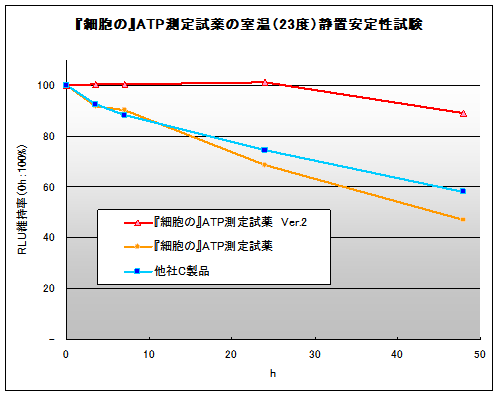
図1.『細胞の』ATP測定試薬®の室温(23℃)配置安定性試験
室温(23℃)に静置した時の試薬劣化度を測定。
Ver.2は室温下でも24時間経過時でも劣化は示さず、昼夜の連続測定にも安心して
使用可能。 -
加温(37℃)試験
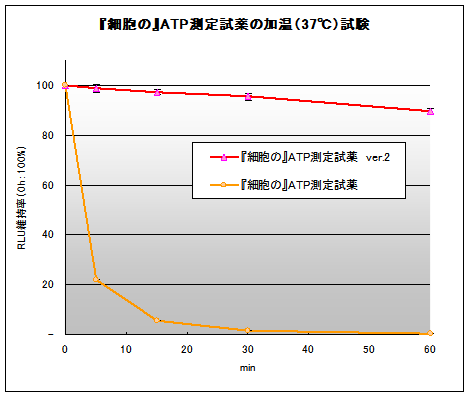
図2.『細胞の』ATP測定試薬®の加温(37℃)試験
加温(37℃)したときの試薬の性能劣化度を測定。
Ver.2は試薬融解時の加温ダメージが小さいことを示す。
-
生細胞と発光量の相関
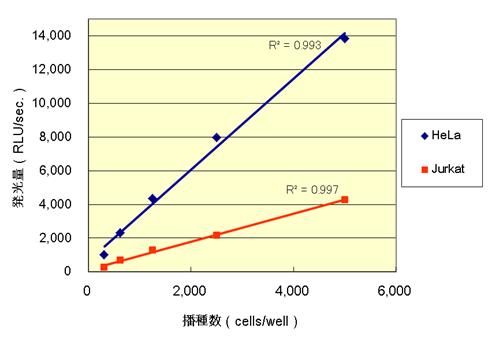
図3.384well プレートにおける細胞数測定
2倍希釈系列に調製した各細胞を分注し(25 µL/well)、4時間培養後、等量の『細胞の』ATP測定試薬® Ver.2 を加え、ルミノメーターで測定(n=3)。
※Jurkat (RPMI1640 + 10% FBS)
※HeLa (MEM + 10% FBS + 1% NEAA) -
各種細胞株のカイネティクスと発光安定性
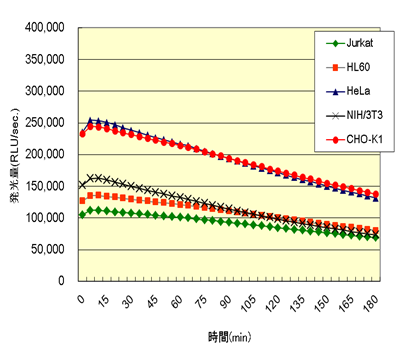
図4.96well プレートにおけるカイネティクス
各細胞※を10,000 cells/wellになるように分注し(100 µL)、一晩培養後、等量の『細胞の ATP測定試薬® Ver. 2を加え、ルミノメーターで測定(n=3)。各細胞における発光半減期は、3時間以上。 ※Jurkat, HL60 (RPMI1640 + 10% FBS)
※HeLa, HepG2 (MEM + 10% FBS+1% NEAA)
※NIH/3T3 (DMEM + 10% FCS)
※CHO-K1 (HamF12 + 10% FBS)
-
生細胞と発光量の相関
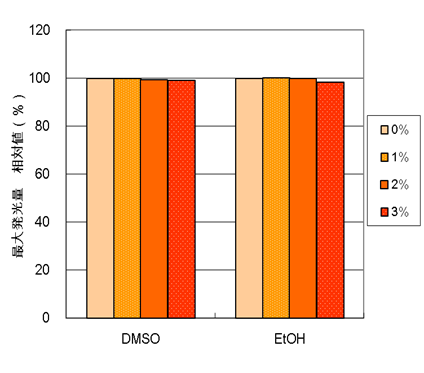
図5.96wellプレートにおける有機溶媒の影響
各濃度の溶媒を含んだDMEM培地でATP溶液(1.E-6M)を調製し、各ウェルに100 μLずつ分注。等量の『細胞の』ATP測定試薬® Ver.2を加えた後、ルミノメーターで測定(n=3)。グラフは、溶媒無添加時の最大発光量に対する相対値で表示。添加量3%以内では、最大発光量にほとんど影響を及ぼさなかった。
プロトコル
- 『細胞の』ATP測定試薬® Ver.2を4℃または室温で、遮光下に解凍し、測定前に室温に戻す。※1, ※2
- 解凍後、試薬瓶をゆっくり数回逆さにしてよく混合する ( 解凍の過程で生じた試薬成分の偏りを均一化する) 。※3
- 試薬添加30分前に、培養プレートを室温に静置し、培地を室温に戻す。
- 『細胞の』ATP測定試薬® Ver.2を96ウェルプレートに100 μLずつ加える。( 25 μL/well for 384 well plates ) ※4, ※5
- マイクロプレートシェーカーで1分間攪拌する。
- プレートを23℃に温度設定したルミノメーターの中で10分間静置する。※6, ※7
- 23℃に温度設定したルミノメーターで発光量の測定を行なう。※7
- 1:本製品をただちに使用したい場合は、37℃で解凍することが可能です。その場合、試薬の解凍が完了したらすぐに室温に戻してください。解凍後、使用しない残りの試薬は、-20℃で遮光保存してください。
- 2:試薬へのATPの混入を防ぐために、プロトコールの全操作に渡って、手袋およびマスクの着用をお勧めします。
- 3:混合の際、ボルテックスミキサー等を用いた激しい攪拌は避けてください。
- 4:培地除去、細胞洗浄は不要です。
- 5:本試薬は光に敏感です。直射日光が当たる所や蛍光灯の直下での作業は控えてください。
- 6:プレートを23℃に温度設定したルミノメーターの中で10分間静置することにより、プレート内の温度がルミノメーター内の温度と平衡化されます。(プレートを室温に10分間静置した時に比べ、発光の安定性がさらに向上します。)
- 7:お使いのルミノメーターの機種によっては、ルミノメーターの温度を24℃または25℃に設定することにより、試薬の10分間静置後からの発光の安定性がさらに向上します。
アプリケーションデータ
測定条件 |
実験手順 |
|
|
測定結果
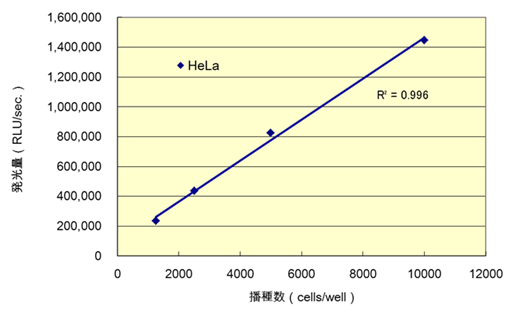
発光試薬『細胞の』ATP 測定試薬® Ver.2 と、マルチタイプのプレートリーダー Infinite® 200PRO を用いて細胞のATP 量の発光測定を行なうと、細胞数に比例したATP 量が確認できた。この結果より、本手法では標準偏差が小さく高精度な検量線が得られ、細胞数とATP 量による発光測定値の相関性が高いため、試薬および測定機器の性能と操作性が高いことがわかる。
参考文献
- Okamoto, A., Koike, M., Yasuda, K., Kakizuka, A. : Biochem. Biophys. Res. Commun., 394, 42 (2010).
- Jia, X., et al. : Life Science., 90(23), 934 (2012).
- Hiyama, G., et al. : Reproduction, 147, 167 (2014).
- Kikuchi, H., Yuan, B., Yuhara, E., Takagi, N., Toyoda, H. : Int . J. Oncol., 43(6), 2046 (2013).
- Kikuchi, H., et al. : Int . J. Oncol., 45(2), 1019 (2014).
- Matsuzaki, M., et al. : Scientific Repports, 5, 17643 (2015).
- Suzuki, T., et al. : Tohoku J. Exp. Med., 236 , 225-232 (2015).
- Matsuzaki, M., Mizushima, S., Ichikawa, Y., Shiba, K., Inaba, K., Sasanami, T. : J. Poult. Sci., 54 ,73 (2017).
- Sakamoto, A., Saotome, M., Hasan, P., Satoh, T., Ohtani, H., Urushida, T., Katoh, H., Hayashi, H. : Experimental Cell Research, 351(1), 109 (2017).
- Morimoto, H., Gu, L., Zeng, H., Maeda, K. : Cosmetics, 4(4), 38 (2017).
- Maeshima, K., et al. : Current Biology, 28 (3), 444 (2018).
物性情報
「物性情報」は参考情報でございます。規格値を除き、この製品の性能を保証するものではございません。
本製品の品質及び性能については、本品の製品規格書をご確認ください。
なお目的のご研究に対しましては、予備検討を行う事をお勧めします。
製造元情報
別名一覧
- 掲載内容は本記事掲載時点の情報です。仕様変更などにより製品内容と実際のイメージが異なる場合があります。
- 製品規格・包装規格の改訂が行われた場合、画像と実際の製品の仕様が異なる場合があります。
- 掲載されている製品について
- 【試薬】
- 試験・研究の目的のみに使用されるものであり、「医薬品」、「食品」、「家庭用品」などとしては使用できません。
- 試験研究用以外にご使用された場合、いかなる保証も致しかねます。試験研究用以外の用途や原料にご使用希望の場合、弊社営業部門にお問合せください。
- 【医薬品原料】
- 製造専用医薬品及び医薬品添加物などを医薬品等の製造原料として製造業者向けに販売しています。製造専用医薬品(製品名に製造専用の表示があるもの)のご購入には、確認書が必要です。
- 表示している希望納入価格は「本体価格のみ」で消費税等は含まれておりません。
- 表示している希望納入価格は本記事掲載時点の価格です。



