ミクログリア除去試薬
ミクログリアは遺伝学的もしくは薬理学的な手法を持用いて除去することが可能であり、ミクログリアの役割を理解するにあたって有効な手段と考えられています。これまでに様々な手法が開発されていますが、それぞれに長所と短所があるため、性質を理解した上で適切な方法を選択する必要があります。当社では、クロドロン酸内包リポソームを用いたミクログリア除去試薬を販売しております。
ミクログリア除去の方法
ミクログリア(Microglia)は、中枢神経系の免疫機能を担っているグリア細胞です。異物・死細胞の貪食やケモカイン・サイトカインの放出を行うほか、神経細胞をモニターしたり、シナプスの剪定に関与したりするなど、中枢神経系の発生や機能発現にも重要な役割を果たしています。またアルツハイマー病やうつ病などの神経・精神疾患において、ミクログリアは機能回復や進行抑制に貢献する一方で、脳内炎症を引き起こすため発症や増悪の原因ともなっています。
ミクログリアの除去は、ミクログリアの役割を明らかにするための有効なアプローチの1つです。またミクログリアを除去した後に、別のミクログリアに置換することで疾患の治療を目指す研究も行われています。これまでにミクログリアを除去する方法がいくつか報告されており1)、遺伝学的なアプローチと薬理学的なアプローチに大別されます。本記事では、ミクログリア除去の方法とそれぞれの方法の特長について紹介します。
遺伝学的手法
ミクログリアの発生に必要な遺伝子(PU.1、TGF-β、CSF-1Rなど)の変異体は、ミクログリア欠失モデルとして扱われてきました。近年では、ミクログリア特異的にジフテリア毒素の受容体を発現させたトランスジェニックマウスに、ジフテリア毒素を投与することで、選択的にミクログリアを除去する方法が用いられています。ジフテリア毒素は脳血液関門(BBB)を透過するため、腹腔内投与でミクログリアを除去できるというメリットがありますが、ミクログリアを除去できる期間が長くないことが欠点です。
薬理学的手法
薬理学的にミクログリアを除去する手法は、トランスジェニックモデルの作成が不要なため、遺伝学的手法と比べて簡便に実施することができます。ミクログリアを除去することができる化合物は主に以下の3種類が使用されています。
クロドロン酸リポソーム
クロドロン酸を内包したリポソームはミクログリアやマクロファージによって貪食されます。細胞質内に放出されたクロドロン酸はミトコンドリアのADP/ATP輸送酵素を阻害し、細胞死を誘導することでミクログリアを除去します。迅速にミクログリアを除去することが可能である一方で、血液脳関門を透過しないため、直接脳内に注入する必要があります。また炎症サイトカインの誘導などの副作用にも留意が必要です。
CSF-1R阻害剤
CSF-1Rはコロニー刺激因子(CSF1)の受容体で、ミクログリアやマクロファージの生存や増殖、分化に必要です。CSF-1Rを阻害することでミクログリアを除去することができ、これまでにPLX5622、PLX3397などのCSF-1R阻害剤がミクログリアの除去に用いられています。これら阻害剤の特長として、経口投与でミクログリアを除去することができることや、除去の効率が高いことが挙げられます。しかしながら、PLX5622、PLX3397は高価であるため、実験のコストが増加するという欠点があります。また、経口投与の場合は末梢組織にも薬剤効果が想定されるため、留意が必要です。
ガンシクロビル
ガンシクロビル(GCV)はヌクレオチドと構造が類似しており、ウイルス由来のDNAポリメラーゼ/逆転写酵素による基質の取り込みを競合的に阻害することから抗ウイルス剤として使用されています。ガンシクロビルを脳室内注射することでミクログリアを除去することが報告され、ミクログリア除去試薬としても用いられています。血液脳関門を透過せず脳室内への注入が必要であることや、除去できる期間が短いこと、アストロサイトの活性化を誘導することなどいくつかの欠点があるものの、脳境界マクロファージ(BAMs: Borderassociated Macrophages)や循環骨髄細胞には影響を与えないことが知られており、これらの細胞への影響を抑えつつ、ミクログリアを除去したいときに有効な手法とされています。
ミクログリアリムーバー
ミクログリアリムーバーはクロドロン酸を内包したリポソームです。ミクログリアによって貪食されたクロドロン酸リポソームは、細胞内でクロドロン酸を放出します。クロドロン酸はATP類似体としてATP代謝を阻害し、ミクログリアの細胞死を誘導します。リポソームに内包することで、クロドロン酸単体よりもミクログリアに取り込まれやすくしています。実験のコントロールとしてミクログリアリムーバー (コントロール用) (別売、コードNo. 131-19511)も販売しております。
特長
- 投与後、約1-3日でミクログリアを除去することが可能
- 市販のミクログリア除去飼料に比べて安価
アプリケーションデータ
マウス大脳皮質のミクログリア除去
マウス大脳皮質に33Gの注射針を刺入後、1 µLのミクログリアリムーバー(コントロール用)あるいはミクログリアリムーバーを注入し、3日経過後にサンプリングした。
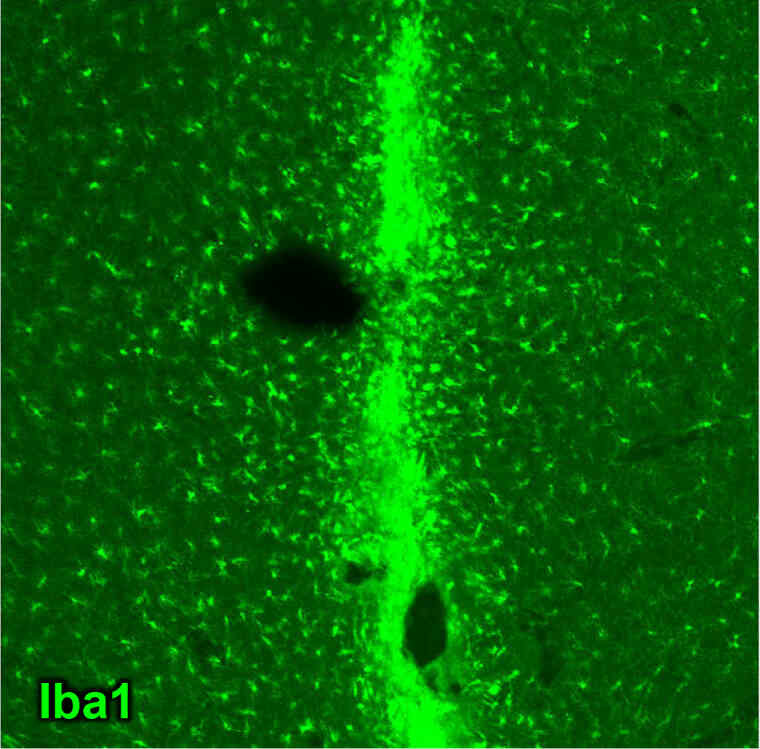
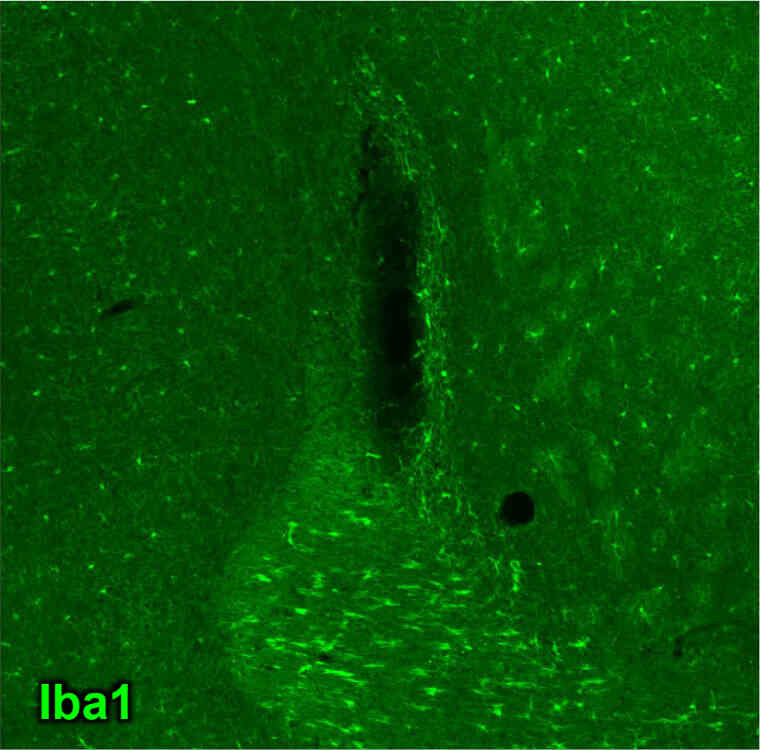
- [結果]
- コントロール群ではミクログリア(もしくはマクロファージ)が損傷部位に多数集積していた。
一方、ミクログリアリムーバー投与群は損傷部位への集積を阻害するとともに、周辺部位におけるミクログリア数が減少あるいは退縮している様子が見られた。
参考文献
- 1) Tahmasebi, F. and Barati, S.: Cell. Mol. Neurobiol., 43(6), 2459(2023).
The Role of Microglial Depletion Approaches in Pathological Condition of CNS
製品一覧
- 項目をすべて開く
- 項目をすべて閉じる
- 掲載内容は本記事掲載時点の情報です。仕様変更などにより製品内容と実際のイメージが異なる場合があります。
- 掲載されている製品について
- 【試薬】
- 試験・研究の目的のみに使用されるものであり、「医薬品」、「食品」、「家庭用品」などとしては使用できません。
- 試験研究用以外にご使用された場合、いかなる保証も致しかねます。試験研究用以外の用途や原料にご使用希望の場合、弊社営業部門にお問合せください。
- 【医薬品原料】
- 製造専用医薬品及び医薬品添加物などを医薬品等の製造原料として製造業者向けに販売しています。製造専用医薬品(製品名に製造専用の表示があるもの)のご購入には、確認書が必要です。
- 表示している希望納入価格は「本体価格のみ」で消費税等は含まれておりません。
- 表示している希望納入価格は本記事掲載時点の価格です。



