膨張顕微鏡法標本作製キット

細胞内には複数のオルガネラが存在し、それぞれのオルガネラの構造を解析することが細胞機能の理解や疾病のメカニズム解明において重要となります。細胞内のオルガネラの構造を高解像度にイメージングするためには、高価な電子顕微鏡や超解像顕微鏡が必要です。一方で蛍光顕微鏡では、アッベの回折限界によりオルガネラの構造を詳細に解析することは困難です。そこで蛍光顕微鏡でオルガネラを観察するための手法の一つとして2015年にExpansion Microscopy法が開発されました。Expansion Microscopy法は吸水性ゲルを利用してサンプル自体を大きくする技術であり、蛍光顕微鏡では困難であった微小な構造のイメージングが可能となります。
本製品は、Expansion Microscopy法を行うためのゲル作成に必要な試薬および枠を同梱したキットであり、細胞を3次元的に約4倍まで膨張することが可能です。
製品概要
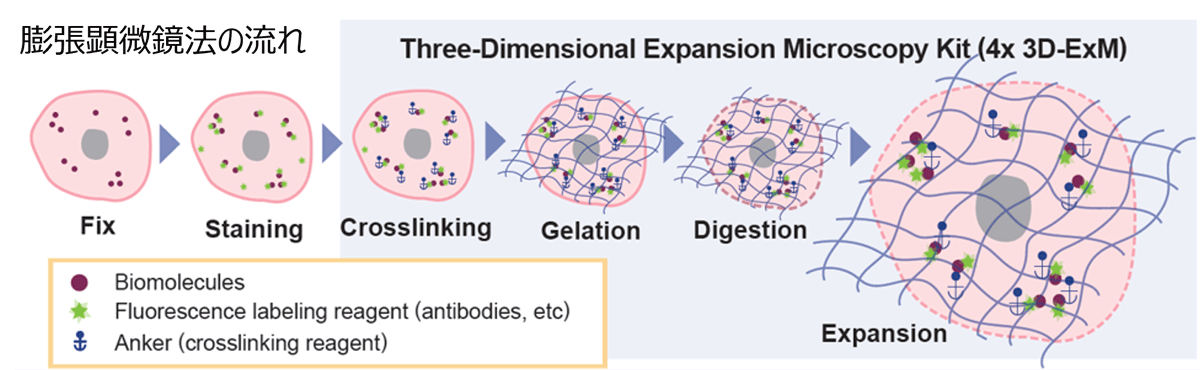
膨張顕微鏡法 (Expansion Microscopy:ExM) とは
細胞内には複数のオルガネラが存在し、それぞれのオルガネラの構造を解析することが細胞機能の理解や疾病のメカニズム解明において重要となります。細胞内のオルガネラの構造を高解像度にイメージングするためには、高価な電子顕微鏡や超解像顕微鏡が必要です。一方で蛍光顕微鏡では、アッベの回折限界によりオルガネラの構造を詳細に解析することは困難です。そこで蛍光顕微鏡でオルガネラを観察するための手法の一つとして2015年にExpansion Microscopy法が開発されました。Expansion Microscopy法は吸水性ゲルを利用してサンプル自体を大きくする技術であり、蛍光顕微鏡では困難であった微小な構造のイメージングが可能となります。
本製品は、Expansion Microscopy法を行うためのゲル作成に必要な試薬および枠を同梱したキットであり、細胞を3次元的に約4倍まで膨張することが可能です。
参考文献 : F. Chen, PW. Tillberg, Science., 2015, 347 (6221): 543–548.
Norman, et.al. Journal of Cell Biology., 2025, 224 (2): e202407116.
This product is covered by U.S. Patent Application No. 17/466,434
his technology is based on research conducted by Dr. Aussie Suzuki at the University of Wisconsin–Madison.
特長
- 細胞を3次元的に約4倍拡大できる
- ゲル作成から膨張までの試薬がオールインワン
- 細胞の微細構造を光学顕微鏡でイメージングできる
使用方法
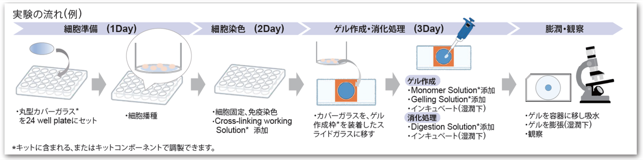
実験の流れ
キットには、実験に必要な試薬が含まれております。細胞の準備からゲルの作成、観察までを詳細に記載したプロトコルを準備しており、はじめてでも安心して実験できます。
【ご注意】
- より詳細な観察をする場合は、水浸レンズの使用を推奨します。
よくある質問:観察時の顕微鏡/レンズについて注意点を教えてください をご参照ください。 - 細胞の染色試薬類 (核染色剤等) はキットに含まれておりません。
使用方法
取扱説明書と撮像マニュアルは下記をご覧ください。
取扱説明書 操作7 :Cover Glassをゲル作成枠 (Mold円内) に移す
取扱説明書 操作16. Moldを取り外し、ゲルを10 cm dishに入れる
取扱説明書 操作.19 ゲルを傷つけないように注意しながら超純水を除去する
データ例
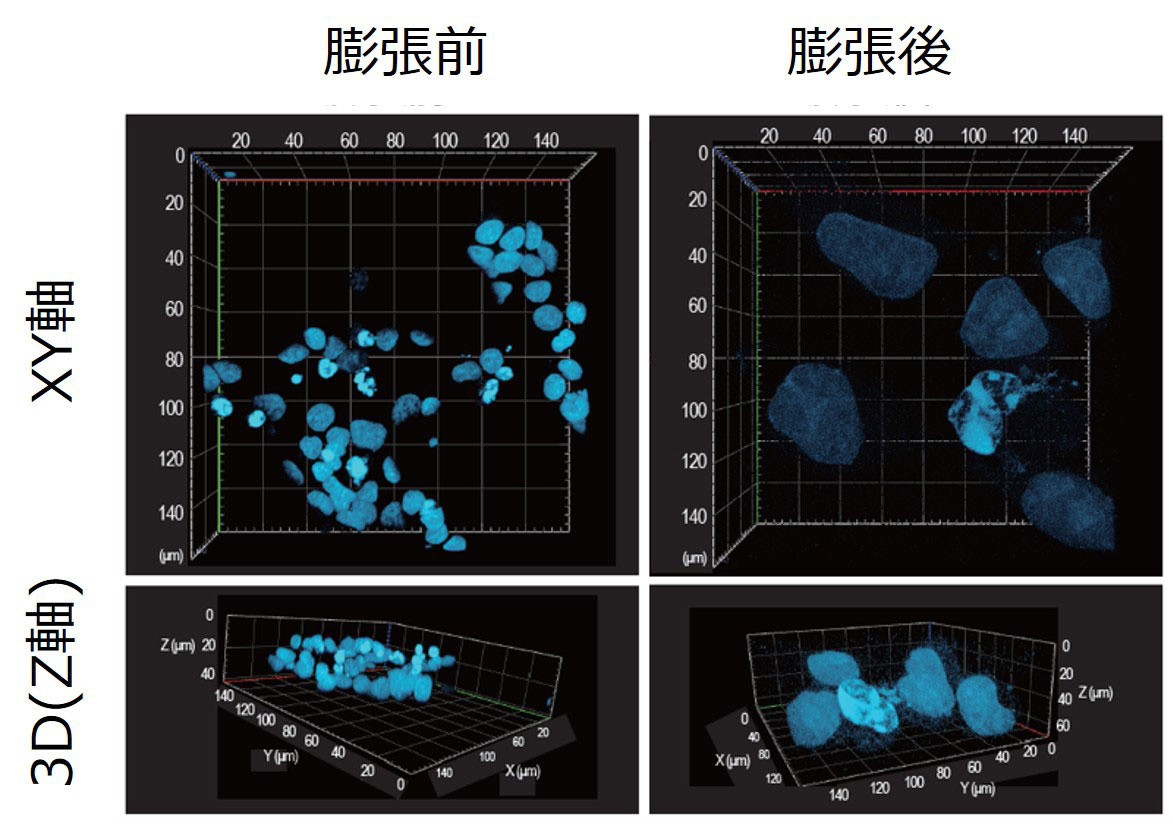
細胞を3次元的に約4倍に拡大
HeLa細胞の核をDAPIで染色し、本キットを用いて膨張顕微鏡法による観察を行いました。
ゲルの大きさと染色した核を膨張の指標として膨張倍率を確認した結果、XYZ軸それぞれに約4倍膨張することを確認しました。
<ゲルの大きさ>

<核染色>
<検出条件>
検出装置: 共焦点レーザー顕微鏡 Lens 40× Water objective
DAPI (青) : Ex/Em = 405/420-480 nm
膨張前: Laser 1.0%, Gain 550 V
膨張後: Laser 2.5%, Gain 680 V
膨張前後の細胞の解像度・サイズ変化の評価
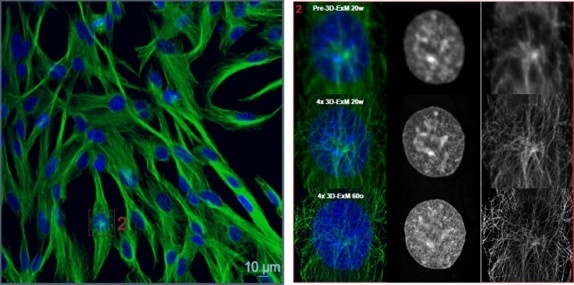
RPE1細胞の核をDAPIで染色後、本キットを用いて細胞を膨張させ、20倍水浸レンズを使用した共焦点顕微鏡で観察しました。同一細胞において、膨張前 (Pre-3D-ExM) と膨張後 (Post-3D-ExM) を比較した結果、膨張後の細胞は解像度が向上し、さらに長軸・短軸の長さおよび面積が約4倍に増大していることを確認しました。

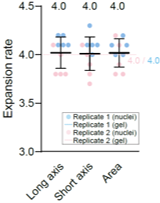
※青枠 (1) 上段、赤枠 (2) 下段は、膨張前後の同一細胞における2つの細胞領域の解像度の変化の例を示しています。
<実験条件>
細胞:RPE1 (hTERT-immortalized retinal pigment epithelial cells)
染色: DAPI 30 min
<観察条件>
顕微鏡システム:スピニングディスクコンフォーカル (Yokogawa CSU + Nikon Ti2 stand+ CMOSカメラ)
Imaging conditions: A 20× water-immersion objective was used for both pre- and post-ExM imaging (the same cell was imaged with identical optical settings) .
405 laser: 60% power with 200 msec exposure for ExM
データ提供:Dr. Aussie Suzuki at the University of Wisconsin–Madison
膨張後の核とチューブリンの観察
RPE1細胞の核およびチューブリンを染色した後、本キットを用いて細胞を膨張させました。その後、20倍水浸レンズを用いて共焦点顕微鏡にて観察し、さらに同一の細胞を60倍油浸レンズでも観察しました。その結果、核および細胞骨格の詳細な形態を確認できました。
<実験条件>
細胞: RPE1 (hTERT-immortalized retinal pigment epithelial cells)
染色:
一次抗体 anti-alpha-Tubulin (DM1A), 1 hour
ニ次抗体 Alexa488 conjugated anti-mouse-IgG, 1 hour
DAPI, 30 min
<観察条件>
顕微鏡システム:スピニングディスクコンフォーカル (Yokogawa CSU + Nikon Ti2 stand+ CMOSカメラ)
Imaging conditions: A 20× water-immersion objective was used for both pre- and post-ExM imaging (the same cell was imaged with identical optical settings) . The same cell was also imaged using a 60× oil-immersion objective to obtain higher-resolution images.
405 laser: 60% power with 200 msec exposure for ExM
488 laser: 60% power with 200 msec exposure for ExM
データ提供:Dr. Aussie Suzuki at the University of Wisconsin–Madison
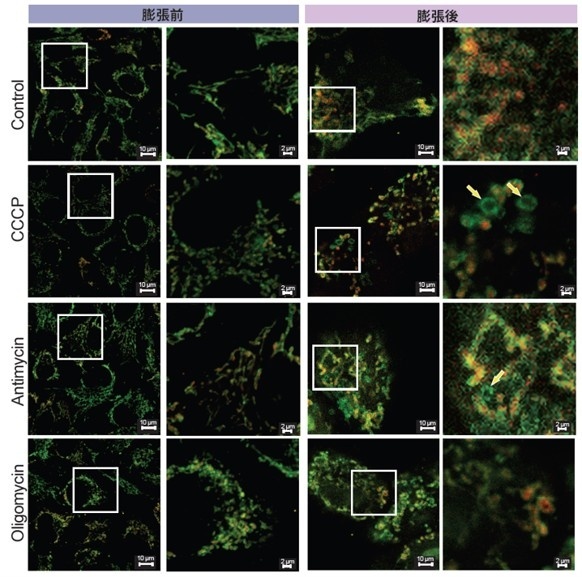
薬剤処理毎のミトコンドリア形態変化の観察
脱分極剤であるCCCP、複合体III阻害剤であるアンチマイシンおよび、ATP合成酵素阻害剤であるオリゴマイシンで処理したHeLa細胞のミトコンドリアの外膜 (TOM20) 、および内膜 (COX IV) を染色し、本キットを用いて膨張顕微鏡法により観察しました。その結果、膨張前の細胞では、ミトコンドリアの分裂は確認できるものの外膜と内膜の判別が困難でした。一方で、膨張後の細胞では、ミトコンドリア膜電位を脱分極させるCCCPおよびアンチマイシン処理では、外膜がリング状 (ミトコンドリア分裂) を示し、内部に内膜タンパク質COX IVが存在しない構造 (黄色矢印) が観察されました。さらに膜電位を脱分極させないオリゴマイシン処理では、分裂したミトコンドリア内部にCOX IVが観察されました。本キットを用いることで、ミトコンドリア分裂時の内膜の変化まで観察することができました。
<実験条件>
CCCP : 10 μmol/L 30 min処理
Antimycin: 10 μmol/L 30 min処理
Oligomycin: 10 μmol/L 30 min処理
<検出条件>
検出装置:共焦点レーザー顕微鏡 (Zeiss LSM800)
TOM20 (緑) : Ex/Em = 488/500 - 550 nm
COX IV (赤) : Ex/Em = 561/580 - 620 nm
膨張前
Lens: 63× Oil objective
TOM20: Laser 1.0 %, Gain 650 V
COX IV: Laser 2.0 %, Gain 650 V
膨張後
Lens: 63× Oil objective
TOM20: Laser 70 %, Gain 700 V
COX IV: Laser 70 %, Gain 750 V
FAQ
同仁化学研究所メーカーホームページよりご覧いただけます。
製品一覧
- 項目をすべて開く
- 項目をすべて閉じる
膨張顕微鏡法標本作製キット
【本サイト掲載情報について】
- 掲載内容は本記事掲載時点の情報です。仕様変更などにより製品内容と実際のイメージが異なる場合があります。
- 掲載されている製品について
- 【試薬】
- 試験・研究の目的のみに使用されるものであり、「医薬品」、「食品」、「家庭用品」などとしては使用できません。
- 試験研究用以外にご使用された場合、いかなる保証も致しかねます。試験研究用以外の用途や原料にご使用希望の場合、弊社営業部門にお問合せください。
- 【医薬品原料】
- 製造専用医薬品及び医薬品添加物などを医薬品等の製造原料として製造業者向けに販売しています。製造専用医薬品(製品名に製造専用の表示があるもの)のご購入には、確認書が必要です。
- 表示している希望納入価格は「本体価格のみ」で消費税等は含まれておりません。
- 表示している希望納入価格は本記事掲載時点の価格です。



