電解液
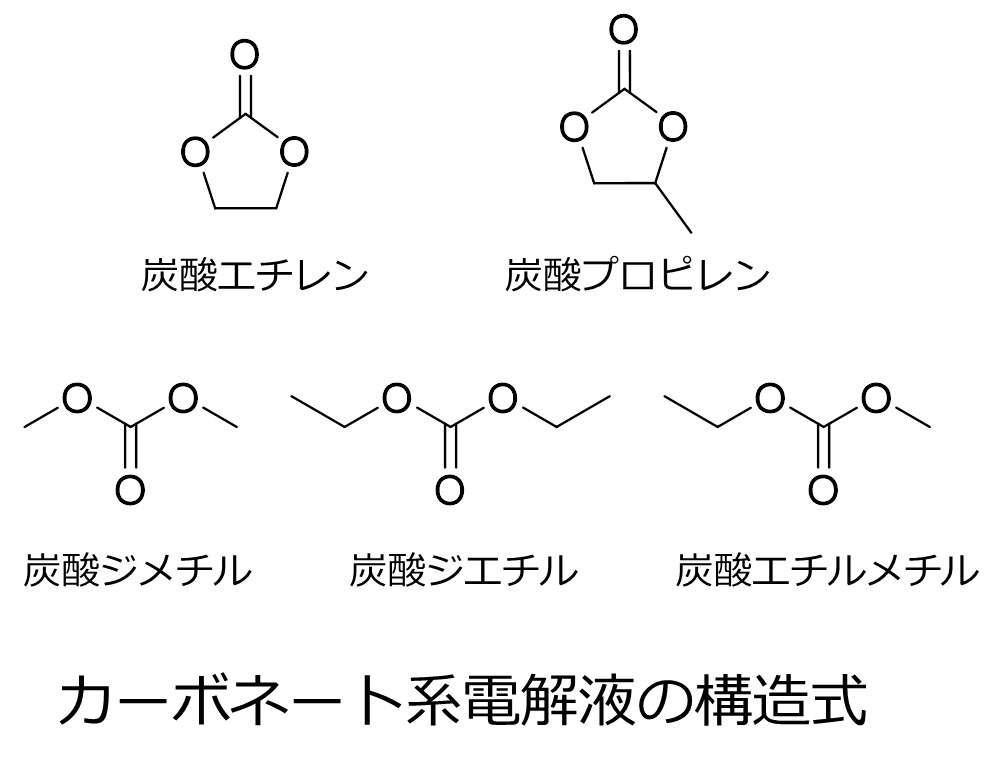
リチウムイオン電池 (LIB) の電解液は、正極負極間のリチウムイオン移動を媒介しています。LIBは約4 Vと高い作動電圧をもつため、電解液にはその電圧でも分解しない広い電位窓をもつこと、また高いイオン伝導度を示すことなどの条件が求められます。水系電解液は1.2 Vほどで電気分解されてしまうため、LIBでは有機溶媒が電解液として使用されています。代表的な有機溶媒としては炭酸エチレン、炭酸プロピレンなどの環状カーボネートがあげられます。環状カーボネートは粘度が高くイオン伝導度の点で不利なため、炭酸ジメチル、炭酸ジエチル、炭酸エチルメチルなどの鎖状カーボネートと混合して使用することが一般的です。また、電解液に重水素化体を混合し充放電後の分解物を分析することで電池内での電解液の挙動確認することができます。
しかし、これらの有機溶媒は燃えやすく安全性に懸念があるため、近年では難燃性のイオン液体や固体電解質を用いたLIBの開発が行われています1-4)。
SEIの形成
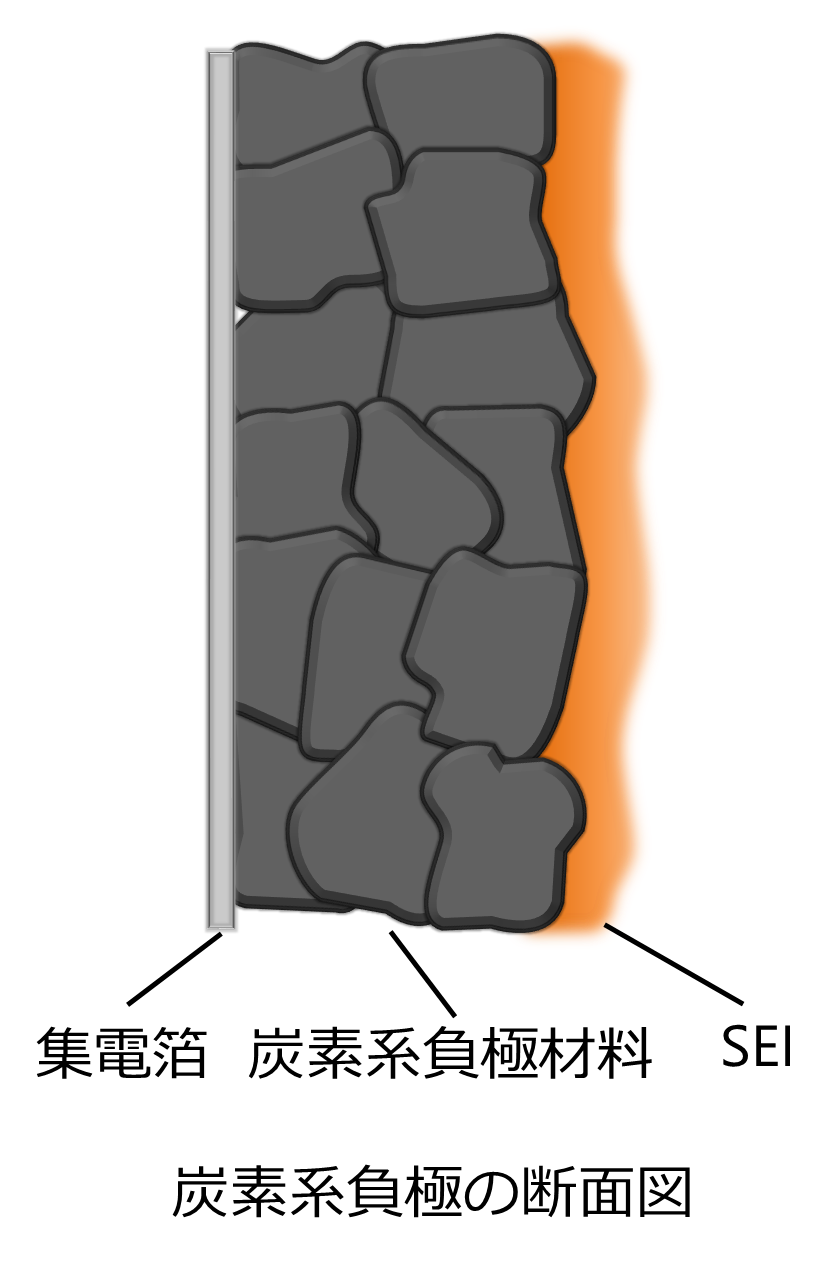
LIBでは炭素系材料が負極材料として一般的に使用されています。充電時、負極の電位は0.1~0.2 V vs Li+/Liになり、非常に強い還元力を示します。この電位では、電解液として使用されている有機溶媒も分解されます。しかし、この分解による生成物が負極表面に堆積し、固体電解質界面(solid-electrolyte interphase、SEI)と呼ばれる薄膜を形成します5)。
SEIはリチウムイオン伝導性でありながら電子絶縁性であるため、電解液のそれ以上の分解を防ぎながら充放電を可能にしています。炭素系材料を負極とするリチウムイオン電池にとって非常に重要な役割を果たすSEIですが、SEIが薄すぎると電解液の分解は止まらず、厚すぎると内部抵抗の上昇につながり、またSEIの形成にはリチウムイオンを消費するため、SEIを安定に制御することが求められています。
参考文献
- Sakaebe, H.and Matsumoto, H.:Electrochem. Commun., 5, 594 (2003).
- Lombardo, L., Brutti, S., Navarra, M. A., Panero, S. and Reale, P.:J. Power Sources, 227, 8 (2013).
- Seino, Y., Ota, T., Takada, K., Hayashi, A. and Tatsumisago, M.:Energy Environ. Sci., 7, 627 (2014).
- Ramakumar, S., Deviannapoorani, C., Dhivya, L., Lakshmi S.S. and Murugan, R.:Prog. Mater. Sci., 88, 325 (2017).
- Peled, E.:J. Electrochem. Soc., 126, 2047 (1979).
製品一覧
- 項目をすべて開く
- 項目をすべて閉じる
カーボネート系電解液
重水素化カーボネート系電解液
イオン液体電解液WILシリーズ
- 掲載内容は本記事掲載時点の情報です。仕様変更などにより製品内容と実際のイメージが異なる場合があります。
- 掲載されている製品について
- 【試薬】
- 試験・研究の目的のみに使用されるものであり、「医薬品」、「食品」、「家庭用品」などとしては使用できません。
- 試験研究用以外にご使用された場合、いかなる保証も致しかねます。試験研究用以外の用途や原料にご使用希望の場合、弊社営業部門にお問合せください。
- 【医薬品原料】
- 製造専用医薬品及び医薬品添加物などを医薬品等の製造原料として製造業者向けに販売しています。製造専用医薬品(製品名に製造専用の表示があるもの)のご購入には、確認書が必要です。
- 表示している希望納入価格は「本体価格のみ」で消費税等は含まれておりません。
- 表示している希望納入価格は本記事掲載時点の価格です。



