ボロン酸
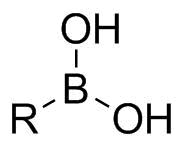
ボロン酸(R-B(OH)2)は、空気や水に安定で取り扱いやすい上に、副生物の除去も容易で毒性・環境負荷なども低いなど優れた特長を併せ持ちます。
鈴木-宮浦カップリングは、天然物全合成から医薬品・有機電子材料の探索・生産に多数応用され、実験室レベルから工業スケールに至るまで、今やなくてはならない試薬です。
本記事はWEBに混在する化学情報をまとめ、それを整理、提供する化学ポータルサイト「Chem-Station」の協力のもと、ご提供しています。
Chem-Stationについて
反応機構
通常炭素-ホウ素結合は強く(有機ホウ素化合物は安定)、そのままではトランスメタル化は起こらない。当量以上の塩基を加え、トランスメタル化活性なボレート型にしてやる必要がある。それゆえ塩基性条件下に不安定な化合物には用いることが難しいという欠点もある。
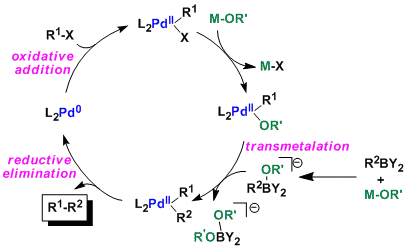
反応例
近年のクロスカップリングの進歩はめざましく、低反応性のアリールクロライドも反応に用いることができるようになった 1, 2)。
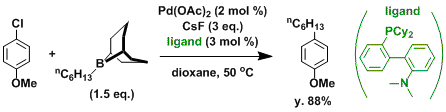
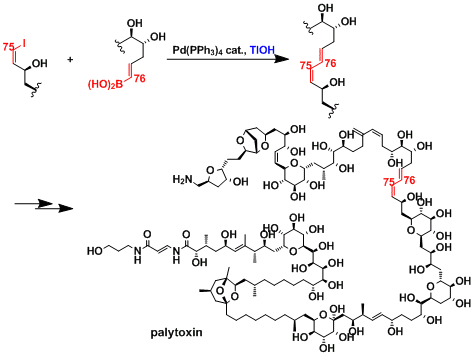
本反応の高い官能基選択性を活かし、Palytoxinの全合成が達成されている。分子量が巨大になるほど反応点同士の接近確率が低くなるため、一般にクロスカップリング反応は困難になる。本合成において岸らは、水酸化タリウムを塩基として加えることで劇的に反応性が向上されることを見出している 3)。
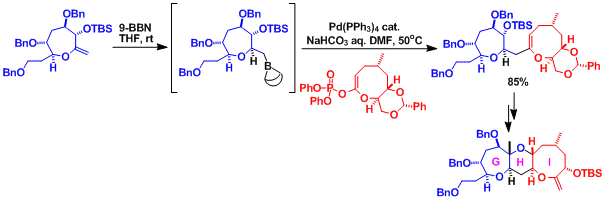
Ciguatoxinの合成研究 4)
三環性化合物の収束的合成にB-アルキル鈴木クロスカップリングが用いられている。 相方のエノールホスフェートはエノールトリフラートに比べ安定性の面で優れている。
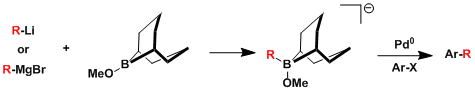
有機ホウ素化合物を経由しない鈴木クロスカップリング
9-BBN-OMeと任意の有機リチウム試薬/Grignard試薬の反応によりボレートを前調製し、鈴木カップリングを行う手法。特にメチル・アルキニル基の場合、ハイドロボレーションで試剤が調製できないため、本法の有用性が高い。
2級アルキルハライドとの鈴木カップリング 5)
通常酸化的付加後の金属-アルキル中間体はβ水素脱離によって速やかに分解する。2級アルキルハライドの場合にはそれが顕著であり、これまでに成功例はなかった。FuらはNi触媒と配位子の膨大なスクリーニングの結果、この困難なカップリング反応を実現させている。
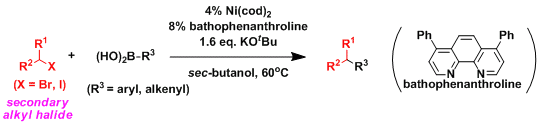
有機トリフルオロボレート塩は空気・水に安定な結晶性化合物である。ボロン酸と比して、当量調節・精製が容易という利点がある。近年ではこれをクロスカップリングパートナーとして用いる研究がなされている 6)。環状トリオールボレート塩 7)も同様の目的に使用可能であることが報告されている。

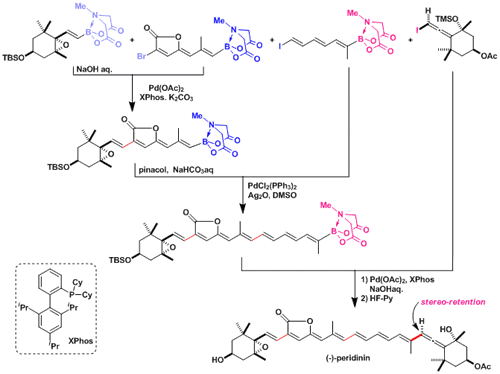
反復型鈴木クロスカップリング戦略によるPeridinineの合成 8)
ここで用いられているMIDAボロネートは保護型有機ボロン酸として現在もっとも先進的な位置づけにある。
鉄触媒を用いた鈴木ー宮浦カップリング反応 10)
①かさ高いジホスフィンリガンドと塩化鉄(II)を錯形成させ、高スピン錯体を生成させる②ボレート形成目的に有機金属種を用いる③添加剤としてMg(II)塩を加えることで、鉄触媒を用いた鈴木ー宮浦クロスカップリング反応を実現している。

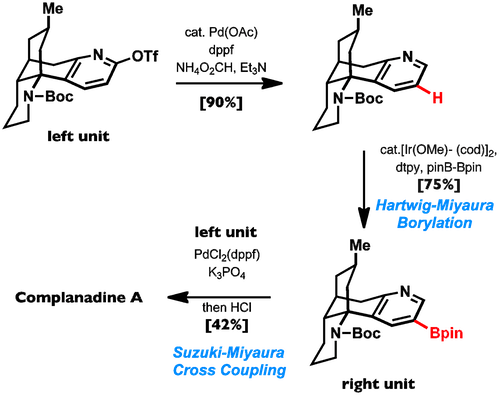
コンプラナジンAの全合成
直接的なボリル化反応(Hartwing-Miyauraボリル化反応)と鈴木ー宮浦クロスカップリング反応を組み合わせて炭素ー炭素結合を構築している。
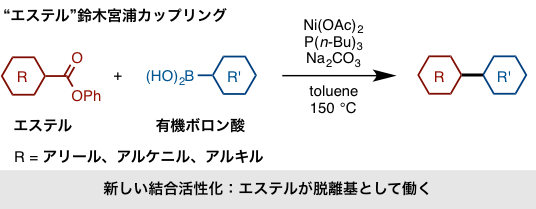
エステルを使った鈴木ー宮浦型クロスカップリング反応 12)
ニッケル触媒を用いることでエステルと有機ボロン酸とのカップリング反応を実現。この反応以前にもエノールおよびフェノール誘導体を用いた鈴木ー宮浦クロスカップリング型反応が知られている。
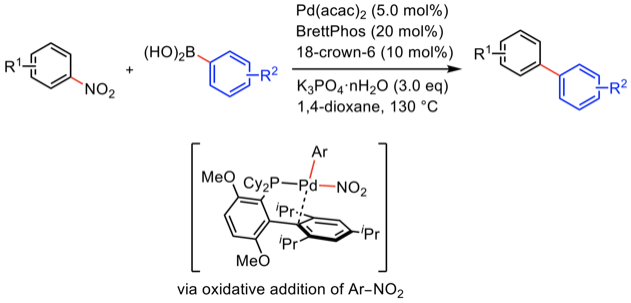
芳香族ニトロ化合物のクロスカップリング反応 13)
芳香族ニトロ化合物を求電子剤として用いる鈴木–宮浦カップリング反応。この反応の鍵過程は、Ar–NO2結合の酸化的付加である。通常、ニトロ化合物と低原子価金属種との反応では、ニトロ基の還元が進行し、ニトロソ化合物やアニリン類が生じるが、BrettPhos-Pd(0)がAr–NO2結合の酸化的付加に極めて有効であり、望みのビアリールカップリング反応が進行する。
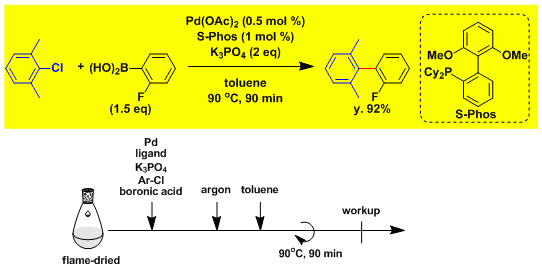
実験手順
アリールクロライドを用いる鈴木-宮浦クロスカップリング 9)
実験のコツ・テクニック
0価のパラジウムは酸素によって失活するため、アルゴンor窒素雰囲気下に反応を行う。基質によっては、溶媒の凍結脱気も必要。
参考文献
- Fu, G. C. et al.: Angew. Chem. Int. Ed., 37, 3387 (1999).
- Buchwald, S. L. et al.: J. Am. Chem. Soc., 121, 9550 (1999). DOI: 10.1021/ja992130h
- Kishi, Y. et al.: J. Am. Chem. Soc., 111, 7530 (1989).; ibid., 116, 11205 (1994).
- Sasaki,M. and Tachibana, K. et al.: Angew. Chem. Int. Ed., 40, 1090 (2001).
- Fu, G. C. et al.: J. Am. Chem. Soc., 126, 1340 (2004). DOI: 10.1021/ja039889k
- (a) Stefani, H. A. et al.: Tetrahedron, 63, 3623 (2007). doi:10.1016/j.tet.2007.01.061
(b) Molandar, G. A. et al.: Aldrichimica Acta, 38, 49 (2005).
(c) Lennox, A. J. J. and Lloyd-Jones, G. C.: Angew. Chem. Int. Ed., 51, 9385 (2012). DOI: 10.1002/anie.201203930 - (a) Yamamoto, Y., Takizaha, M., Yu, X.-Q. and Miyaura, N.: Angew. Chem. Int. Ed., 47, 928 (2008). doi:10.1002/anie.200704162
(b) Yamamoto,Y.: Heterocycles, 85, 799 –819 (2012). DOI: 10.3987/REV-12-728 - Woerly, E. M., Cherney, A. H., Davis, E. K. and Burke, M. D.: J. Am. Chem. Soc., 132, 6941 (2010). doi: 10.1021/ja102721p
- Altman, R. A. and Buchwald, S. L.: Nature Protocols, 2, 3115 (2007). doi:10.1038/nprot.2007.411
- Hatakeyama,T., Hashimoto, T., Kondo, Y., Fujiwara, Y., Seike,H., Takaya, H., Tamada, Y., Ono, T. and Nakamura, M.: J. Am. Chem. Soc., 132, 10674 (2010). doi:10.1021/ja103973a
- Fischer, D.F. and Sarpong, R.: J. Am. Chem. Soc., 132, 5926 (2010). DOI: 10.1021/ja101893b
- Muto, K., Yamaguchi, J., Musaev. D. G. and Itami, K.: Nature Commun, 6, 7508 (2015). DOI: 10.1038/ncomms8508
- (a) Rosen, B. M., Quasdorf, K. W., Wilson, D. A., Zhang, N., Resmerita, A.-M., Garg, N. K. and Percec, V.: Chem. Rev., 111, 1346 (2011). DOI: 10.1021/cr100259t
(b) Jana, R., Pathak, T. P. and Sigman, M. S.: Chem. Rev., 111, 1417 (2011). DOI: 10.1021/cr100327p - Yadav, M. R., Nagaoka, M., Kashihara, M., Zhong, R.-L., Miyazaki, T., Sakaki, S. and Nakao Y.: J. Am. Chem. Soc., 139, 9423 (2017). DOI: 10.1021/jacs.7b03159
製品一覧
- 項目をすべて開く
- 項目をすべて閉じる
- 掲載内容は本記事掲載時点の情報です。仕様変更などにより製品内容と実際のイメージが異なる場合があります。
- 掲載されている製品について
- 【試薬】
- 試験・研究の目的のみに使用されるものであり、「医薬品」、「食品」、「家庭用品」などとしては使用できません。
- 試験研究用以外にご使用された場合、いかなる保証も致しかねます。試験研究用以外の用途や原料にご使用希望の場合、弊社営業部門にお問合せください。
- 【医薬品原料】
- 製造専用医薬品及び医薬品添加物などを医薬品等の製造原料として製造業者向けに販売しています。製造専用医薬品(製品名に製造専用の表示があるもの)のご購入には、確認書が必要です。
- 表示している希望納入価格は「本体価格のみ」で消費税等は含まれておりません。
- 表示している希望納入価格は本記事掲載時点の価格です。



