F-PDX® (患者由来腫瘍異種移植片) を用いたin vitro ( ex vivo ) 試験受託サービス

F-PDX® (患者由来腫瘍異種移植片) を用いたin vitro ( ex vivo ) 試験受託サービス

担がん動物 Fukushima Patient Derived Tumor Xenograft (福島PDX® / F-PDX®) は、福島医薬品関連産業支援拠点化事業により樹立されたPDXです。福島事業独自の基準で管理されており、元の腫瘍の病理組織や遺伝子発現の特徴を維持されています。
免疫不全マウスに移植して抗がん剤などの薬効評価を in vivo で行うことが可能です。また、免疫不全マウスに移植せず、そのまま薬効評価を行う ex vivo 試験を行うことも可能です。
臨床試験前に F-PDX® を使用した薬効評価を行うことで、新薬候補のドロップアウトのリスクを低減できる可能性があります。
F-PDX® (Fukushima Patient-derived tumor Xenograft) とは – 福島県立医科大学 高木 基樹 教授
ヒトがん細胞株は、世界初の株化細胞 (安定して増殖を繰り返す細胞) としてHeLa細胞が樹立されてから多くのがん細胞株が作製され、がんの生物学や抗がん剤の評価などで幅広く研究に使用されてきた。しかしながら、これらのがん細胞株は長期間の培養による増殖を繰り返したため、ゲノム配列や遺伝子発現に変化が生じ、がん組織の特徴を維持していない細胞がほとんどである。これらのがん細胞株を用いた皮下異種移植腫瘍動物モデルが抗がん剤の評価等で広く使用されてきたが、抗がん剤の臨床での薬効と一致しないことが知られており、がん細胞株で評価された抗がん剤の85%程度が臨床試験において予想された薬効を示さないことが報告されている。
そこで、近年、患者由来のがん組織を免疫不全マウスに移植し、がん組織の構造や特徴を正確に反映したpatient-derived xenograft (PDX) モデルが開発された。PDXモデルを用いた抗がん剤の薬効は、臨床試験での薬効と高い相関性を示すことが報告されており、新しい抗がん剤の臨床試験の前に、抗がん剤の効果を予め確認するためにPDXモデルの利用が推進されている。
福島医薬品関連産業支援拠点化事業では、肺、大腸、卵巣、子宮、肉腫や造血器腫瘍等の様々ながん組織からPDXを樹立し、Fukushima (F)-PDX® と名付けた。F-PDX®とは、1) 造血器腫瘍系では2世代以上の継代が可能であること、固形腫瘍系は3世代以上の継代が可能であること、2) 凍結腫瘍組織の再生着を確認したもの、3) 各世代における病理組織学的解析、網羅的遺伝子発現解析、細胞表面抗原発現解析等によって腫瘍の特徴が確認されたもの、である。
F-PDX®の特徴
- 患者腫瘍組織の一部を免疫不全マウスに移植・継代して樹立
- インフォームド・コンセントを取得済み
- 元の腫瘍の病理組織や遺伝子発現の特徴が維持されていることを確認済み
- 多発性骨髄腫を含む多様ながん腫について160系統以上をラインアップ (リストはこちら)
- ゲノム解析データ、移植試験データ、臨床情報などをもとに選択可能
- ヒト感染症が陰性であることを確認済み
- 凍結腫瘍組織として提供可能
F-PDX®で作製した患者由来細胞とがん細胞株の比較
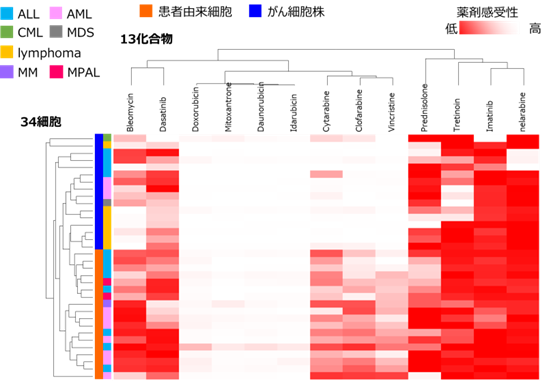
- F-PDX®モデルとがん細胞株の in vitro 評価結果をクラスタ解析できます
- 患者由来細胞とがん細胞株では薬剤感受性のパターンが異なります
受託サービス概要
- 患者腫瘍移植マウスモデル (F-PDX®) を用いて、化合物の in vitro ( ex vivo) アッセイを行います
- 化合物の細胞増殖阻害活性や細胞障害性活性を測定いたします
- 固形腫瘍・造血器腫瘍に対応しています (F-PDX®のリストはこちら)
- F-PDX®の選択、実験条件 (化合物の濃度、化合物の作用時間、アッセイまでの時間など) はお客様とご相談の上、ご要望に可能な限り対応いたします
- お客様が興味を持っているマーカー (遺伝子発現・変異) を確認した上で試験に用いるF-PDX®を選択可能です
- FFPE切片を用いて、免疫染色による標的タンパク質の発現を確認後、試験に用いる細胞株を選択できます
- お客様から調べてほしい候補化合物を提供いただき、それらを作用させて感受性試験を行います
- 化合物以外の中分子、抗体、ウイルス液、細胞等のあらゆるモダリティーに対応いたします
- PDX試験を行うよりも安価かつ動物の個体差なく試験可能です
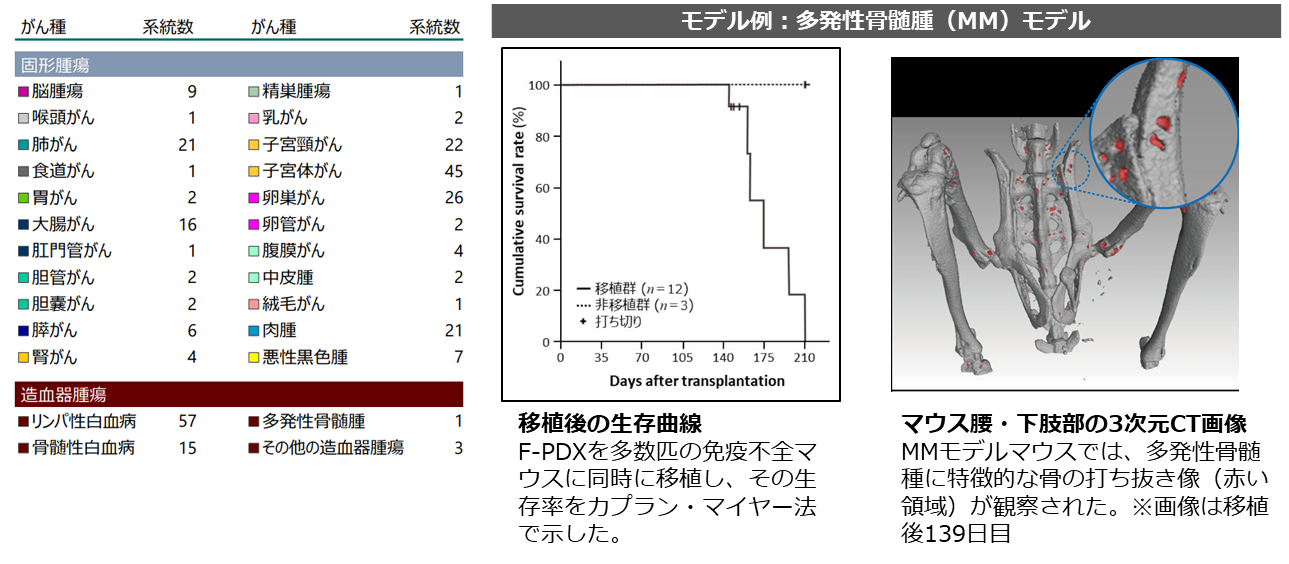
がん種および系統数、モデル例
リストはこちら
F-PDX®由来固形腫瘍の in vitro 評価系
- 動物モデルで評価する前に、免疫不全マウスで増殖した固形腫瘍細胞 (F-PDX®由来細胞) を用いて in vitro アッセイを行います
- 様々な患者由来固形腫瘍細胞を用いて、低コストかつ短時間で抗がん剤の薬効評価が可能です (F-PDX®のリストはこちら)
- 細胞増殖阻害試験や細胞障害性試験を行うことが可能です
-
細胞 F-PDX®マウスから作製した凍結腫瘍組織 被験物質 抗がん剤8種 (公比3, 20 µMから10濃度, n=3) -
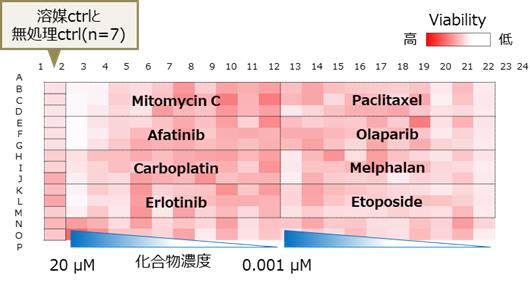
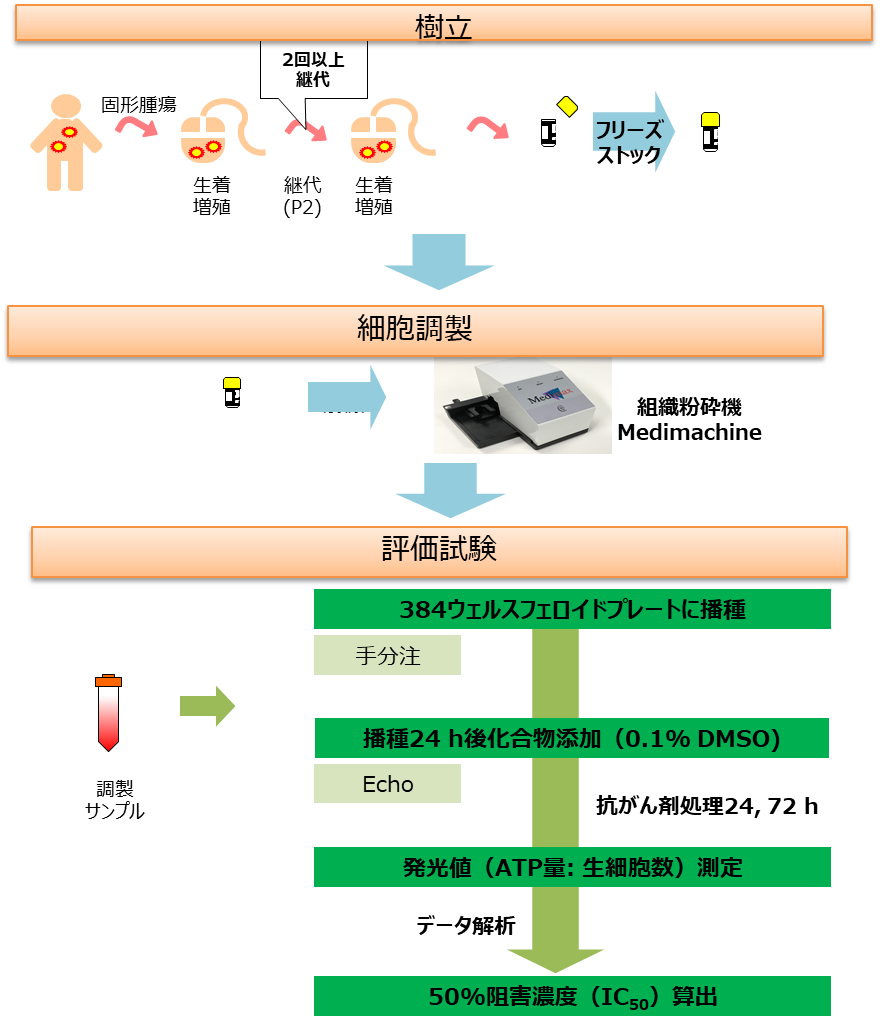
F-PDX® (卵巣がん) を用いた抗がん剤評価
処理 72 h後
| 希釈倍率 | 5 | |||
|---|---|---|---|---|
| アッセイプレート | 384ウェル スフェロイド | |||
| 0 h | 24 h | 72 h | ||
| 発光値 | 2,333,726 | 2,136,794 | 1,175,004 | |
| CV値 | 20.7% | 22.3% | 8.4% | |
| 細胞増殖 | 1日後 | 3日間 | ||
| 0.92 | 0.5 | |||
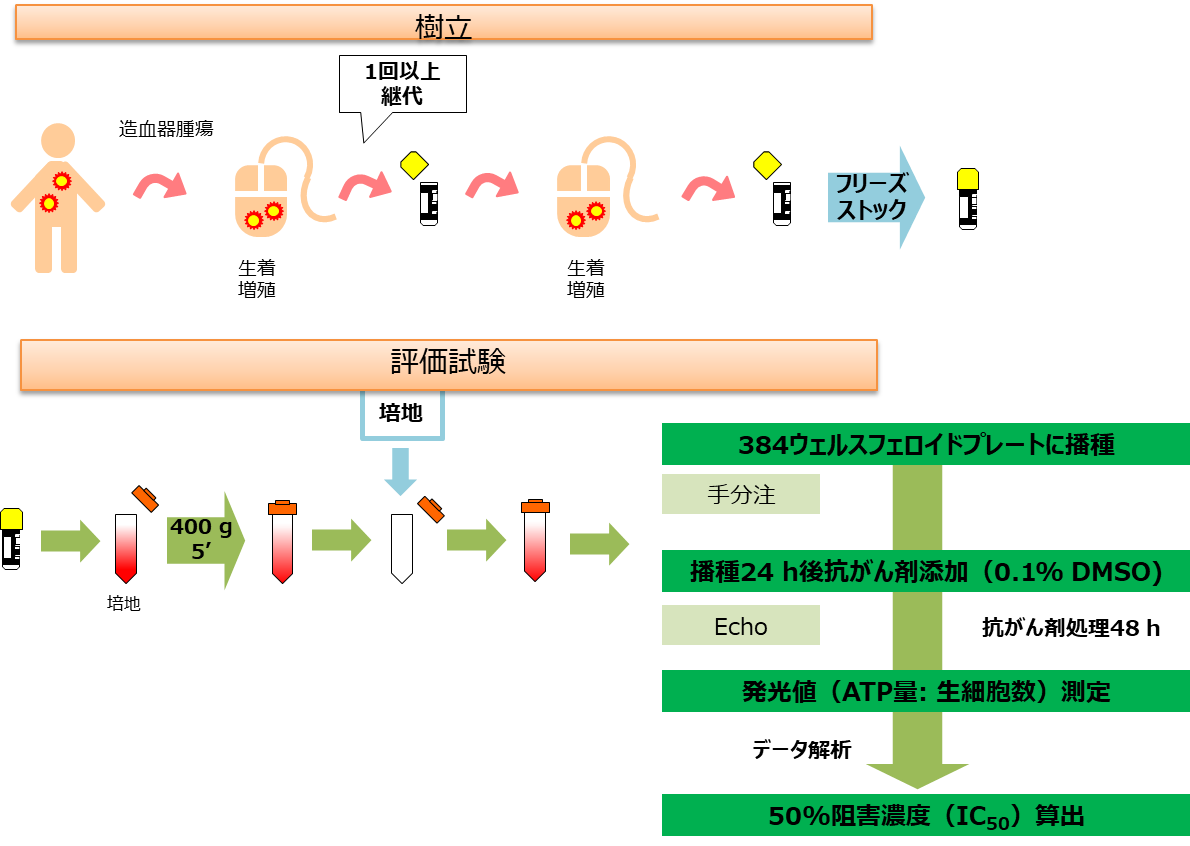
F-PDX®で作製した造血器腫瘍由来細胞のin vitro ( ex vivo ) 評価
- 動物モデルで評価する前に、免疫不全マウスで増殖した造血器腫瘍細胞 (F-PDX®由来細胞) を用いて in vitro アッセイを行います
- 様々な患者由来造血器腫瘍細胞を用いて、低コストかつ短時間で抗がん剤の薬効評価が可能です
- 細胞増殖阻害試験や細胞障害性試験を行うことが可能です
- 急性リンパ性白血病由来細胞 (ALL)、急性骨髄性白血病由来細胞 (AML)、多発性骨髄腫を用いてアッセイが可能です (F-PDX®のリストはこちら)
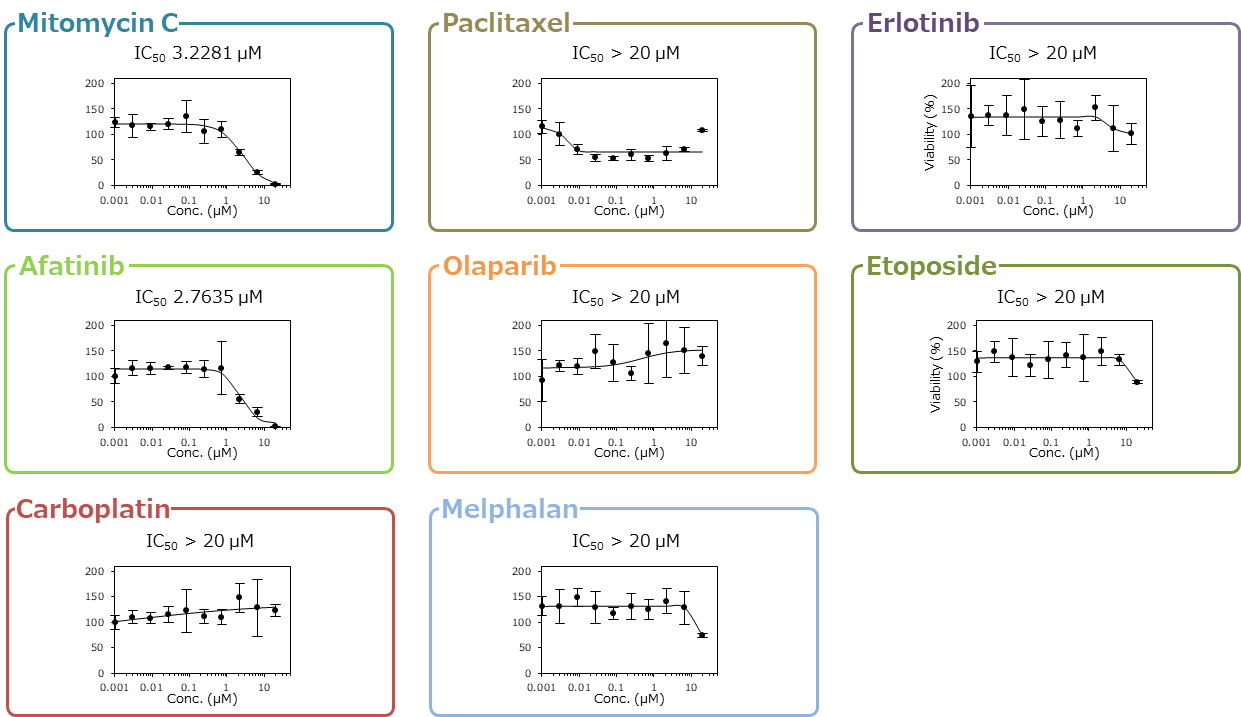
F-PDX®で作製したALL患者由来細胞の in vitro 評価
高い精度と再現性で抗がん剤の細胞増殖阻害活性が測定可能です

F-PDX®で作製したAML患者由来細胞の in vitro 評価
高い精度と再現性で抗がん剤の細胞増殖阻害活性が測定可能です

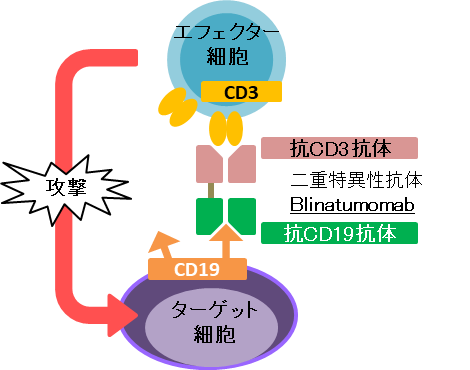
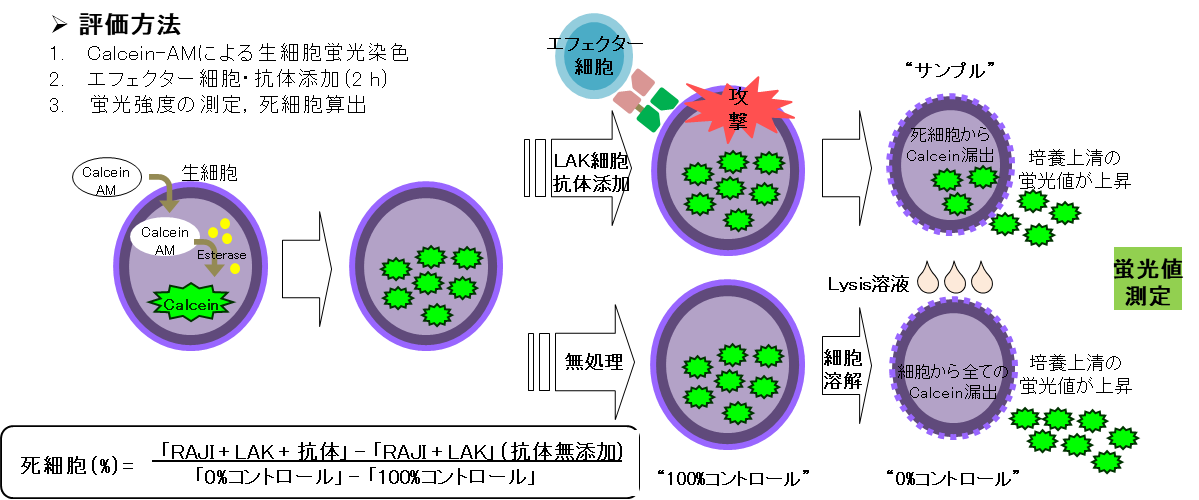
二重特異性抗体とT-LAK細胞を用いたF-PDX®造血器腫瘍の評価
- 細胞:F-PDX®造血器腫瘍4種
- 抗体:Blinatumomab (BLINCYTO)
- 公比10、最高濃度10nM、n=3、処理2時間
- T-LAK細胞:抗CD3抗体で固相化したフラスコとIL-2を含む培地を用いてPBMCを16日間培養後、フリーズストックを作製、アッセイ2日前に解凍
- 染色試薬:Calcein-AM :Promo Cell (DMSO 0.25%)
価格・納期
ご希望の試験内容に応じて変動します。
詳しくはお問い合わせください。
参考資料、文献等、その他
お見積り・ご注文について
- 掲載内容は本記事掲載時点の情報です。仕様変更などにより製品内容と実際のイメージが異なる場合があります。
- 掲載されている製品について
- 【試薬】
- 試験・研究の目的のみに使用されるものであり、「医薬品」、「食品」、「家庭用品」などとしては使用できません。
- 試験研究用以外にご使用された場合、いかなる保証も致しかねます。試験研究用以外の用途や原料にご使用希望の場合、弊社営業部門にお問合せください。
- 【医薬品原料】
- 製造専用医薬品及び医薬品添加物などを医薬品等の製造原料として製造業者向けに販売しています。製造専用医薬品(製品名に製造専用の表示があるもの)のご購入には、確認書が必要です。
- 表示している希望納入価格は「本体価格のみ」で消費税等は含まれておりません。
- 表示している希望納入価格は本記事掲載時点の価格です。



