DDS・医薬品・再生医療の研究開発に
ニッピ 低エンドトキシン 局方精製ゼラチン(製造専用)
ニッピ社の低エンドトキシンゼラチンは従来のゼラチンに比べて、大幅にエンドトキシンを低減させています。エンドトキシンと強く反応する免疫系に対して不活性です。日本薬局方「精製ゼラチン」規格に適合し、メディゼラチンは注射用の賦形剤として実績があります。
スポンジやパウダー状等のご希望の形状や、架橋による物性強度の調製を行った上でのご提供も可能です(詳細お問合せください)。
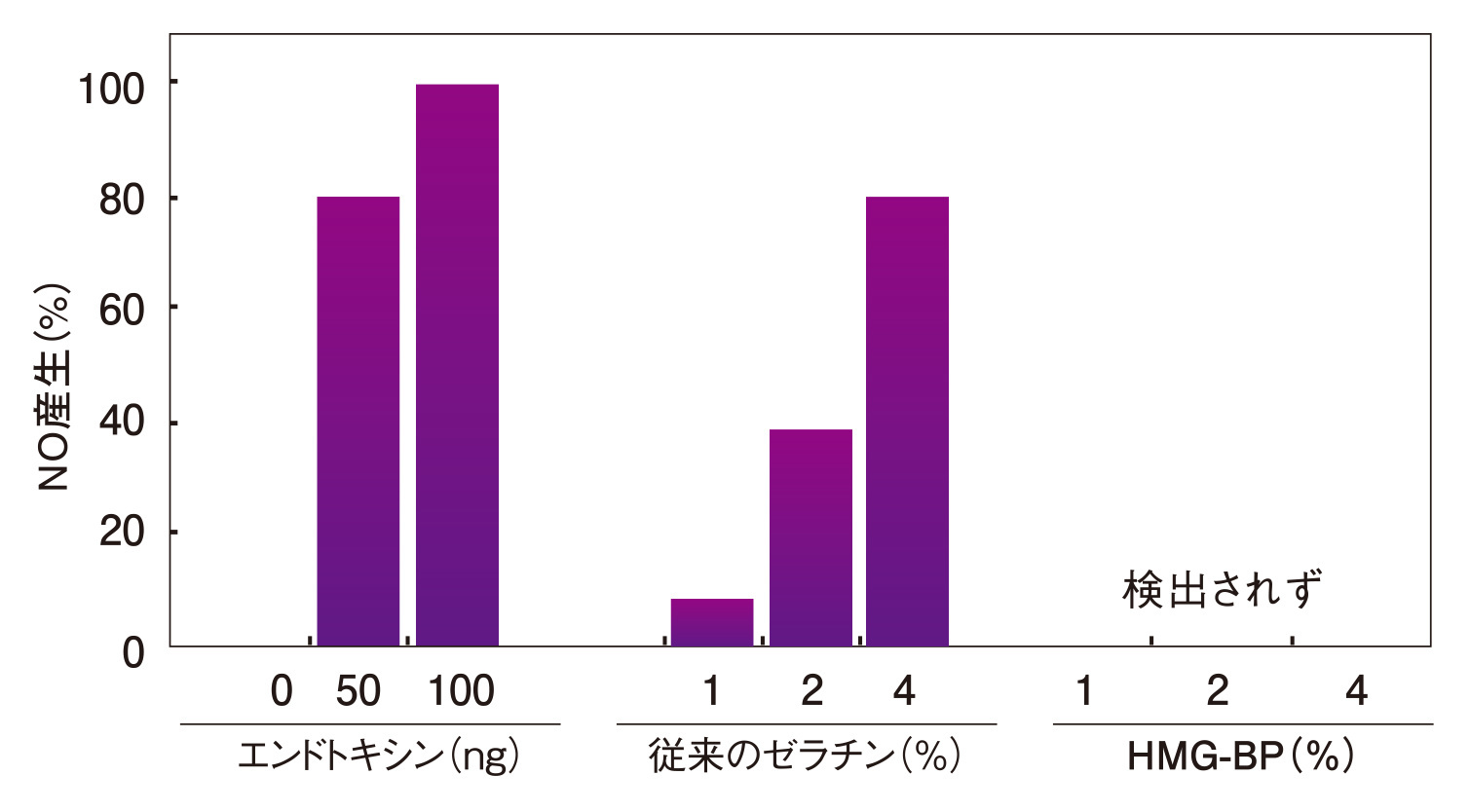
マクロファージ(マウス由来)のNO産生に対する各種ゼラチンの影響
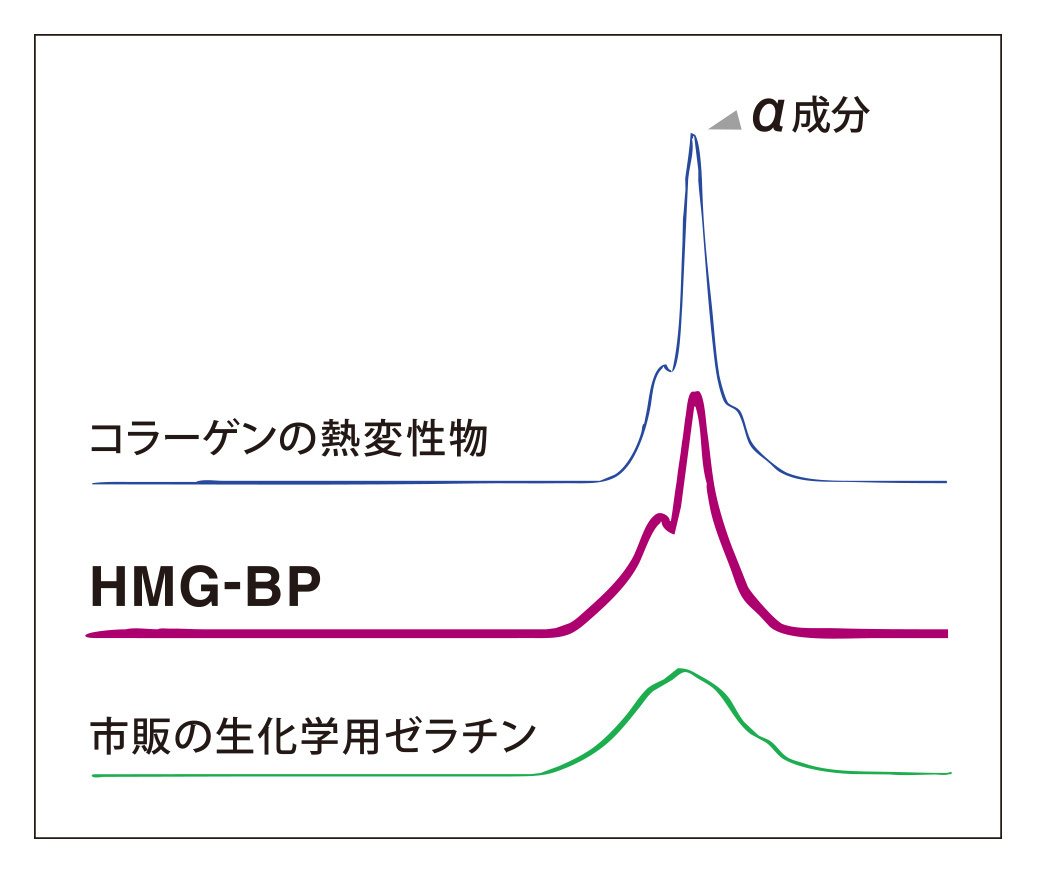
各種ゼラチンの分子量分布
メディゼラチン HMG-BP

特長
- 日本薬局方「精製ゼラチン」規格適合
(製造元コード:892311は日本薬局方「製造専用」医薬品適合) - ゲル化タイプのブタ皮アルカリ処理ゼラチン(250g以上の高ゼリー強度)
- 無菌試験適合(0.2 μmのメンブレンフィルターろ過済み)
- ウイルス不活化工程あり(ウイルスクリアランス試験実施済み)
- 皮内反応試験陰性/抗原性試験陰性
- 低エンドトキシン管理 (10 EU/g以下)
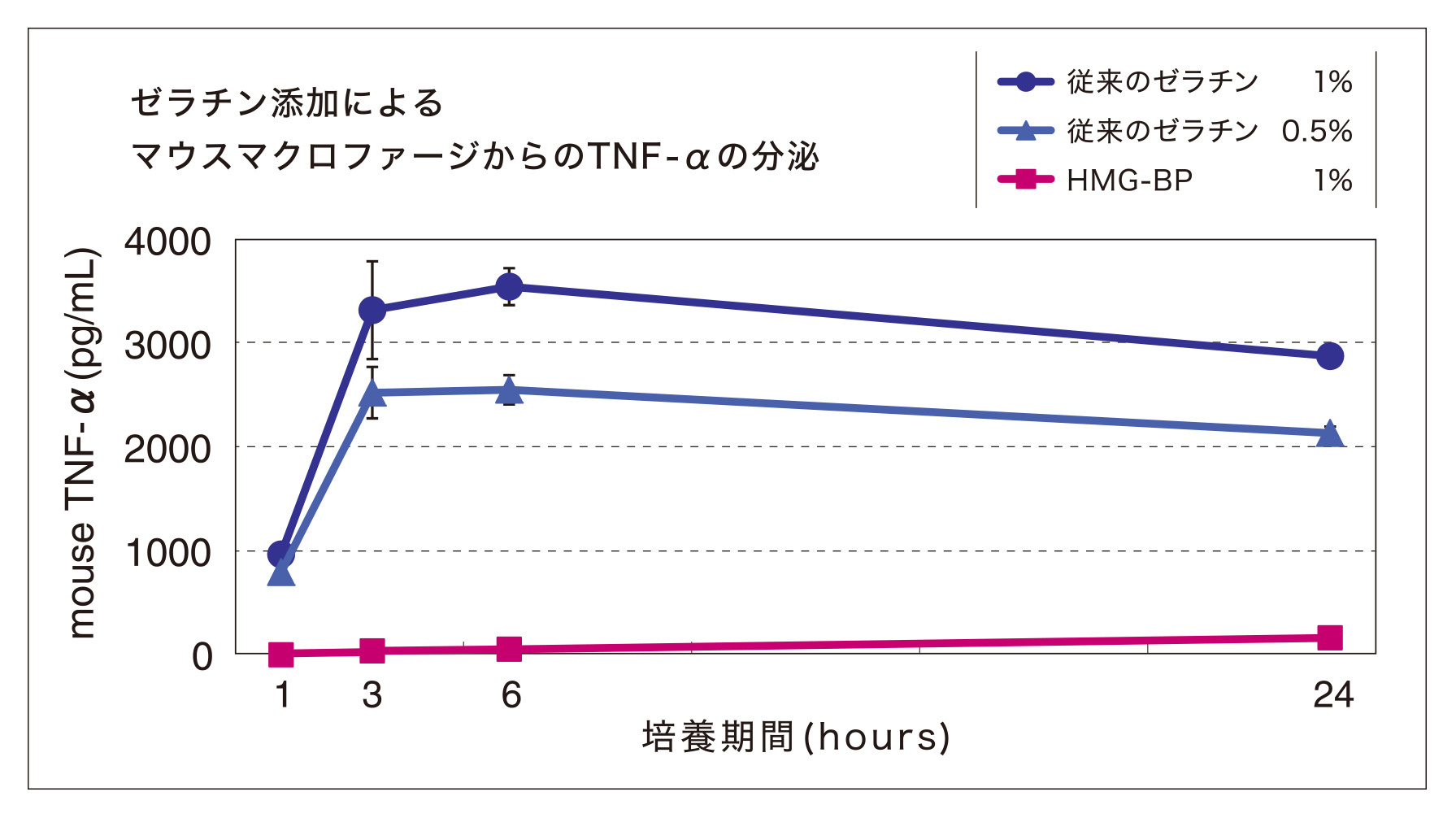
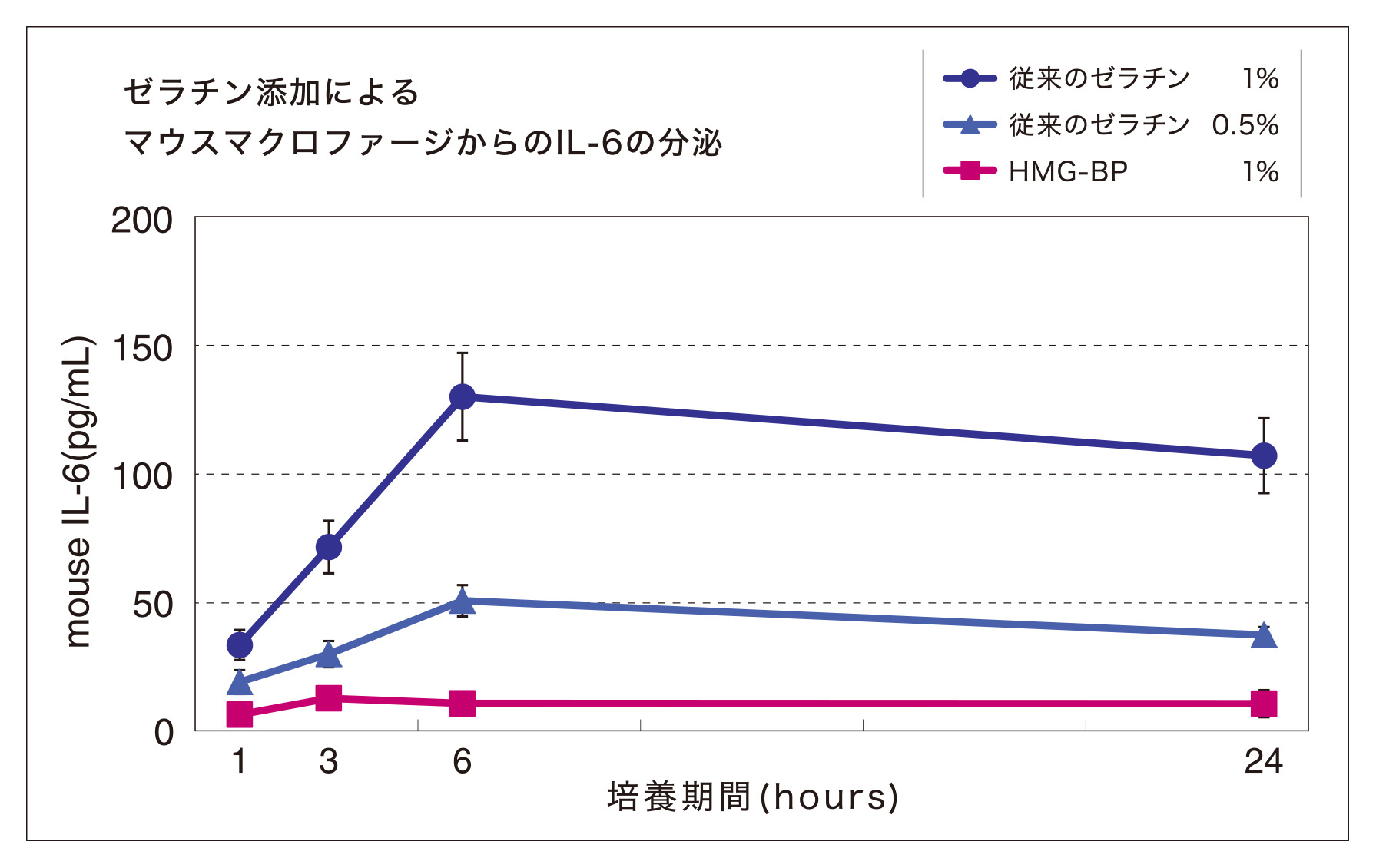
使用事例:マウスマクロファージを用いた生物的試験
方法
- 使用細胞株:RAW264.7 (マクロファージ様細胞)
- 培地:DMEM + 10% FBS
細胞を1日培養した後、ゼラチンを添加し、一定時間培養を行った。その後、上清を回収し、各種サイトカインを測定した。
結果
マウスマクロファージに1%のHMG-BPを添加してもTNF-αやIL-6といった炎症性サイトカインは分泌されなかった。
ハイグレードゼラチン AP

特長
- 日本薬局方「精製ゼラチン」規格適合 (製造元コード:892313は日本薬局方「製造専用」医薬品適合)
- 非ゲル化タイプのブタ皮酸処理ゼラチン
- 無菌試験適合 (0.2 μmのメンブレンフィルターろ過済み)
- 低エンドトキシン管理 (10 EU/g以下)
製品一覧
- 項目をすべて開く
- 項目をすべて閉じる
307-34416:日本薬局方「精製ゼラチン」(製造専用)
303-34413, 301-34414:日本薬局方「精製ゼラチン」規格適合
303-34413, 301-34414:日本薬局方「精製ゼラチン」規格適合
309-34334:日本薬局方「精製ゼラチン」(製造専用)
301-34333, 305-34331:日本薬局方「精製ゼラチン」規格適合
301-34333, 305-34331:日本薬局方「精製ゼラチン」規格適合
- 掲載内容は本記事掲載時点の情報です。仕様変更などにより製品内容と実際のイメージが異なる場合があります。
- 掲載されている製品について
- 【試薬】
- 試験・研究の目的のみに使用されるものであり、「医薬品」、「食品」、「家庭用品」などとしては使用できません。
- 試験研究用以外にご使用された場合、いかなる保証も致しかねます。試験研究用以外の用途や原料にご使用希望の場合、弊社営業部門にお問合せください。
- 【医薬品原料】
- 製造専用医薬品及び医薬品添加物などを医薬品等の製造原料として製造業者向けに販売しています。製造専用医薬品(製品名に製造専用の表示があるもの)のご購入には、確認書が必要です。
- 表示している希望納入価格は「本体価格のみ」で消費税等は含まれておりません。
- 表示している希望納入価格は本記事掲載時点の価格です。
Share