ブラウンヒドロホウ素化反応
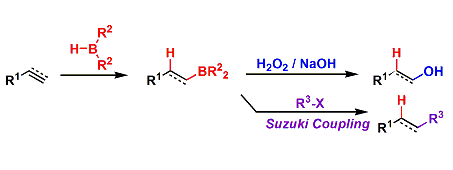
アルキン→アルデヒド、アルケン
B-H結合のオレフィンへの位置・立体選択的syn-付加と、引き続くH2O2/NaOH酸化により、アルケンからanti-Markovnikov型アルコールが合成できます。オキシ水銀化や水和反応ではMarkovnikov型アルコールしか得られないため、これと相補的に用いることができます。アルキンを原料として用いれば、カルボニル化合物が合成可能です。
最も基本的な反応剤であるボラン(BH3)は、二量体のジボランとして存在しています。これは有毒気体であり、反応性もそれほど高くないため実際にはあまり用いません。
単量体にする目的で配位子を結合させたボラン錯体(BH3・L)が現実には多用されます。配位子としてはTHF、ジメチルスルフィド、アミンなどが代表的です。また、これらボラン錯体は溶液状態で市販されており、簡便に使用できます。
しかし、ボラン錯体を用いる場合は、ヒドロホウ素化の位置/立体/官能基選択性に難を示す場合が少なくありません。この問題は、ボランに巨大な置換基を導入することで解決できます。BとHの電気陰性度にはそれほど差が無く、静電的要因よりはむしろ立体障害の影響が大きいためです。
下に代表的な反応剤を示します。酸素官能基を持つカテコールボランやピナコールボランのヒドロホウ素化は遅く、遷移金属触媒を必要とする場合もあります。
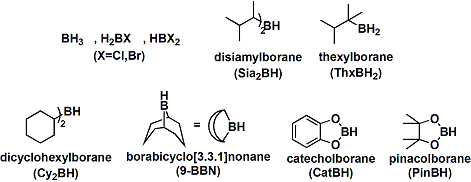
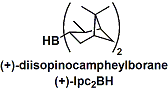
置換基をキラルなものとした光学活性ボランを用いれば、光学活性アルコールも合成可能です。特に天然物から誘導されるジイソピノカンフェイルボラン(Ipc2BH)は実用性が高く、大量スケールの反応にも多用されます。
近年ではパラジウムによるカップリング反応が発達し、ヒドロホウ素化→鈴木-宮浦クロスカップリングという連続的な変換によって、炭素-炭素結合を良好な収率で合成できるようになりました。
Purdue大学のH.C.Brown教授は本反応の開発を含めた有機ホウ素化学発展の業績により、G.Wittigとともに1979年のノーベル化学賞を受賞しています。
本記事はWEBに混在する化学情報をまとめ、それを整理、提供する化学ポータルサイト「Chem-Station」の協力のもと、ご提供しています。
Chem-Stationについて
反応機構
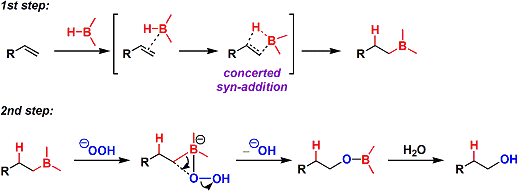
①B-H結合の付加
まず、オレフィンとB上の空軌道が相互作用してπ錯体を形成します。その後協奏的なsyn付加機構で進みます。
②B-C結合の酸化的開裂
まず、B上の空軌道に過酸化水素の共役塩基が配位します。その後ヒドロキシル基が脱離する形で転位反応を起こします。炭素原子上の立体化学は保持されます。
反応例
9-BBNによる位置選択性の改善例
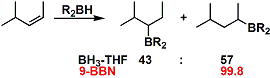
過酸化水素の代わりに、ヒドロキシルアミンスルホン酸塩やクロラミンで酸化を行うとアミンが合成できます。
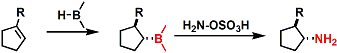
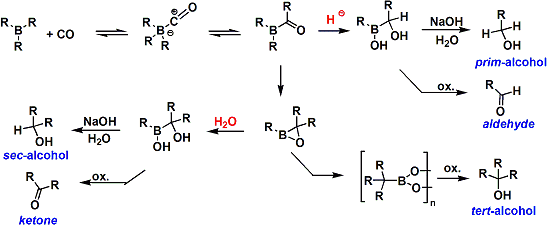
トリアルキルホウ素化合物を一酸化炭素存在下高温で反応させると、アルキル基が全てカルボニル炭素に転位します。引き続き加水分解を行うことで、三級アルコールが合成可能です。本法により通常合成の難しいかさ高いアルコールも合成できます。中間体ボラエポキシドからの転位は非常に遅いため、系中に水を添加しておくと3つめのアルキル基の転位が抑えられます。これにより2級アルコールもしくはケトンの合成も可能となります。また、LiBH4などのヒドリド源を共存させて反応を行うと、アルキル基が一つ転位したボラケトンの段階で還元され、第一級アルコールもしくはアルデヒドを得ることが出来ます。
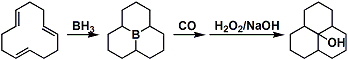
触媒量のRh(I)存在下末端アルキンへヒドロホウ素化を行うと、通常とは異なるZ-ビニルホウ素化合物が合成できます。1)ロジウムビニリデン中間体を経由すると考えられています。
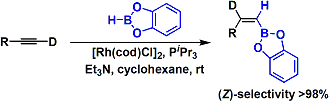
条件によって位置選択性を完全に逆転させることも可能となっています。Rh触媒を用いるケースでは、ケトンなどよりもオレフィンが優先して反応します。配位性官能基を持つ基質において、Crabtree触媒を用いたヒドロホウ素化2)を行うと、directing効果によるジアステレオ選択性が発現します。
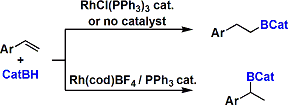
巧みな立体選択的Hydroborationにより、岸らによってMonensinの全合成が達成されています。3)
アリル位反発を避けるよう最安定配座をとったとき、立体障害の少ない方からボランが付加するモデルで選択性は説明されます。
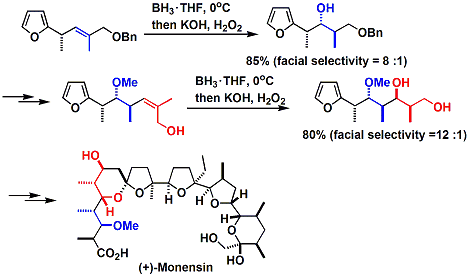
ピリジン・ボラン錯体を用いると、室温でヒドロホウ素化が進行します。ボラン・THF錯体とは異なり、一置換で反応が停止します。得られたホウ素化体はさまざまな有用化合物へと変換可能です。4)
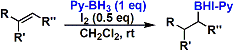
B(C6F5)3添加による反応性向上5)
Rh触媒を用いたヒドロホウ素化反応において、B(C6F5)3添加が反応性および位置選択性において劇的な影響を与えます。B(C6F5)3は、ピナコールボランのヒドリドと複合体をつくり、酸化的付加を促進させる効果を示しています。
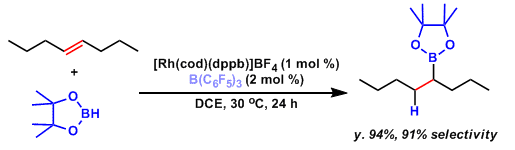
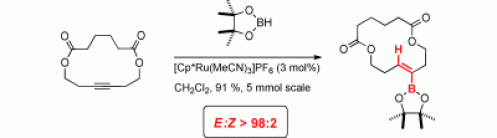
トランス選択的なヒドロホウ素化反応6)
[Cp*Ru(MeCN)3]PF6(Cp*=η5-C5Me5) を触媒として用いると、内部アルキンへのヒドロホウ素化がトランス選択的に進行します。
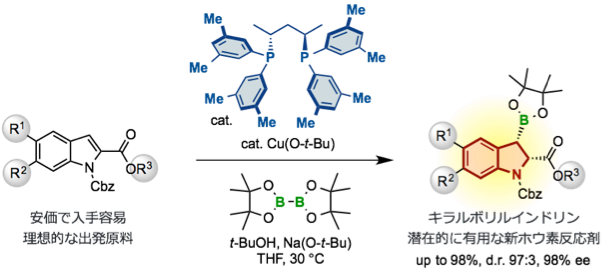
インドールの触媒的不斉ヒドロホウ素化反応7)
脱芳香族化を伴う不斉ヒドロホウ素化反応です。2位にエステルをもつインドール類に対し、銅(I)触媒による脱芳香族不斉ヒドロホウ素化反応が高ジアステレオかつエナンチオ選択的に進行します。
参考文献
- Ohmura, T., Yamamoto, Y. and Miyaura, N. : J. Am. Chem. Soc., 122, 4990 (2000). DOI: 10.1021/ja0002823
- (a) Evans, D. A. and Fu, G. C. : J. Am. Chem. Soc., 113, 4042 (1991). DOI: 10.1021/ja00010a083 (b) Evans, D. A., Fu, G. C. and Hoveyda, A. H. : J. Am. Chem. Soc., 114, 6671 (1992). DOI: 10.1021/ja00043a009
- Schmid, G., Fukuyama, T., Akasaka, K. amd Kishi, Y. : J. Am. Chem. Soc., 101, 259 (1979). DOI: 10.1021/ja00495a064
- Clay, J. M. and Vedejs, E. : J. Am. Chem. Soc., 127, 5766 (2005). DOI: 10.1021/ja043743j
- Lata, C. J. and Crudden, C. M. : J. Am. Chem. Soc., 132,131 (2010). DOI:10.1021/ja904142m
- Sundararaju, B. and Fürstner, A. : Angew. Chem. Int. Ed., 52, 14050 (2013). DOI: 10.1002/anie.201307584
- Kubota, K., Hayama, K., Iwamoto, H. and Ito, H. : Angew. Chem. Int. Ed., 54, 8809 (2015). DOI: 10.1002/anie.201502964
基本文献
- Brown, H. C. and Subba Rao, B C. : J. Am. Chem. Soc., 78, 5694 (1956). DOI: 10.1021/ja01602a063
- Brown, H. C. and Subba Rao, B. C. : J. Am. Chem. Soc., 80, 1552 (1958). DOI: 10.1021/ja01540a011
- Brown, H. C. : “Hydroboration” W. A. Benjaminem (1962).
- Zweifel, G. et al. : Org. React., 13, 1 (1963). DOI: 10.1002/0471264180.or013.01
Review
- Brown, H. C. : Tetrahedron, 37, 3547 (1981). doi:10.1016/S0040-4020(01)98886-6
- Burgess, K. and Ohlmeyer, M. J. : Chem. Rev., 91, 1179 (1991). DOI: 10.1021/cr00006a003
- Beletskaya, I. and Pelter, A. : Terahedron, 53, 4957 (1997). doi:10.1016/S0040-4020(97)00001-X
- Crudden, C. M. and Edwards, D. : Eur. J. Org. Chem, 4695 (2003). DOI: 10.1002/ejoc.200300433
製品一覧
- 項目をすべて開く
- 項目をすべて閉じる
- 掲載内容は本記事掲載時点の情報です。仕様変更などにより製品内容と実際のイメージが異なる場合があります。
- 掲載されている製品について
- 【試薬】
- 試験・研究の目的のみに使用されるものであり、「医薬品」、「食品」、「家庭用品」などとしては使用できません。
- 試験研究用以外にご使用された場合、いかなる保証も致しかねます。試験研究用以外の用途や原料にご使用希望の場合、弊社営業部門にお問合せください。
- 【医薬品原料】
- 製造専用医薬品及び医薬品添加物などを医薬品等の製造原料として製造業者向けに販売しています。製造専用医薬品(製品名に製造専用の表示があるもの)のご購入には、確認書が必要です。
- 表示している希望納入価格は「本体価格のみ」で消費税等は含まれておりません。
- 表示している希望納入価格は本記事掲載時点の価格です。



