プロテオーム研究用 消化酵素
プロテオーム解析において、質量分析は、タンパク質の同定や翻訳後修飾に関する情報を得る手法の1つです。
質量分析を行うためには、電気泳動後のゲルより目的タンパク質を切り出し、酵素処理してペプチド断片にする必要があります。
本製品は、最もよく使われるタンパク質分解酵素であるトリプシンとリシルエンドペプチダーゼを質量分析の前処理用として、使いやすい容量に微量小分けした凍結乾燥品です。
特長
- リシルエンドペプチダーゼは、タンパク質の切断部位を特異的かつ効率的に分解でき、ペプチド質量によるデータベース検索が容易になる
- リシルエンドペプチダーゼとトリプシンを併用することにより、リシン残基における切断の確実性が増し、得られるペプチド数が増加する
- 自己消化が少なく、使用量に応じて微量小分けされている
実験例
トリプシン(Tp)、リシルエンドペプチダーゼ(Lep)およびこれらを併用した場合の比較
SDS-PAGE後のBSAバンド(100 ng)をトリプシン、リシルエンドペプチダーゼ®およびこれらの併用によってゲル内消化し、MALDI-TOFMSを用いて質量分析しました。
図にはそのマススペクトル、表にはその評価を示しました。
図. Tp単独とTpとLepを併用した場合の質量分析スペクトル
TpとLepの併用では、Tp単独では得られないピークが、m/z 2000付近に得られました。
これはペプチドの回収率が上がったことを示します。
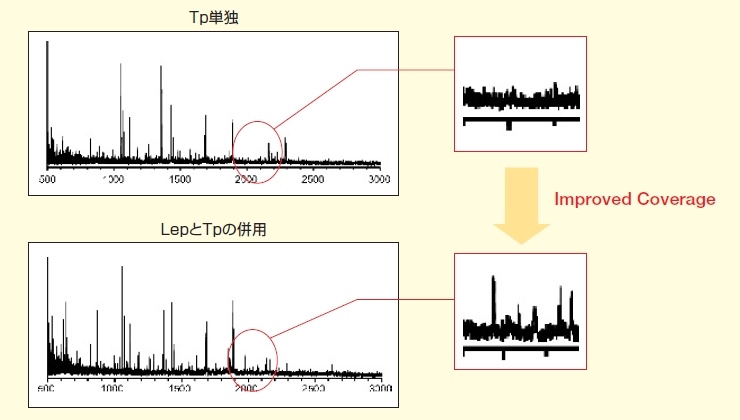
表. TpとLepおよびこれらを併用した場合の比較
Lep単独使用では、Missed Cleavageがほとんどないことがわかります。
TpとLepの併用では、Tp単独と比較してMissed Cleavageが減少し、同定できたペプチド数が増加しています。
| Tp | Lep | Tp と Lep の併用 | |
|---|---|---|---|
| 切断部位 | Arg, Lysの C末端 | Lysの C末端 | Arg, Lysの C末端 |
| Missed Cleavage (切れ残ったペプチドの割合)※ |
多い(8 %) | ほとんどない(0 %) | 少ない(3 %) |
| 同定できたペプチド数 | 17 | 19 | 22 |
(データ提供:大阪府立母子医療センター 和田芳直先生)
※Missed Cleavage 1でデータベース検索した時のCoverage(得られたペプチドが配列全体に占める割合)からMissed Cleavage 0で検索した時のCoverageを引いた値。
参考文献
- Wada, Y. and Kadoya, M.: J. Mass Spectrom., 38, 117(2003).
- Shevchenko, A., Wilm, M., Vorm, O. and Mann., M.: Anal. Chem., 68, 850(1996).
製品一覧
- 項目をすべて開く
- 項目をすべて閉じる
- 掲載内容は本記事掲載時点の情報です。仕様変更などにより製品内容と実際のイメージが異なる場合があります。
- 掲載されている製品について
- 【試薬】
- 試験・研究の目的のみに使用されるものであり、「医薬品」、「食品」、「家庭用品」などとしては使用できません。
- 試験研究用以外にご使用された場合、いかなる保証も致しかねます。試験研究用以外の用途や原料にご使用希望の場合、弊社営業部門にお問合せください。
- 【医薬品原料】
- 製造専用医薬品及び医薬品添加物などを医薬品等の製造原料として製造業者向けに販売しています。製造専用医薬品(製品名に製造専用の表示があるもの)のご購入には、確認書が必要です。
- 表示している希望納入価格は「本体価格のみ」で消費税等は含まれておりません。
- 表示している希望納入価格は本記事掲載時点の価格です。




