スルホニル化試薬
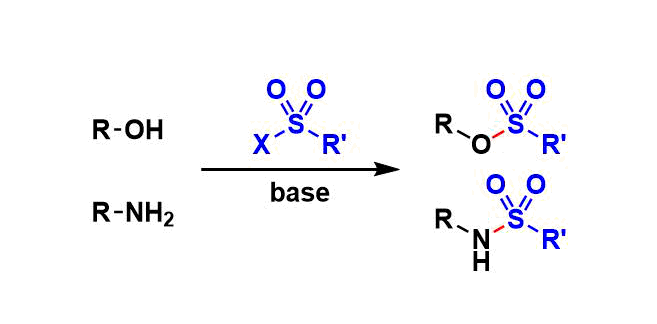
スルホニル基は、フェノールもしくはアミンの保護基として有用である。
アルコールをスルホニル化すれば脱離能が向上し、置換/脱離反応に活性となる。このため、脂肪族アルコール保護の目的に使われるケースは稀である。
一方で保護基の電子求引性を利用し、電子豊富フェノールの酸化防止目的で用いられることは多い。
アミンの保護には有効である。スルホンアミドとして保護すれば、アミンの求核性・塩基性をうまく抑えることができる。特に一級アミンを保護した場合には、スルホンアミドのN-Hプロトンの酸性度が十分高くなる。このため、光延反応やアルキル化条件へと伏すことができ、二級アミン合成にも用いることができる。この目的においては、Tsに比べて脱保護容易なNs基がよく用いられる(福山アミン合成)。
置換基(R')に応じて性質が異なるため、ケースバイケースで上手く選択することが求められる。
本記事はWEBに混在する化学情報をまとめ、それを整理、提供する化学ポータルサイト「Chem-Station」の協力のもと、ご提供しています。
Chem-Stationについて
反応例
保護基の種類
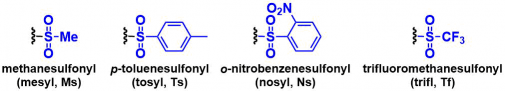
スルホニル保護基としては、以下のものが頻用される。
- メタンスルホニル基 (methanesulfonyl, Ms)
- p-トルエンスルホニル基 (toluenesulfonyl, Ts)
- o-ニトロベンゼンスルホニル基 (nitrobenzenesulfonyl, Ns)
- トリフルオロメタンスルホニル基 (trifluoromethanesulfonyl, Tf)
保護
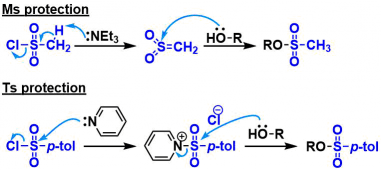
Ms基とTs基では保護時の反応機構が異なる。活性種を効率的に生成する目的で、それぞれ性質の異なる塩基が用いられる。すなわち、Ms保護ではトリエチルアミン、Ts保護ではピリジン(もしくはDMAP-トリエチルアミン)を用いることが一般的である。Ns基もTs基と同様の条件で保護できる。
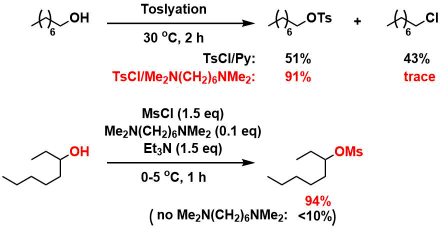
条件によってはCl置換が併発することがある。その場合には無水物(Ms2O・Ts2O)もしくはMe2N(CH2)nNMe2添加条件1) を用いると良い。スズアセタール法を用いることで選択的なMs化・Ts化を行なうことも可能。
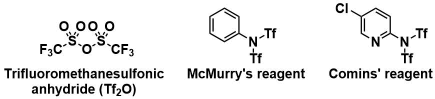
Tf保護にはTf2Oを用いることが一般的である2)。塩基はEt3N、もしくはやや高価だが求核性のない2,6-(tBu)2-pyridineなどが候補となる。Tf2Oはエノール保護には適していない事が多く、溶媒にTHFを用いると重合が併発する問題がある。この場合には代替試薬として、より穏和な反応性をもつMcMurry試薬3)・Comins試薬4)が用いられる。
脱保護
スルホニル基は保護が容易である一方、脱保護は難しく、往々にして厳しめの条件が必要となる。ヒドリド還元、酸性条件、酸化条件、高熱条件に耐性がある一方で、強塩基性条件や1電子還元条件に不安定であるため、これが脱保護条件の選定方針になる。
Ms基については、メチル基C-Hの高い酸性度を活かした強ブレンステッド塩基脱保護条件が知られている5) - 8)。この条件下では脂肪族メシラートや他種のスルホンアミドは維持される。
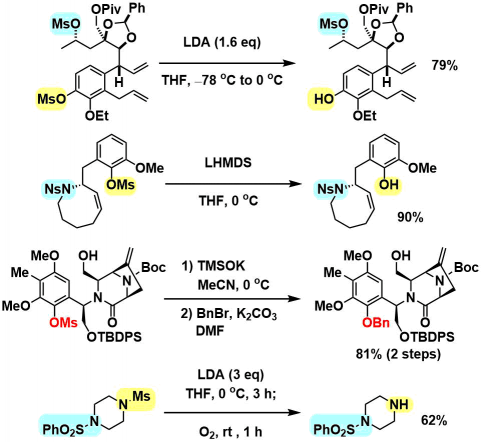
Ts基は一般に脱保護が難しく、熱KOH条件などの厳しい条件が必要となる。一電子還元条件であるMg/MeOH系9)によって穏和に脱保護条件が行える。ただし本条件下ではTsアミドは脱保護されない。
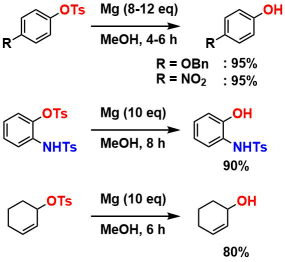
Tsアミドはより強力な還元条件によって脱保護される。Ti(OiPr)4/TMSCl/Mg系10)、SmI2/amine/water系11)、Na-naphthalenide系12)、Na-anthracenide系13)などの条件が知られている。
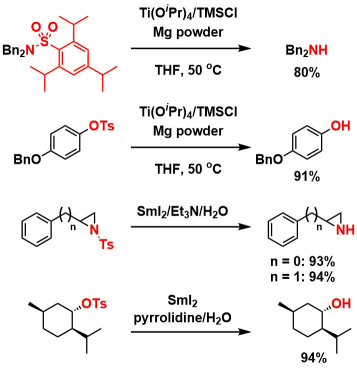
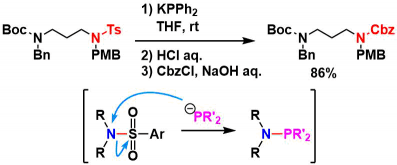
変わり種としては、非常に求核力の強いリンアニオンで処理すると窒素上での求核反応が起こり、結果としてTsアミドの切断が生じることが知られている14)。
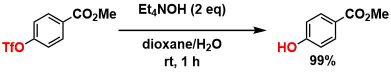
フェノールのTf保護体はEt4NOH条件で簡便に脱保護可能である。メチルエステルやシリルエーテルなどは保持される15)。
Ns基はチオラートの求核付加によって穏和な条件下脱保護できるため、合成化学的価値が特別に高い。
実験手順
アルコールのトシル化16)

デシルアルコール(1.58 g、10 mmol)をクロロホルム(10 mL)に溶解し、氷浴(0 ℃)で冷却した後、ピリジン(1.62 mL、20 mmol)を加え、続いて塩化p-トルエンスルホニル(2.85 g、15 mmol)を少しずつ撹拌しながら添加。反応は2.5時間で完了。
エーテル(30 mL)および水(7 mL)を添加し、有機層を2N HCl、5 %NaHCO3水溶液および水で洗浄し、MgSO4で乾燥させた。
溶媒を減圧下で除去し、粗生成物をシリカゲルカラムクロマトグラフィー(展開溶媒:2 %エーテル/石油エーテル)によって精製し、目的物を油状物(3.06 g、98 %)として得た。
参考文献
- Yoshida, Y., Shimonishi, K., Sakakura, Y., Okada, S., Aso, N. and Tanabe, Y.: Synthesis, 1633(1999). DOI: 10.1055/s-1999-3561
- Hendrickson, J. B. and Bergeron, R.: Tetrahedron Lett., 14, 3839(1973). doi:10.1016/S0040-4039(01)87051-9
- (a) Hendrickson, J. B., Bergeron, B. and Sternbach, D. D.: Tetrahedron, 31, 2517(1975). doi:10.1016/0040-4020(75)80263-8
(b) McMurry, J. E. and Scott, W. J.: Tetrahedron Lett., 24, 979(1983). doi:10.1016/S0040-4039(00)81581-6
(c) Scott, W. J.: Acc. Chem. Res., 21, 47(1988). DOI: 10.1021/ar00146a001 - Comins, D. L. and Dehghani, A.: Tetrahedron Lett., 33, 6299(1992). doi:10.1016/S0040-4039(00)60957-7
- Ritter, T., Stanek, K., Larrosa, I. and Carreira, E. M.: Org. Lett., 6, 1513(2004). DOI: 10.1021/ol049514j
- Kita, Y., Toma, T., Kan, T. and Fukuyama, T.: Org. Lett., 10, 3251(2008). doi:10.1021/ol801111r
- Mori, K., Rikimaru, K., Kan, T. and Fukuyama, T.: Org. Lett., 6, 3095(2004). doi:10.1021/ol048857e
- Naito, H., Hata, T. and Urabe, H.: Org. Lett., 12, 1228(2010). DOI: 10.1021/ol100086j
- (a) Nyasse, B. and Ragnarsson, U.: Chem. Commun., 1017(1997). doi: 10.1039/A701408B
(b) Sridhar, M., Ashokkumar, B. and Narendar, R.: Tetrahedron Lett., 39, 2847(1998). doi:10.1016/S0040-4039(98)00314-1
(c) Alonso, D. A. and Andersson, P. G.: J. Org. Chem., 63, 9455(1998). doi:10.1021/jo9815296
(d) Pasupathy, K.: Synlett, 1942(2003). DOI: 10.1055/s-2003-42033 - Shohji, N., Kawaji, T. and Okamoto, S.: Org. Lett., 13, 2626(2011). DOI: 10.1021/ol200740r
- Ankner, T. and Hilmersson, G.: Org. Lett., 11, 503(2009). DOI: 10.1021/ol802243d
- Ji, S., Gortler, L. B., Waring, A., Battisti, A. J., Bank, S., Closson, W. D. and Wriede, P. A.: J. Am. Chem. Soc., 89, 5311(1967). DOI: 10.1021/ja00996a055
- Quaal, K. S., Ji, S., Kim, Y. M., Closson, W. D. and Zubieta, J. D.: J. Org. Chem., 43, 1311(1978). DOI: 10.1021/jo00401a005
- Yoshida, S., Igawa, K. and Tomooka, K.: J. Am. Chem. Soc., 134, 19358(2012). DOI: 10.1021/ja309642r
- Ohgiya, T. and Nishiyama, S.: Tetrahedron Lett., 45, 6317(2004). doi:10.1016/j.tetlet.2004.06.104
- Kabalka, G. W., Varma, M., Varma, R. S., Srivastava, P. C. and Knapp, F. F. Jr.: J. Org. Chem., 51, 2386(1986). DOI: 10.1021/jo00362a044
基本文献
- Fischer, E. and Lipschitz, W.: Ber., 48, 360(1915).
- Bordwell, F. G. and Boutan, P. J.: J. Am. Chem. Soc., 79, 717(1957). DOI: 10.1021/ja01560a059
- Kampouris, E. M.: J. Chem. Soc., 2651(1965). DOI:10.1039/JR9650002651
- Kabalka, G. W., Varma, M., Varma, R. S., Srivastava, P. C. and Knapp, F. F. Jr.: J. Org. Chem., 51, 2386(1986). DOI: 10.1021/jo00362a044
- Lei, X., Jalla, A., Shama, M. A. A., Ctafford, J. M. and Cao, B.: Synthesis, 47, 1578(2015). DOI: 10.1055/s-0034-1378867
製品一覧
- 項目をすべて開く
- 項目をすべて閉じる
- 掲載内容は本記事掲載時点の情報です。仕様変更などにより製品内容と実際のイメージが異なる場合があります。
- 掲載されている製品について
- 【試薬】
- 試験・研究の目的のみに使用されるものであり、「医薬品」、「食品」、「家庭用品」などとしては使用できません。
- 試験研究用以外にご使用された場合、いかなる保証も致しかねます。試験研究用以外の用途や原料にご使用希望の場合、弊社営業部門にお問合せください。
- 【医薬品原料】
- 製造専用医薬品及び医薬品添加物などを医薬品等の製造原料として製造業者向けに販売しています。製造専用医薬品(製品名に製造専用の表示があるもの)のご購入には、確認書が必要です。
- 表示している希望納入価格は「本体価格のみ」で消費税等は含まれておりません。
- 表示している希望納入価格は本記事掲載時点の価格です。



