同仁化学 オートファジー検出試薬(DAPGreen,DAPRed,DALGreen)
オートファジーは、細胞内の不要なタンパク質・細胞内小器官等の再利用や代謝のための分解機構として様々な疾患への関与が示唆されています。
DAPRed, DAPGreen, DALGreen は培養細胞に添加するだけで簡便にオートファジーを検出できる蛍光試薬です。DAPRed, DAPGreen はオートファゴソーム膜に取り込まれ蛍光を発します。一方、DALGreen は凝集タンパク質等が分解されるオートリソソーム段階で蛍光を発します。
この様に "DAPRed, DAPGreen, DALGreen は、オートファゴソーム形成およびリソソームとの融合・内容物の分解" の過程を試薬の添加だけでモニタリングすることができます。
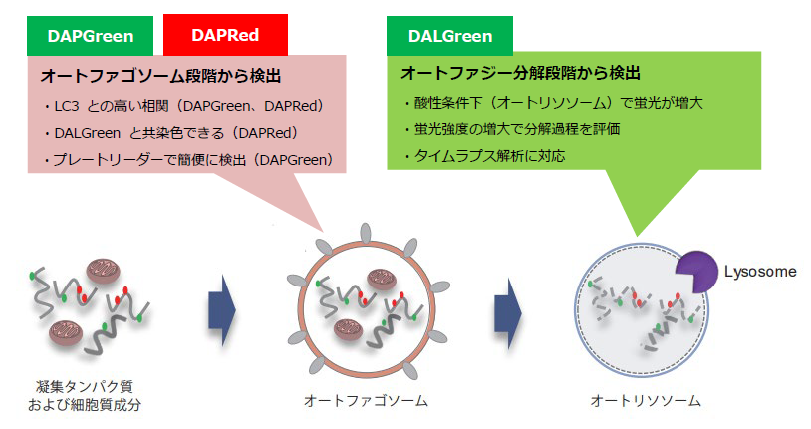
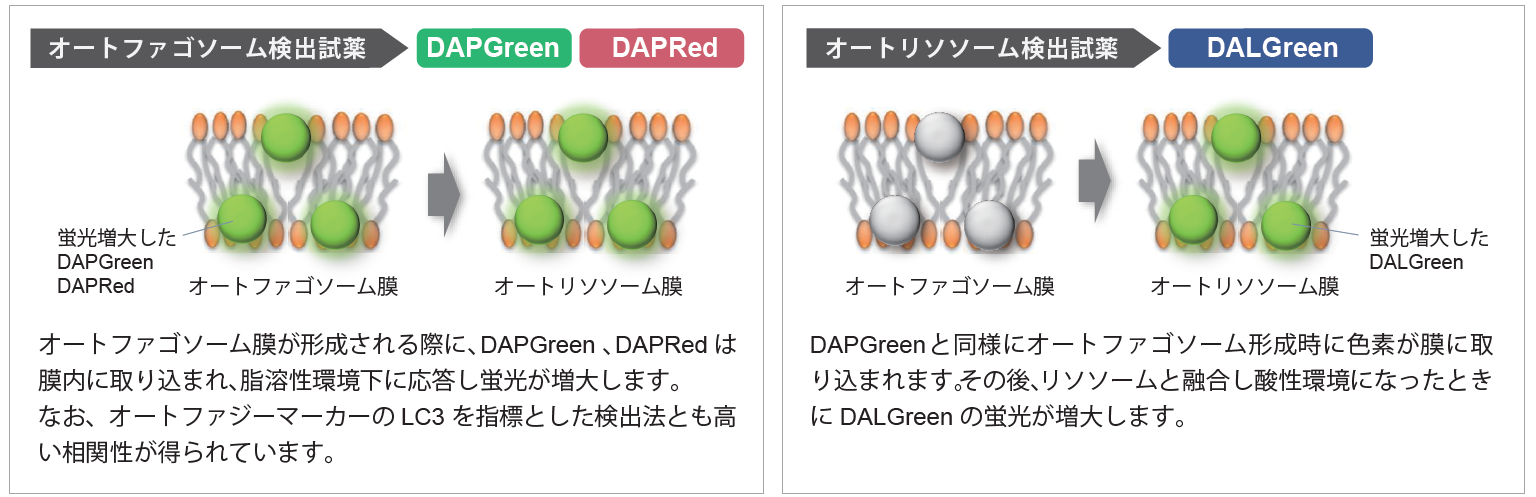
検出試薬の概要
蛍光顕微鏡だけでなくフローサイトメーターでも検出頂けます。また DAPGreen では、プレートリーダーによる検出も実現しました。ご使用の装置で検出可能な蛍光特性をご確認のうえ、ご使用ください。
| 対応装置 | 蛍光特性 | 容量/使用回数の目安 | 既存検出法 | |||
|---|---|---|---|---|---|---|
| 蛍光顕微鏡 | フローサイトメーター | プレートリーダー | ||||
| DAPGreen | 〇 | 〇 | 〇 | Ex. 425-475 nm Em. 500-560 nm ※共焦点顕微鏡では 488 nm にて励起可能 |
5 nmol x 1 / 35 mm dish : 25 枚分 (0.1 µmol/L で使用時) |
LC3-GFP MDC Cyto-ID など |
| DAPRed | 〇 | ✖ | ✖ | Ex. 500-560 nm Em. 690-750 nm |
5 nmol x 1 / 35 mm dish : 25 枚分 (0.1 µmol/L で使用時) |
|
| DALGreen | 〇 | 〇 | ✖ | Ex. 350-450 nm Em. 500-560 nm ※共焦点顕微鏡では 488 nm にて励起可能 |
20 nmol x 1 / 35 mm dish : 10 枚分 (最大濃度で使用時) |
LC3-GFP-RFP など |
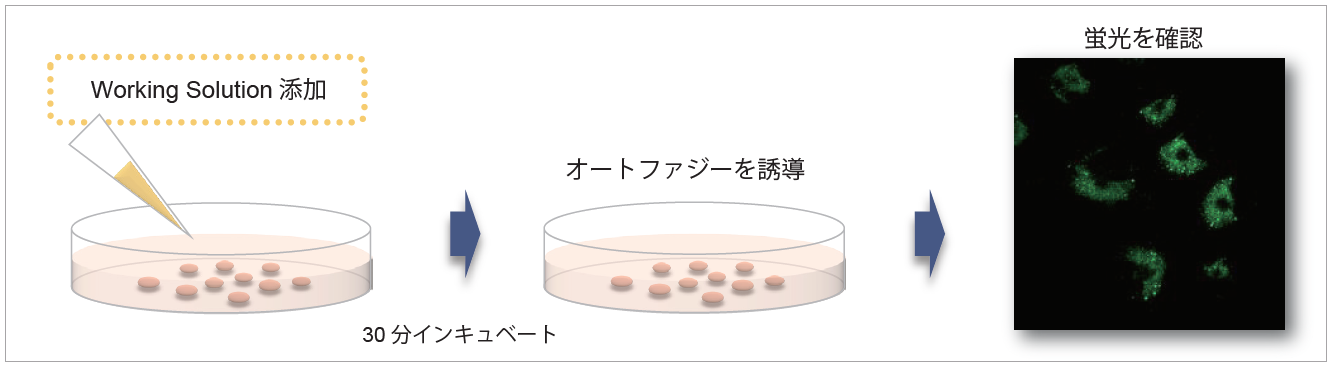
操作方法
遺伝子導入は不要です。準備した細胞に試薬を添加するだけの簡単操作で蛍光イメージングを実現します。
LC3との高い相関
オートファジーマーカーである LC3 を指標とした検出法と共染色を行い局在の比較を行った。
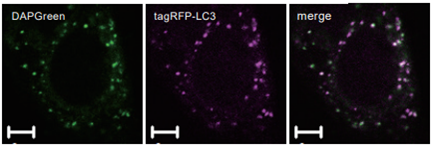
結果
DAPGreenと、LC3が共局在する結果が得られた。
検出条件
DAPGreen:Ex. 488 nm / Em. 500-563 nm
オートファジー誘導条件
RFP-LC3 発現 HeLa 細胞に DAPGreen 添加後、Rapamycin によりオートファジーを誘導した。誘導から 4 時間後に、DAPGreen及び RFP の蛍光像を共焦点顕微鏡にて確認した。
DAPRed と DALGreen の共染色
オートファゴソーム染色試薬 DAPRed とオートリソソーム染色試薬 DALGreen により、HeLa 細胞を染色後、飢餓培養によるオートファジーの誘導を確認した。
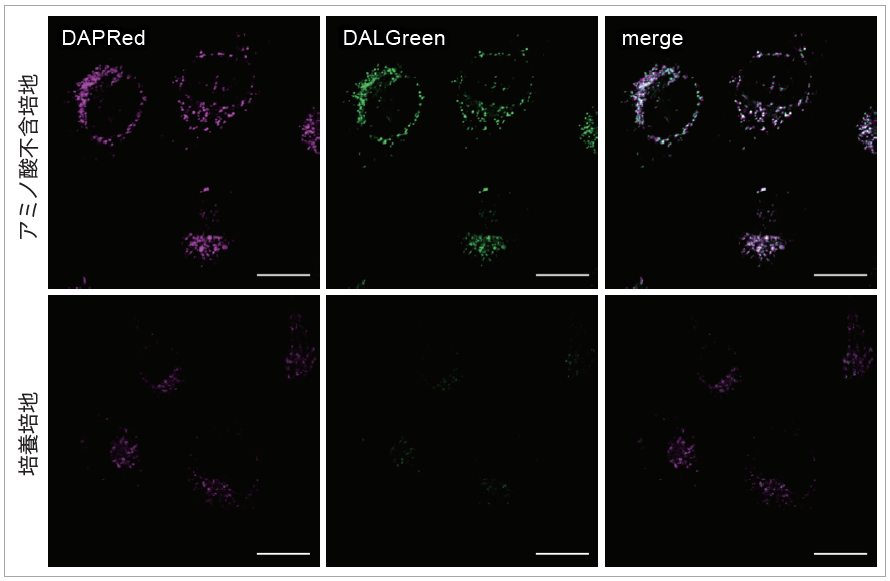
結果
アミノ酸不含培地で培養した HeLa 細胞において、DAPRed と DALGreen の蛍光の増大が確認された。
検出条件
DAPRed:Ex. 561 nm / Em. 600-700 nm
DAPGreen:Ex. 488 nm / Em. 500-563 nm
オートファジー誘導条件
DAPRed および DALGreen で染色後の HeLa 細胞を増殖培地またはアミノ酸不含培地にて5 時間培養し、共焦点顕微鏡にて観察した。
タイムラプスで検出
HeLa 細胞を DALGreen で染色後、飢餓培養にて 6 時間までの細胞の状態を観察した。
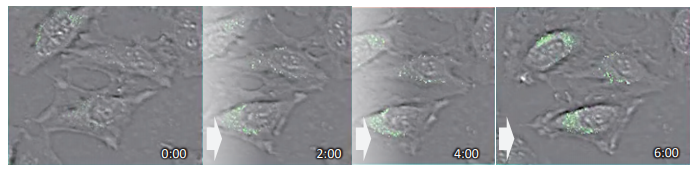
イメージング条件
- 培養条件:アミノ酸不含培養培地
- 装置:共焦点イメージングサイトメーター(横河電機株式会社:CQ1)
- 蛍光フィルター:Ex. 405 / Em. 525/50
- 倍率:20x
オートファジーを誘導した細胞において、DALGreen の蛍光の増大が確認された。
- 本タイムラプスの動画は、同仁化学ホームページにてご覧いただけます。
ULK1/2 ノックアウト細胞での評価
MEF 細胞の野生株およびオートファゴソーム膜形成に関与している ULK1/2 をノックアウトした株を用いて Rapamycin と Chloroquine刺激により比較した。
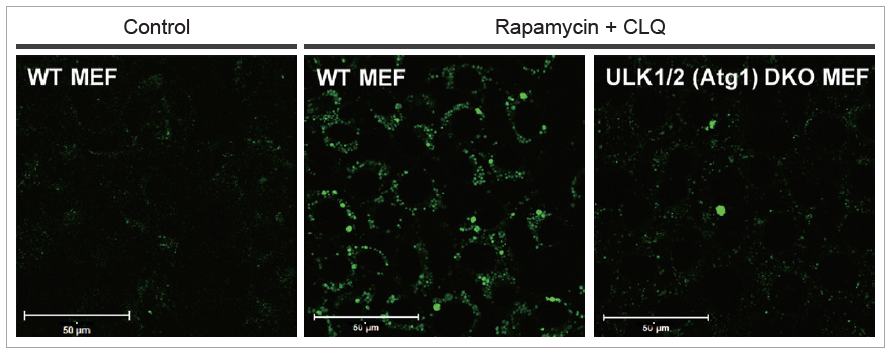
結果
野生株においては DALGreen の蛍光強度の増大が確認されましたが、ULK1/2 ノックアウトマウスにおいては、蛍光の増大は殆ど確認できなかった。
オートファジー誘導条件
DALGreen にて染色後、増殖培地または、500nmol/L Rapamycin 及び 10 µmol/L Chloroquine を含む培地で 8 時間培養し、共焦点顕微鏡にて観察した。
その他アプリケーション
フローサイトでの定量解析
オートファジー誘導後に、DAPGreen の蛍光をフローサイトメーターにて検出した。
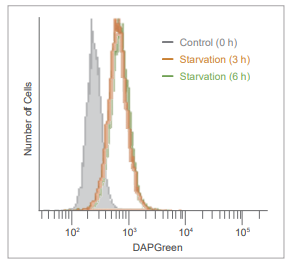
結果
飢餓培養開始から 3 時間後には、強い蛍光シグナルが検出された。
検出条件
検出波長:Ex. 488 nm / Em. 500-560 nm
オートファジー誘導条件
DAPGreen で染色後の HeLa 細胞を、アミノ酸不含培地にて 0、3、6 時間培養し、フローサイトメーターにて検出した。
プレートリーダーでの定量解析
オートファジー誘導後の DAPGreen の蛍光を、プレートリーダーにて検出した。
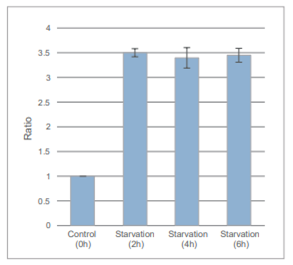 |
結果飢餓培養を開始してから 2 時間後には、コントロールより約 3.5 倍強い蛍光を確認した。 検出条件検出波長 :Ex. 450 nm / Em. 535 nm オートファジー誘導条件DAPGreen で染色後の HeLa 細胞を、アミノ酸不含培地にて 0、2、4、6 時間培養し、プレートリーダーにて検出した。 |
顕微鏡によるオートリソソーム解析例
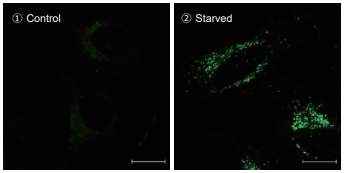
オートファジーの誘導の有無で、DALGreen による蛍光像を共焦点顕微鏡にて確認した。
結果
飢餓培養によりオートファジーを誘導した HeLa 細胞において、DALGreenの蛍光が増大したPuncta(斑点)を確認した。
イメージング条件
検出波長 :Ex. 488 nm / Em. 500-563 nm
オートファジー誘導条件
DALGreenにて染色した細胞を以下の条件で培養。
- Control:増殖培地で6時間培養
- Starved:アミノ酸不含培地で6時間培養
MDCとの比較
DALGreenと既存のオートファジー検出用蛍光色素MDC(Monodansylcadaverine)を用いて、飢餓条件下で培養したHeLa細胞におけるオートファジーを検出した。
-
DALGreenによるイメージング
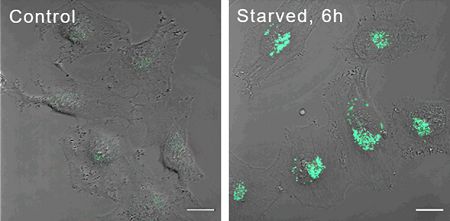
- 濃度:1 µmol/L
- インキュベート時間:30 min
- 検出波長:Ex. 488 nm/ Em. 500-563 nm
- スケールバー:40 µm
試薬添加後に飢餓誘導(6h)
-
MDCによるイメージング
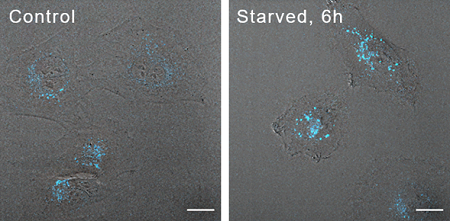
- 濃度:10 µmol/L
- インキュベート時間:30 min
- 検出波長: Ex. 405 nm/ Em. 450-546 nm
- スケールバー:40 µm
飢餓誘導(6h)後に試薬添加
結果
DALGreen にて染色した細胞では、飢餓誘導による蛍光強度の増大がみられた。一方で、MDC による評価では、蛍光強度の変化は、ほとんど見られなかった。
波長
MDC の極大励起波長は紫外域にあるため488 nmでの励起は困難だが、DALGreen では共焦点顕微鏡による488 nm 励起での観察が可能であった。
染色操作
- DALGreen:試薬添加 ⇒ 飢餓誘導
- MDC:飢餓誘導 ⇒試薬添加
DALGreen はオートファジー誘導前に試薬を添加するため、オートファジーをライブでモニターできる。
参考文献
H. Iwashita, H. T. Sakurai, N. Nagahora, M. Ishiyama, K. Shioji, K. Sasamoto, K. Okuma, S. Shimizu, and Y. Ueno, "Small fluorescent molecules for monitoring autophagic flux", FEBS Lett., 2018, 592, (4), 559-567
※同仁化学ホームページにて、文献のダウンロードが可能です。
製品一覧
- 項目をすべて開く
- 項目をすべて閉じる
- 掲載内容は本記事掲載時点の情報です。仕様変更などにより製品内容と実際のイメージが異なる場合があります。
- 掲載されている製品について
- 【試薬】
- 試験・研究の目的のみに使用されるものであり、「医薬品」、「食品」、「家庭用品」などとしては使用できません。
- 試験研究用以外にご使用された場合、いかなる保証も致しかねます。試験研究用以外の用途や原料にご使用希望の場合、弊社営業部門にお問合せください。
- 【医薬品原料】
- 製造専用医薬品及び医薬品添加物などを医薬品等の製造原料として製造業者向けに販売しています。製造専用医薬品(製品名に製造専用の表示があるもの)のご購入には、確認書が必要です。
- 表示している希望納入価格は「本体価格のみ」で消費税等は含まれておりません。
- 表示している希望納入価格は本記事掲載時点の価格です。



