デス・マーチン酸化
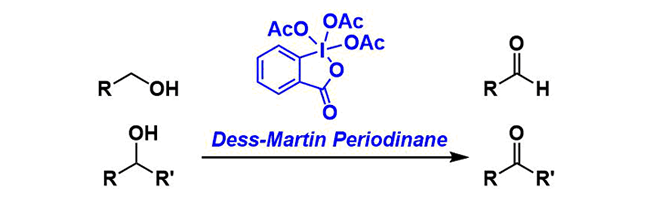
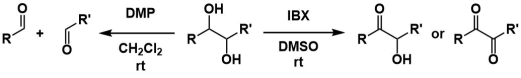
Dess-Martinペルヨージナン(DMP)は温和な酸化剤であり、第1級アルコールからアルデヒドを、第2級アルコールからケトンを得ることができます。
反応は室温付近で速やかに進行し、極めて高い官能基許容性を誇るため、複雑な化合物合成によく使用されています。
たとえば立体的に混みあったアルコール、ラセミ化しやすいα位に不斉中心を持つカルボニル化合物、α,β-不飽和アルデヒドの合成、酸・塩基に不安定な基質にも適用でき、アミン・スルフィド・セレ二ドなども共存可能です。
本記事はWEBに混在する化学情報をまとめ、それを整理、提供する化学ポータルサイト「Chem-Station」の協力のもと、ご提供しています。
Chem-Stationについて
基本文献
- Dess, D. B., Martin, J. C.: J. Org. Chem., 48, 4155 (1983). DOI: 10.1021/jo00170a070
- Dess, D. B., Matrin, J. C.: J. Am. Chem. Soc., 113, 7277 (1991). DOI:10.1021/ja00019a027
- Meyer, S. D., Schreiber, S. L., Nieuwenhuyzen, M.: J. Org. Chem., 59, 7549 (1994). DOI:10.1021/jo00103a067
- Stevenson, P. J., Treacy, A. B.: J. C. S. Perkin Trans. 2 , 589 (1997). DOI: 10.1039/a605253c
- Schröckeneder, A., Stichnoth, D., Mayer, p., Trauner, D.: Beil. J. Org. Chem., 8, 1523 (2012). DOI:10.3762/bjoc.8.172
<Review of DMP oxidation>
- Tohma, H., Kita, Y.: Adv. Synth. Catal., 346, 111 (2004). DOI:10.1002/adsc.200303203
- Ladziata, U., Zhdankin, V. V.: ARKIVOC, ix, 26 (2006).
- Uyanik, M., Ishihara, K.: Chem. Commun., 16, 2086 (2009). DOI: 10.1039/b823399c
- Silva, L. F., Olofsson, B.: Nat. Prod. Rep., 28, 1722 (2011). DOI: 10.1039/c1np00028d
- Zhdankin, V. V.: J. Org. Chem., 76, 1185 (2011). DOI:10.1021/jo1024738
<Comprehensive review for hypervalent iodines>
- Stang, P. J., Zhdankin, V. V.: Chem. Rev., 96, 1123 (1996). DOI: 10.1021/cr940424+
- Zhdankin, V. V., Stang, P. J.: Chem. Rev., 102, 2523 (2002). DOI: 10.1021/cr010003+
- Zhdankin, V. V.., Stang, P. J.: Chem. Rev., 108, 5299 (2008). DOI: 10.1021/cr800332c
- Yoshimura, A., Zhdankin, V. V.: Chem. Rev., 116, 3328 (2016). DOI: 10.1021/acs.chemrev.5b00547
反応機構
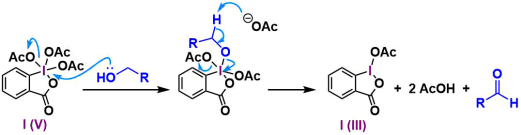
ヨウ素(V)上で酢酸と原料アルコールが配位子交換を起こし、複合体を形成します(1H-NMRによって確認: J. Org. Chem., 61, 9272 (1996).)。α位の脱プロトン化を経由して酸化が起こり、アルデヒドまたはケトンを与えます。機構上、二当量の酢酸が生じますが、これに対して不安定な化合物の場合でも、ピリジンやNaHCO3などを緩衝目的に共存させると適用できます。
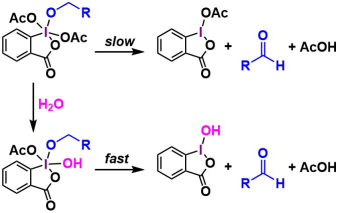
また、1当量の水の添加が反応を加速することが知られています(J. Org. Chem., 59, 7549 (1994).)。これは配位子交換によってヨウ素上に置換したヒドロキシル基の電子供与能によって、アセトキシ-ヨウ素結合の開裂速度が速くなることに起因していると考察されています。
反応例
アルコールの化学選択的酸化
MIDAボロネートの構造は保持され、対応するアシルボランを与えます1)。
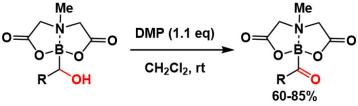
極めてエピ化しやすい基質に対しても、立体化学を損なうことなく酸化できます2)。
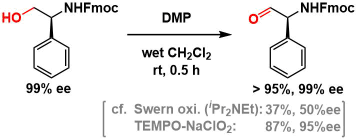
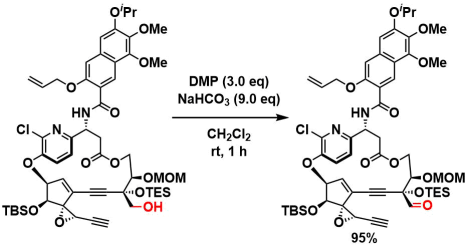
こちらは、酸化に敏感なジヒドロピリジン骨格を維持したままアルコールが酸化される事例です3)。
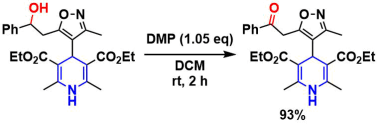
その他の反応形式
アルデヒドからアシルアジドへの変換4)
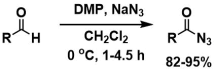
温和な条件でのチオアセタールの除去・トランスアセタール化5)
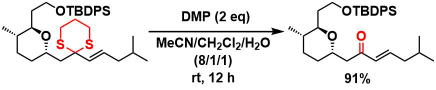
前駆体であるIBXと異なり、1,2-ジオールの場合は開裂体を与えます。
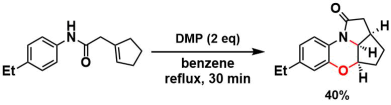
アニリドからの天然物様骨格の合成6)
天然物合成への応用
Kedarcidin Chromophoreの合成7)
Azithromycinの合成8)
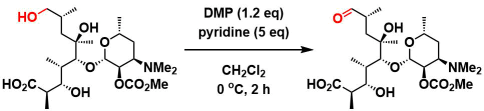
Spongistatin2の合成9)
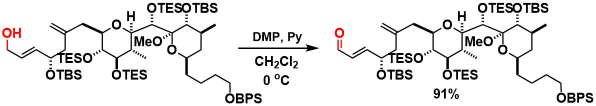
Dragmacidin Dの合成10)
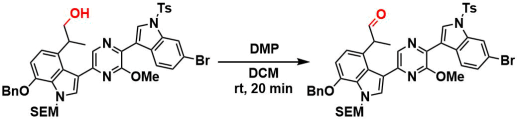
実験手順
試薬の調製
試薬は2-ヨード安息香酸から容易に調製できます。オリジナルの調製法11)では再現性に問題がありましたが、触媒量のTsOHを加えるアセチル化12)、Oxoneを用いるIBX調製法13)を用いると、より簡単な後処理かつ高収率でDMPが得られます。
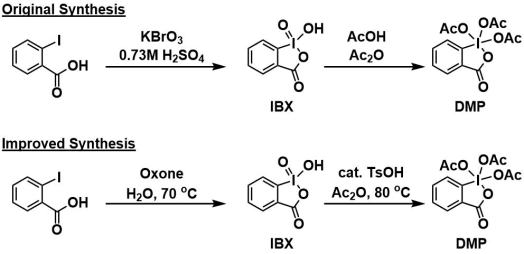
水添加プロトコルによる酸化14)
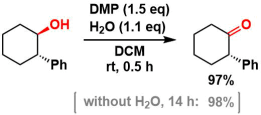
H2O (10 μL, 0.55 mmol) をCH2Cl2 (10 mL)中に加えて、ピペットで吸い出すことを数回繰り返し、wet CH2Cl2を調製する。
2-フェニルシクロヘキサノール(88.4 mg, 0.502 mmol)およびDMP (321 mg、0.502 mmol)の dry CH2Cl2溶液(3 mL)に、滴下漏斗でwet CH2Cl2をゆっくり加える。滴下完了(およそ30分間)に近づくにつれ、透明な溶液は濁った溶液になる。混合物をエーテルで希釈し、ロータリーエバポレータで数mLに濃縮する。30 mLのエーテルで抽出後、15 mLの10% Na2S2O3/飽和NaHCO3水溶液(1:1)、10 mLの水、10 mLの飽和食塩水で洗浄する。この水層を20 mLのエーテルで逆抽出し、有機層を水および飽和食塩水で洗浄した。合わせた有機層を硫酸ナトリウムで乾燥し、濃縮する。フラッシュクロマトグラフィー (hexane/AcOEt = 20:1→10:1)で精製することで、2−フェニルシクロヘキサノン (84.7 mg、97%)を 結晶性固体として得た。
実験のコツ、テクニック
- 反応混合物をエーテルで希釈後、NaOH水溶液かNaHCO3/Na2S2O3水溶液を加え抽出するか、直接シリカゲルカラムにより分離できるので、反応後の後処理は簡便です。
- 爆発性があるため市販されていませんでしが、改良合成法の開発に伴い、販売が再開されました。しかし比較的高価な試薬でありますので、大量に用いる場合には自前で調製する必要があります。後処理時の水をいかに除去するかで活性が異なってきます。
- DMPおよび前駆体のIBXは、ヨウ素のhypervalent化合物であることから爆発性についての危険が指摘されていますので、反応スケールや取扱には細心の注意を払うべきです。
参考文献
1) He, Z., Trinchera, P., Adachi, S., St Denis, J. D., Yudin, A. K.: Angew. Chem. Int. Ed., 51, 11092 (2012). DOI:10.1002/anie.201206501
2) Myers, A. G., Zhong, B., Movassaghi, M., Kung, D. W., Lanman, B. A., Kwon, S.: Tetrahedron Lett., 41, 1359 (2000). DOI:10.1016/S0040-4039(99)02293-5
3) Nelson, J. K., Burkhart, D. J., McKenzie, A., Natale, N. R.: Synlett , 2213(2003). DOI: 10.1055/s-2003-42052
4) Bose, D. S., Rerddy, A. V. N.: Tetrahedron Lett., 44, 3543 (2003). DOI:10.1016/S0040-4039(03)00623-3
5) Langille, N. F., Dakin, L. A., Panek, J. S.: Org. Lett., 5, 575 (2003). DOI: 10.1021/ol027518n
6) Nicolaou, K. C., Zhong, Y.-L., Baran, P. S.: Angew. Chem. Int. Ed., 39,622 (2000).DOI: 10.1002/(SICI)1521-3773(20000204)39:3<622::AID-ANIE622>3.0.CO;2-B
7) Ogawa, K., Koyama, Y., Ohashi, I., Sato, I., Hirama, M.: Angew. Chem. Int. Ed., 48, 1110 (2009). DOI:10.1002/anie.200805518
8) Kim, H. C., Kang, S. H.: Angew. Chem. Int. Ed., 48, 1827 (2009). DOI:10.1002/anie.200805334
9) Smith, A. B., III, Lin, Q., Doughty, V. A., Zhuang, L., McBriar, M. D., Kerns, J. K., Brook, C. S., Murase, N., Nakayama, K.: Angew. Chem. Int. Ed., 40, 196 (2001).DOI:10.1002/1521-3773(20010105)40:1<196::AID-ANIE196>3.0.CO;2-T
10) Garg, N. K., Sarpong, R., Stoltz, B. M.: J. Am. Chem. Soc., 124, 13179 (2002).DOI:10.1021/ja027822b
11) Boeckman Jr., R. K., Shao, P., Mullins, J. J.: Org. Synth. Coll. Vol. 2004, 10, 696.
12) Ireland, R. E., Liu, L.: J. Org. Chem., 58, 2899 (1993). DOI:10.1021/jo00062a040
13) Frigerio, M., Santagostino, M., Sputore,S.: J.Org.Chem., 64, 4537(1999). DOI:10.1021/jo9824596
14) Meyer, S. D., Schreiber, S. L.: J. Org. Chem., 59, 7549(1994). DOI:10.1021/jo00103a067
製品一覧
- 項目をすべて開く
- 項目をすべて閉じる
- 掲載内容は本記事掲載時点の情報です。仕様変更などにより製品内容と実際のイメージが異なる場合があります。
- 掲載されている製品について
- 【試薬】
- 試験・研究の目的のみに使用されるものであり、「医薬品」、「食品」、「家庭用品」などとしては使用できません。
- 試験研究用以外にご使用された場合、いかなる保証も致しかねます。試験研究用以外の用途や原料にご使用希望の場合、弊社営業部門にお問合せください。
- 【医薬品原料】
- 製造専用医薬品及び医薬品添加物などを医薬品等の製造原料として製造業者向けに販売しています。製造専用医薬品(製品名に製造専用の表示があるもの)のご購入には、確認書が必要です。
- 表示している希望納入価格は「本体価格のみ」で消費税等は含まれておりません。
- 表示している希望納入価格は本記事掲載時点の価格です。



