低分子DNA用ポリアクリルアミドゲル
スーパーセップ™ DNA
スーパーセップ™DNAは、2本鎖DNA用の非変性ポリアクリルアミドゲルです。アクリルアミド濃度とゲル架橋度を低分子量DNAの分離に最適化しています。20~200 bpのDNAの分離に適しています。
製品仕様
| アクリルアミド濃度 | 15% |
|---|---|
| プレートサイズ | 100 x 100 x 3 (mm) |
| ゲルサイズ | 90 x 85 x 1 (mm) |
| ウェル数 | 17 ウェル |
| ウェル容積 | 25 μL/ウェル |
| 推奨泳動槽 | イージーセパレーター™ (製品コード:292-36411) |
推奨ランニングバッファー
- 1 x TBEバッファー
- 1 x Tris Glycineバッファー (25 mmol/L Tris, 192 mmol/L Glycine)
例:
5 x TBE (コードNo. 318-90041)
10 x Tris-Glycine Buffer (コードNo. 201-18601)
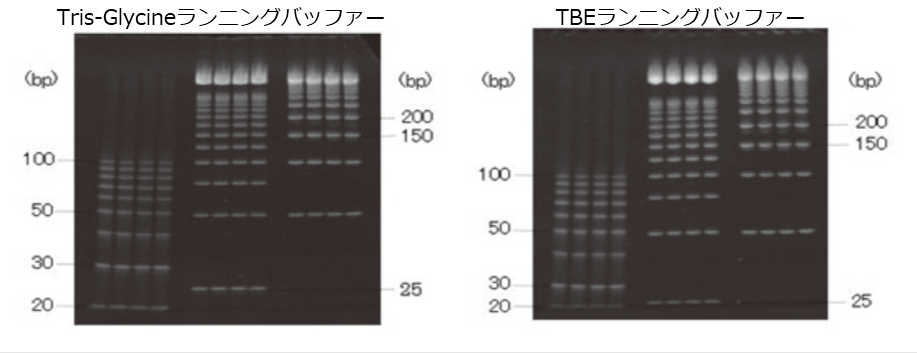
使用例① 低分子DNAの分離例
スーパーセップ™ DNAとTris-Glycineバッファーを用いることで20~200 bpのDNAをきれいに分離できました(左図)。また、TBEバッファーでは、30~200 bpのDNAをきれいに分離できました(右図)。
スーパーセップ™ DNAは200 bp以下のPCR産物, 特にsmall RNAクローニングのゲルからの切り出しに利用可能です。
使用例② アガロースゲルとの比較
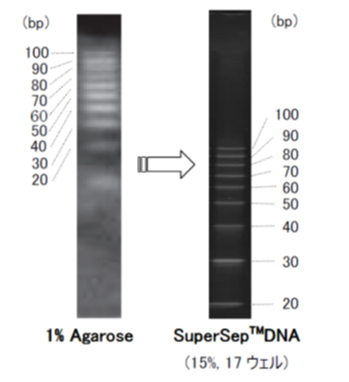
低分子DNAはアガロースゲルで電気泳動を行うとバンドがスメアになりやすいですが、スーパーセップ™ DNAではきれいな分離像を得ることができます。
-
1% アガロースゲルとの比較
-
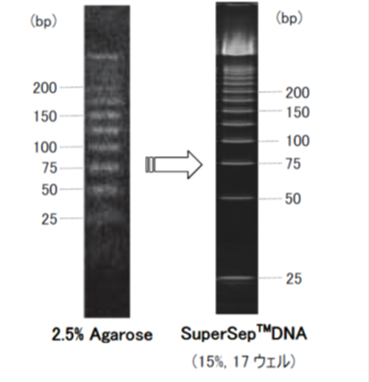
2.5% アガロースゲルとの比較
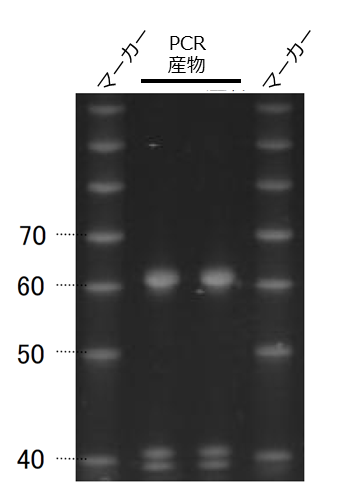
使用例③ PCR産物泳動例
前処理プロトコール
PCR産物をそのまま泳動すると、低分子量タンパク質の混入などによりバンドがスメアになることがあります。
そのような場合には、下記の前処理を推奨します。
- PCR後にフェノール : クロロホルム : イソアミルアルコール (25 : 24: 1) を等量加え、混合する。
- 4℃, 14,000 rpm (18,800 x g)で5分間遠心分離し、上層をマイクロチューブに移す。
- 2のマイクロチューブに、Ethachinmate 1 μL, 回収した水層の1/4量の10 mol/L Ammonium acetate, 全容量の2倍量の99.5% エタノールを加えて混合する。
- 4℃, 14,000 rpm (18,800 x g)で15分間遠心分離し、上清を除く。沈殿を70% エタノールで2回洗浄する。
- 45℃以下で乾燥後、沈殿を滅菌水10 μLに溶解し、6 x Loading Buffer Triple Dye 2 μLを加え混合する。
- ゲルに6 μLをアプライする。
泳動条件
泳動バッファー:25 mmol/L Tris, 192 mmol/L Glycine
電流:30 mA x 60分 (定電流)
染色:エチジウムブロマイド染色 x 15分間
製品一覧
- 項目をすべて開く
- 項目をすべて閉じる
【本サイト掲載情報について】
- 掲載内容は本記事掲載時点の情報です。仕様変更などにより製品内容と実際のイメージが異なる場合があります。
- 掲載されている製品について
- 【試薬】
- 試験・研究の目的のみに使用されるものであり、「医薬品」、「食品」、「家庭用品」などとしては使用できません。
- 試験研究用以外にご使用された場合、いかなる保証も致しかねます。試験研究用以外の用途や原料にご使用希望の場合、弊社営業部門にお問合せください。
- 【医薬品原料】
- 製造専用医薬品及び医薬品添加物などを医薬品等の製造原料として製造業者向けに販売しています。製造専用医薬品(製品名に製造専用の表示があるもの)のご購入には、確認書が必要です。
- 表示している希望納入価格は「本体価格のみ」で消費税等は含まれておりません。
- 表示している希望納入価格は本記事掲載時点の価格です。
Share




