Wittig(ウィッティヒ)反応

正の形式電荷を持つヘテロ原子により隣接位のアニオンが安定化された化学種を、一般にイリド(ylide)と呼ぶ。リンイリド(phosphorous ylide)を用いてカルボニル化合物からアルケンを合成する反応を Wittig 反応という。
古典的な E2 脱離条件によるオレフィン合成は、強酸/強塩基および高温加熱といった過激な条件が必要であり、位置選択性や二重結合異性化の問題が常に付随する。比して本法の利点は、カルボニル基が特異的に C=C 結合へと変換される官能基選択性の高さ、および低温で進行しうる条件の穏和さにある。操作も簡単で、収率も良好であり、幾何異性も制御可能である。このため、カルボニルからアルケンを合成する手法の First Choice として現在でも多用されている。
欠点は生成するホスフィンオキシドの除去が時に難しいことである。本法の改良法である Wittig-Horner 法(トリフェニルホスフィンの代わりにホスファイトを用いる)、Horner-Wadsworth-Emmons 反応では、ホスフィン副生物が高極性・水溶性のため、簡便に除去可能になっている。
電子求引性置換基によりカルボアニオンが安定化され、単離可能なタイプのリンイリドを安定イリドとよぶ。安定イリドとの反応からは E-オレフィンが生成する。一方、単離不可能な(水・空気で分解する)タイプのリンイリドを不安定イリドと呼ぶ。このものは、ホスホニウム塩を塩基で処理して用時調製する。不安定イリドとの反応では Z-オレフィンが生成する。
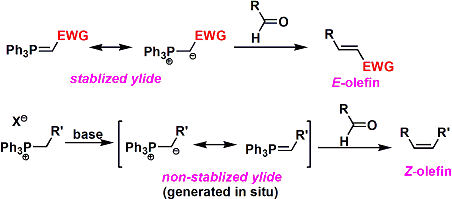
反応性・試薬の塩基性・幾何異性制御等の問題もあり、四置換オレフィン合成への適用は通常難しい。
本記事はWEBに混在する化学情報をまとめ、それを整理、提供する化学ポータルサイト「Chem-Station」の協力のもと、ご提供しています。
Chem-Stationについて
反応機構
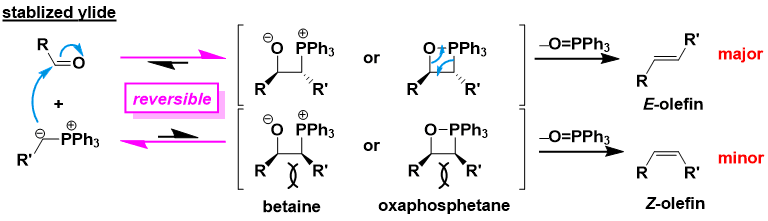
まず、リンイリドがカルボニル化合物に付加し、ベタイン中間体もしくはオキサホスフェタン中間体を生じる。引き続きホスフィンオキシドが脱離してアルケンを与える。リン―酸素結合が強いことが、反応を進行させる駆動力となっている。オキサホスフェタン中間体については、配位子のデザインにより安定化されたものが単離・構造決定されている。一方でベタイン中間体については現在に至るまで確認されておらず、存在は推測の域を出ない。
安定イリドの場合には、カルボニル+リンイリド付加段階が可逆となる。熱力学的支配下にもっとも安定となるオキサホスフェタン中間体を経由し、反応が進行する。このため E-オレフィンが主生成物になる。
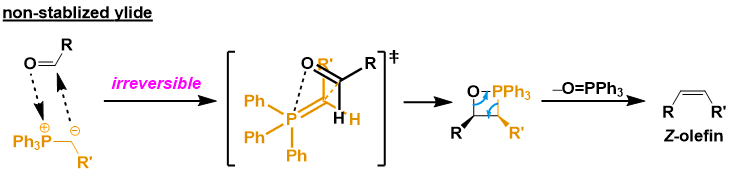
不安定イリドの場合には試薬の反応性が高く、カルボニル+リンイリドの付加が不可逆的に進行する。このため速度論支配型の遷移状態を経てオキサホスフェタン中間体が生成する。具体的には、もっとも立体反発の少ない下図のような四員環遷移状態を経由する。引き続くホスフィンオキシドの脱離を経て、Z-オレフィンを与える。 リチウム塩などが系中に含まれると Z-選択性は低下するので注意。
反応例
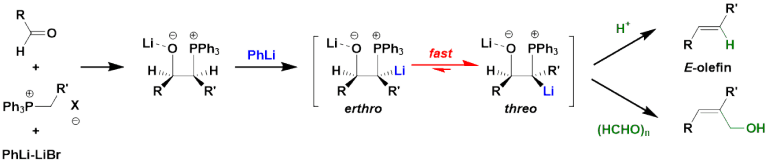
リンイリドをアルデヒドに低温で付加させて生じる中間体を、PhLiなどの強塩基で処理すると、β-オキシドイリドが生成する。これは熱力学的に安定な threo 型に速やかに移行することが知られている。これを活用すれば、不安定イリドから E-オレフィンが合成できる(Schlosser変法)。β-オキシドイリドは様々な求電子剤とも反応するため、多官能基化も可能である。
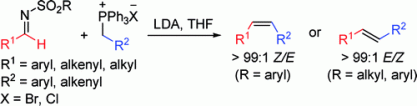
リンイリド試薬は通常エステルとは反応しないが、分子内反応は例外。エノールエーテル型生成物を与える。
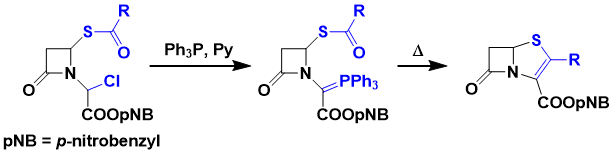
MOMCl と PPh3から調製されるメトキシメチレントリフェニルホスフィンは、アルデヒド/ケトンの一炭素増炭剤として有用である1)。
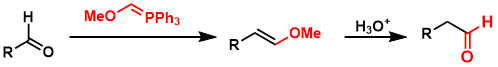
ホスホラン化合物は還元されやすい特性を利用し、リンを触媒量に減じた Wittig 反応が近年開発された2)。
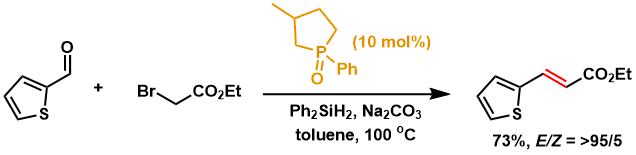
カルボニル化合物の代わりにスルホニルイミンを求電子剤とすれば、窒素置換基に応じてオレフィンの幾何異性が制御される3)。
参考文献
- Levins, S. G. : J. Am. Chem. Soc., 80, 6150 (1958). DOI: 10.1021/ja01555a068
- (a) O’Brien, C. J., Tellez, J. L., Nixon, Z. S., Kang, L. J., Carter, A. L., Kunkel, S. R., Przeworski, K. C. and Chass, C. A. : Angew. Chem. Int. Ed., 48, 6836 (2008). DOI: 10.1002/anie.200902525 (b) O’Brien, C. J. et al. : Chem. Eur. J., 19, 15281 (2013). DOI: 10.1002/chem.201301444
- Dong, D.-J. ., Li, H.-H. and Tian, S.-K. J. : Am. Chem. Soc., 132, 5018 (2010). DOI: 10.1021/ja910238f
基本文献
- Wittig, G. and Scholkopf, U. : Ber., 87, 1318 (1954). doi:10.1002/cber.19540870919
- Wittig, G. and Scholkopf, U. : Ber., 88, 1654 (1955). doi:10.1002/cber.19550881110
<Schlosser Modification>
- Schlosser, M. and Christmann, K. F. : Angew. Chem. Int. Ed. Engl., 5, 126 (1966). doi:10.1002/anie.196601261
<review>
- Maercker, A. : Org. React., 14, 270 (1965).
- Vollhardt, K. P. C. : Synthesis, 765 (1975). DOI: 10.1055/s-1975-23920
- Becker, K. B. : Tetrahedron, 36, 1717 (1980). doi:10.1016/0040-4020(80)80068-8
- Murphy, P. J. and Brennan, J. : Chem. Soc. Rev., 17, 1 (1988). DOI: 10.1039/CS9881700001
- Maryanoff, B. E. and Reitz, A. B. : Chem. Rev., 89, 863 (1989). DOI: 10.1021/cr00094a007
- Cristau, H.-J. : Chem. Rev., 94, 1299 (1994). DOI: 10.1021/cr00029a006
- Burton, D. J., Yang, Z.-Y. and Qiu, W. : Chem. Rev., 96, 1641 (1996). DOI: 10.1021/cr941140s
- Nicolaou, K. C., Harter, M. W., Gunzner, J. L. and Nadin, A. : Liebigs Ann., 7, 1283 (1997). DOI: 10.1002/jlac.199719970704
- 田中圭, 富士薫 : 有機合成化学協会誌, 56, 521 (1998). doi:10.5059/yukigoseikyokaishi.56.521
- Murphy, P. J. and Lee, S. E. : J. Chem. Soc. Perkin Trans., 1, 3049 (1999). DOI: 10.1039/A803560A
- Hoffmann, R. W. : Angew. Chem. Int. Ed., 40, 1411 (2001). [abstract]
- Rein, T. and Pedersen, T. M. : Synthesis, 579 (2002). DOI: 10.1055/s-2002-23535
- Xu, S. and He, Z. : RSC Adv., 3, 16885 (2013). DOI: 10.1039/C3RA42088D
- Byrne, P. A. and Gilheany, D. G. : Chem. Soc. Rev., 42, 6670 (2013).
製品一覧
- 項目をすべて開く
- 項目をすべて閉じる
【本サイト掲載情報について】
- 掲載内容は本記事掲載時点の情報です。仕様変更などにより製品内容と実際のイメージが異なる場合があります。
- 掲載されている製品について
- 【試薬】
- 試験・研究の目的のみに使用されるものであり、「医薬品」、「食品」、「家庭用品」などとしては使用できません。
- 試験研究用以外にご使用された場合、いかなる保証も致しかねます。試験研究用以外の用途や原料にご使用希望の場合、弊社営業部門にお問合せください。
- 【医薬品原料】
- 製造専用医薬品及び医薬品添加物などを医薬品等の製造原料として製造業者向けに販売しています。製造専用医薬品(製品名に製造専用の表示があるもの)のご購入には、確認書が必要です。
- 表示している希望納入価格は「本体価格のみ」で消費税等は含まれておりません。
- 表示している希望納入価格は本記事掲載時点の価格です。
お問合せについてお問合せ等につきましては、「お問合せ窓口」からお問合せください。
また、お客様から寄せられた「よくある質問」を掲載しています。お問合せの前に一度ご確認ください。



