オキシトシン ELISAキットワコー
Oxytocin ELISA Kit Wako
|
比較
|
製品コード
|
容量
|
価格
|
在庫
|
|
|---|---|---|---|---|---|
|
|
|
96回用
|
|
20以上 |
ドキュメント
キットコンポーネント
96回用
| 抗体固相化プレート | 1プレート |
|---|---|
| オキシトシン標準品 | 100 μL |
| 緩衝液 | 60 mL |
| ビオチン結合オキシトシン | 1本 |
| ペルオキシダーゼ結合ストレプトアビジン溶液 | 100 μL |
| 発光試薬1 | 6 mL |
| 発光試薬2 | 6 mL |
| 洗浄液(10×) | 100 mL |
| 検体前処理液1 | 5 mL |
| 検体前処理液2 | 12 mL |
| プレートシール | 4枚 |
製品概要
オキシトシン(Oxytocin)は9アミノ酸のペプチドホルモンであり、ストレス緩和や抗不安/抗恐怖作用を示し、母性行動の形成にも関与することから、通称「幸せホルモン」、「愛情ホルモン」などと呼ばれています。うつや自閉症など精神疾患の治療や機能性素材の開発などでも注⽬されている分子です。しかしながらこれまでのオキシトシンの測定は、C18 カラムを⽤いた煩雑な前処理や多量の検体が必要といった課題がありました。
オキシトシンELISA キットワコーは、検体中のオキシトシンを定量できるELISAキットです。検体の前処理は試薬の混合、撹拌、遠心分離のみと簡便で、最低必要検体量も50 μL と従来のオキシトシン測定の課題を克服しました。
特長
- 簡便な前処理
検体の前処理はキット添付の前処理液を添加し、撹拌、遠心分離するだけ。C18 カラムや有機溶媒は不要。 - 少量検体で測定可能
最低必要検体量は50 μL(n=1)。 - 短時間測定
測定時間は2.5時間。前処理も約30分で可能。 - 多様な検体に対応
ヒト唾液 / 尿 / 血清 / 血漿、マウス・ラット血清 / 血漿に対応。
[注意事項]
本キットは高感度な競合法を採用しているため、プレートシェーカーおよび発光測定用プレートリーダーが必要となります。
日本国内における受託サービスで本キットを利用するには許可が必要です。詳細は当社にお問合せください。
-
キット性能
検量線範囲 4.00~1,024 pg/mL 測定対象 オキシトシン 測定対象検体 ヒト 唾液 / 尿 / 血清 / 血漿
マウス 血清 / 血漿
ラット 血清 / 血漿必要検体量 50 μL (n=1での最低必要量)
200 μL (n=2での推奨検体量)測定時間 約2.5 時間 検出法 発光系 (発光測定用プレートリーダーが必要) -
検量線例
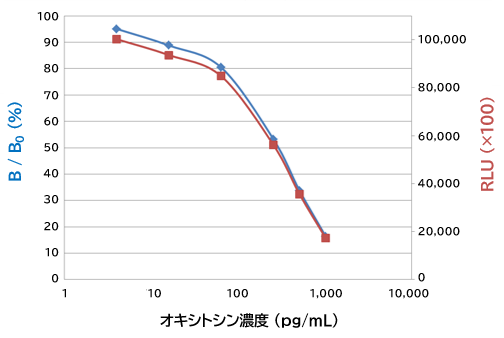
-
測定原理
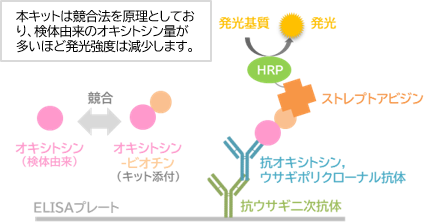
-
① 測定プレートの各ウェルにはあらかじめ抗オキシトシン, ウサギポリクローナル抗体-抗ウサギ二次抗体が固相化されています。 ② プレートのウェルにビオチン結合オキシトシン溶液と標準溶液もしくは前処理済検体を入れて競合反応させます。 ③ ビオチンとHRP結合ストレプトアビジンを反応させます。 ④ HRP用の発光基質を添加します。 ⑤ ウェル中のHRP活性(発光強度)を測定することで検体中のオキシトシン濃度を測定します。
前処理方法の比較
-
当社前処理法 (約30 分, 回収率: 90-120 %)
検体 (唾液 / 尿 / 血清 / 血漿)
↓
検体前処理液1 添加
↓
撹拌後、室温10 分静置 (5 分経過後に一度撹拌)
↓
検体前処理液2 添加
↓
撹拌後、室温10 分静置 (5 分経過後に一度撹拌)
↓
遠心分離
↓
上清を分取し測定用検体とする -
E社前処理法 (約2~4 時間, 回収率: 42-110 %)
検体 (唾液 / 尿 / 血清 / 血漿)
↓
TFA添加、混合
↓
遠心分離
↓
上清をTFA、アセトニトリルで平衡化したC18カラムに添加
↓
TFAで洗浄、アセトニトリルで溶出
↓
溶出画分の減圧、乾固
↓
緩衝液で溶解し測定用検体とする
検体の濃縮方法(オプション)
以下の方法で検体の濃縮が可能です。オキシトシン濃度が低い検体にお試しください。
ただし必要検体量が増えますのでご注意ください。
濃縮プロトコール例 (3倍濃縮, 二重測定)
| 唾液 / 尿 / 血清検体を各300 μL(通常の二重測定に必要な唾液量の3倍)を採取する。 | |
| ▼ | |
| 検体前処理液1を30 μL添加し、撹拌後5分静置する。その後、撹拌しさらに5分静置する。 | |
| ▼ | |
| 検体前処理液2を225 μL添加し、撹拌後5分静置する。その後、撹拌しさらに5分静置する。 | |
| 撹拌後、遠心処理(5000-6000×g, 10分, 4℃)を行い、上清を360 μL分取する。 | |
| ▼ | |
| 分取した上清を以下条件にて濃縮、乾固する。 使用機器: miVac Duo LV (Cat No. DPP-10000-G00, SP SCIENTIFIC社) 販売元であるスクラムのページに移動します 濃縮条件: 30℃、3時間 乾固した検体は4℃で保管。 |

|
| ▼ | |
| 乾固検体にキット添付緩衝液を120 μL添加する。(液量比で3倍濃縮) |
濃縮前後の測定値の比較
| ID | 濃縮(-) | 濃縮 (+) | 濃縮効果率 |
|---|---|---|---|
| 測定値 (pg/mL) | 測定値 (pg/mL) | ||
| 唾液検体 | |||
| No.1 | 28.4 | 80.5 | 2.83 |
| No.9 | 15.1 | 40.3 | 2.67 |
| No.10 | 20.5 | 55.2 | 2.69 |
| 尿検体 | |||
| 検体1 | 36.8 | 105 | 2.85 |
| 検体2 | 12.0 | 31.9 | 2.66 |
| 検体3 | 44.5 | 151 | 3.39 |
| 血清検体 | |||
| 検体4 | 48.8 | 122 | 2.50 |
| 検体5 | 31.9 | 99.7 | 3.13 |
| 検体6 | 33.8 | 95.6 | 2.83 |
濃縮後の測定値と濃縮前の測定値から濃縮効果率を算出したところ、濃縮効果率は唾液検体で2.67-2.83、尿検体で2.66-3.39、血清検体で2.50-3.13といずれの検体種においても、濃縮効果の確認ができ、約3倍に近い値が得られた。
データ
添加回収試験
-
ヒト検体
添加(pg/mL) 測定値(pg/mL) 回収量(pg/mL) 回収率(%) 尿検体1 0 31.6 - - 100 125 93.4 93.4 尿検体2 0 52.9 200 250 197 98.5 添加(pg/mL) 測定値(pg/mL) 回収量(pg/mL) 回収率(%) 血清検体1 0 19.7 - - 100 112 92.3 92.3 血清検体2 0 30.2 - - 200 211 181 90.5 添加(pg/mL) 測定値(pg/mL) 回収量(pg/mL) 回収率(%) 唾液検体1 0 28.4 ー ー 25 50.2 21.8 87.2 500 505 477 95.4 唾液検体2 0 20.7 ー ー 25 46.4 25.7 103 500 517 496 99.2 唾液検体3 0 3.48* ー ー 25 25.2 21.7 86.8 500 444 440 88 唾液検体4 0 9.29 ー ー 25 35.8 26.5 106 500 541 531 106 唾液検体5 0 2.18* ー ー 25 23.4 21.2 84.8 500 444 442 88.4 唾液検体6 0 45.1 ー ー 25 66.5 21.4 85.6 500 599 554 111 唾液検体7 0 45.5 ー ー 25 67 21.5 86 500 474 429 85.8 唾液検体8 0 1.07* ー ー 25 24.4 23.3 93.2 500 435 434 86.8 唾液検体9 0 15.1 ー ー 25 39.2 24.1 96.4 500 506 491 98.2 唾液検体10 0 20.5 ー ー 25 44.7 24.2 96.8 500 469 449 89.8 唾液検体11 0 8.88 ー ー 25 34.3 25.4 102 500 449 440 88 * 検量線範囲外(<4.00 pg/mL)であったため参考値
-
マウス検体
添加量(pg/mL) 測定値(pg/mL) 回収量(pg/mL) 回収率(%) 血清検体 0 49.7 - - 50 107 57.3 115 100 152 102 102 250 305 255 102 500 586 536 107 平均 107 添加量(pg/mL) 測定値(pg/mL) 回収量(pg/mL) 回収率(%) 血漿検体 0 61.8 - - 50 110 48.2 96.4 100 156 94.2 94.2 250 320 258 103 500 595 533 107 平均 100 ラット検体
添加量(pg/mL) 測定値(pg/mL) 回収量(pg/mL) 回収率(%) 血清検体 0.00 18.8 - - 50.0 83.0 64.2 128 100 136 117 117 250 289 271 108 500 535 516 103 平均 114 添加量(pg/mL) 測定値(pg/mL) 回収量(pg/mL) 回収率(%) 血漿検体 0.00 60.1 - - 50.0 110 49.9 99.8 100 167 107 107 250 335 274 110 500 573 513 103 平均 105
希釈直線性試験
ヒト唾液
前処理した流涎検体にオキシトシンを100 pg/mL添加し、キット取扱説明書の検体調製方法に従って検体を調製した。調製した検体をキット緩衝液で10段階に希釈後、測定を行った(二重測定)。
参考文献
掲載論文
Nakata, M. et al.: Int. J. Mol. Sci., 24(9), 8248(2023). [マウス血漿]
1,5-Anhydro-D-Fructose Exhibits Satiety Effects via the Activation of Oxytocin Neurons in the Paraventricular Nucleus.
FAQ
検体について
- 測定可能な検体は何ですか。
- ヒト唾液 / 血清 / 血漿 / 尿、マウス血清 / 血漿、ラット血清 / 血漿で測定可能なことを確認しています。
- 必要な検体量はどのくらいですか。
- n=1の最低必要検体量は50 μLです。マウス血清・血漿ではキット付属の緩衝液で2倍、4倍に薄めても検出可能です。n=2では200 μLを推奨検体量としています。200 μLが必要なのは、前処理液2を添加し、遠心分離した後に生じる「ゲルを含む沈殿」を吸い込むことなく上清を分取するためです。(ゲルを吸い込まなければ、原理上200 μLより少ない検体でも測定は可能です)
- 検体の保存はどのようにすればよいですか。
- 検体を長期保存する場合は、検体にプロテアーゼ阻害剤である100KIU/mL アプロチニン(例: 製品コード 018-18111)と防腐剤である1/750 量(v/v)Proclin™950 を添加し、- 80℃以下での凍結保存を推奨します。
なお唾液検体の場合は、アプロチニンやProclin™ 950を添加しなくても、室温であれば6時間、冷蔵であれば24時間、-20℃であれば1ヶ月、-80℃であれば6ヶ月は測定値があまり変わりませんでした。(室温, 0時間での測定値に対する変化率が±15%以内)
なお繰り返しの凍結融解はできるだけ避けてください。当社では4回以上凍結融解すると測定値が15%以上変動することを確認しています。
- 唾液検体の採取はどのような方法が良いですか。
- 測定用の唾液採取には流涎法を推奨しています。流涎法とはバイアルやチューブなどに唾液を垂れ流すことで検体を採取する方法です。
コットンおよび不活化ポリマー素材のスワブで採取した場合にも、流涎法と同程度に測定が可能なことを確認しておりますが、スワブの素材によっては、測定対象が吸着する可能性がありますのでご注意ください。
前処理について
- 検体の前処理で、静置時間を延ばすことはできますか。
- 検体前処理液1の処理時間は延長しないでください。前処理液1は酸を含む溶液のため、添加後、検体は酸性状態になります。長時間の静置は検体マトリックスの変性が懸念されます。
検体前処理液2の処理時間は多少(1~4分程度)延びても問題ありません。標準の処理時間である5分は下回らないでください。
- 前処理で注意すべきポイントはありますか。
- 検体前処理液2に含まれるゲルは撹拌後時間が経過すると沈降するため、時々撹拌を加え、沈降に注意しながら添加してください。ゲルが十分に懸濁できておらず、添加するゲル量が不足している場合、反応阻害物質の除去不良のため異常値になる(B0のRLU<検体のRLU)可能性があります。また測定試料に検体前処理液2のゲルが混入すると異常値の原因となりますので、上清の分取時にゲルを吸い込まないようご注意ください。
- 粘性の高い唾液検体はどのように前処理すれば良いですか。
- 粘性の強い唾液は、本キットの添付文書に記載している前処理のみでは期待する測定値が得られない場合があります。その場合にはあらかじめアプロチニンとProclin™950を添加した唾液を一度凍結融解し、遠心分離 (例: 5,000g, 10分, 4℃)後の上清を検体として、本キットの添付文書に記載する前処理に進んでください。
- オキシトシン濃度の低い唾液検体はどのように処理すれば良いですか。
- オキシトシン濃度が低い検体については「唾液検体の濃縮方法(オプション)」をお試しください。必要検体量は増えますが、検体を濃縮して測定することが可能です。
- 前処理後の検体は保管可能ですか。
- 前処理した検体の保管は推奨していません。どうしても検体を保管しなければならない場合、密閉したポリプロピレンまたはポリエチレン製のチューブにて冷蔵(2-10℃)で保管し、翌日測定してください。測定時に不溶解物がみられる場合には、遠心分離等で除去し、上清を測定用検体としてください。
- 脳破砕液サンプルに検体前処理液1を入れると白濁しますが、このまま進めてもよいですか。
- 検体中のタンパク質濃度が高い場合や細胞破砕残物等が多く含まれている場合には、変性による白濁が発生するケースがございます。 その後、検体処理液2を添加し、ゲルを遠心分離で除いた上清中に白濁した不溶解物がない状態であれば、処理検体として測定に用いていただいて問題ありません。 不溶解物が残る場合は、遠心gを10,000g程度に上げるか、0.2μmフィルター処理を実施した後に処理検体としてご使用ください。
測定対象について
- バソプレッシンとの交差性はどの程度ですか。
- [Arg8]-バソプレッシンとの交差性は約2.9%です。
- メソトシン、イソトシン、バソトシンの測定は可能ですか。
- メソトシン、イソトシン、バソトシンについてはデータがございません。
キットについて
- 本キットの抗体を購入することは可能ですか。
- 抗体単体での販売はしておりません。
- 本キットの標準品 (オキシトシン)はどのようにして値付けを行っていますか。
- 本キット 標準品のオキシトシン濃度はWHO世界標準品 (OXYTOCIN 4th International Standard NIBSC code: 76/575) を用いて、値付けを行っております。
- プレートは分割使用できますか。
- いずれもセパレートタイプのプレートを使用しており、1列(8ウェル)毎に取り外しできるため、キットの分割使用が可能です。使用する分だけ取り外して、残りは冷蔵保管していただくと使用期限内は安定です。なお、プレートシールは使用するウェル分だけハサミ等で切ってご使用ください。
キットの使用について
- 本キットで測定する際に必要な試薬、器具、装置は何ですか。
- 本キットの使用には以下の試薬、器具、装置が必要です。本キットは高感度な競合法を採用しているため、プレートシェーカーおよび発光測定用プレートリーダーが必要となります。
- 精製水(蒸留水)
- 標準溶液 / 検体希釈用チューブ
- 洗浄液希釈用ガラス器具(メスシリンダー・ビーカー)
- チップ交換型ピペット(使い捨てチップで10 μL を正確にピペッティングできるもの、および200~500 μLを正確にピペッティングできるもの)
- 連続分注ピペット、100μL を連続分注できるもの
- ペーパータオル等の吸水性のあるもの(洗浄後にプレートに残った液を取り除く)
- 撹拌器(Vortex タイプ)
- マイクロプレート振とう器(約600~800 rpm)
- 96 ウエルプレート用洗浄機(あれば好ましい)または洗浄瓶
- 96 ウエルプレートリーダー(発光測定用)
- データ処理ソフトウェア
- 使用できるプレートリーダーにはどのようなものがありますか。
- 本キットの測定には発光測定用のプレートリーダーが必要となります。
当社では以下の装置を取り扱っております。
- プレートリーダーの測定条件をお教えください。
- 一例として、Tecan社 Infinite M200 PROを使用した時の条件を下記に示します。
装置: Tecan Infinite M200 PRO
ソフトウェア: PlateManegerV5
測定タイプ: エンドポイント測定
測定モード: 発光強度
プレートサイズ: 12 x 8
ウェルスキャンサイズ: 1 x 1
波長数: 1
測定値換算: W1
測定値単位: RLU
アテニュエーション1: AUTOMATIC
インテグレーションタイム1: 500 ms
セトルタイム1: 300 ms
- プレートシェーカーはどのようなものを選べば良いですか。
- ELISAプレートを500 rpm程度で撹拌できるシェーカーが必要です。
当社では以下の装置を取り扱っております。- プレートシェイカーMS 3 basic (IKA, コードNo. 627-05691 )
- MS3.4 マイクロプレート用アタッチメント (IKA, コードNo. 620-05681 )
- 本キットを使って受託サービスを提供することは可能ですか。
- 検査・受託会社において、本品を用いた営利目的での受託測定サービス※は基本的にお断りしております。
※顧客から依頼を受けて検体中のオキシトシンを測定し、その結果を提供することを目的としたサービス
トラブルシューティング
- 検量線が上手く引けない場合、どのようにすれば良いですか。
- 競合反応は可逆的ですが、ビオチン標識オキシトシン溶液添加後、標準品や検体を加えるまでに時間がかかりすぎてしまうと、バラつきの増加や、ベース発光強度の上昇が起こり、検量線の傾きが得られないことがあります。
検体や標準品は10-15分(競合反応時間の約1/10以内)を目安に添加を完了してください。検体数が多い場合には、フレキシブルプレート等に検体を分注し、マルチチャンネルピペットで分注すると効率的です。
- バックグラウンドよりも検体の測定値が高くなる場合、どうすれば良いですか。
- 前処理で検体中の反応阻害物質が除去できていないと、バックグラウンドよりも検体のRLUが高くなる(競合ELISAにおいてB0のRLU<検体のRLU)場合があります。特に検体前処理液2に含まれるゲル量が不足していると反応阻害物質が除去できないことがあります。ゲルは撹拌後時間が経過すると沈降するため、時々撹拌を加え沈降に注意しながら添加してください。また前処理後の試料に検体前処理液2のゲルが混入すると異常値の原因となりますので、上清の分取時にゲルを吸い込まないようご注意ください。
- 低濃度域の測定が上手くできない場合、どうすれば良いですか。
- 各工程の撹拌を十分に行ってください。特に注意すべきは以下の工程です。
検体あるいは標準品の添加直後
十分に撹拌が必要です。連続的に撹拌を行うより、一旦停止し再度撹拌を開始する方が均一に混和されます。目安として[マイクロプレート振とう器で600-800 rpmで10秒間撹拌→一旦停止→再度撹拌]を3回繰り返すことを推奨します。 競合反応中
推奨の撹拌速度は500 rpmです。撹拌の速度や強度が不足している場合、低濃度域における反応性が低下する恐れがあります。 ペルオキシダーゼ結合ストレプトアビジン溶液の添加直後
検体や標準品の添加直後と同様に十分な撹拌が必要です。目安として[マイクロプレート振とう器で600-800 rpmで10秒間撹拌→一旦停止→再度撹拌]を3回繰り返すことを推奨します。
- 洗浄時、ウェルの中に泡が残る場合、どうすれば良いですか。
- 洗瓶等を用いたマニュアル洗浄の場合、最終回数の洗浄のみ洗浄液をオーバーフローさせて泡を回避する方法をお試しください。洗浄にはキット付属の洗浄液をご使用ください。超純水はハングリーウォーターとも呼ばれ、接する物質を取り込む性質が強く、抗原抗体結合物等への影響が懸念されるため、洗浄には使用しないでください。
概要・使用例
| 概要 | オキシトシンは9アミノ酸からなるペプチドホルモンです。視床下部で産生されており、出産や授乳をきっかけに主に下垂体後葉から放出され、子宮の収縮や母乳の分泌を促進します。その他にも母性行動の形成や抗ストレス作用などに関与することから、通称「幸せホルモン」、「愛情ホルモン」と呼ばれています。 本品は検体中のオキシトシンを測定可能なELISAキットです。本キットは従来より簡便な前処理で測定可能であり、従来前処理法として行われていたC18カラムや有機溶媒を用いた精製が不要です。 検量線範囲 :4-1,024pg/mL 測定対象検体:ヒト唾液、尿、血漿、血清、マウス血清、血漿、ラット血漿、血清 必要検体量 :50μL(n=1での最低必要量)、200μL(n=2での推奨量) 測定時間 :2時間半 検出法 :発光 ■受託測定サービスについて 検査・受託会社において、本品を用いた営利目的での受託測定サービス※は基本的にお断りしております。 ※顧客から依頼を受けて検体中のオキシトシンを測定し、その結果を提供することを目的としたサービス |
|---|
物性情報
「物性情報」は参考情報でございます。規格値を除き、この製品の性能を保証するものではございません。
本製品の品質及び性能については、本品の製品規格書をご確認ください。
なお目的のご研究に対しましては、予備検討を行う事をお勧めします。
製造元情報
別名一覧
- 掲載内容は本記事掲載時点の情報です。仕様変更などにより製品内容と実際のイメージが異なる場合があります。
- 製品規格・包装規格の改訂が行われた場合、画像と実際の製品の仕様が異なる場合があります。
- 掲載されている製品について
- 【試薬】
- 試験・研究の目的のみに使用されるものであり、「医薬品」、「食品」、「家庭用品」などとしては使用できません。
- 試験研究用以外にご使用された場合、いかなる保証も致しかねます。試験研究用以外の用途や原料にご使用希望の場合、弊社営業部門にお問合せください。
- 【医薬品原料】
- 製造専用医薬品及び医薬品添加物などを医薬品等の製造原料として製造業者向けに販売しています。製造専用医薬品(製品名に製造専用の表示があるもの)のご購入には、確認書が必要です。
- 表示している希望納入価格は「本体価格のみ」で消費税等は含まれておりません。
- 表示している希望納入価格は本記事掲載時点の価格です。