ReStart LUCTM Full Kit
ReStart LUCTM full Kit
- 製造元 :
- 東洋ビーネット(株)
- 保存条件 :
- -80℃ (ドライアイス輸送)
- 構造式
- ラベル
- 荷姿
|
比較
|
製品コード
|
容量
|
価格
|
在庫
|
|
|---|---|---|---|---|---|
|
|
|
100回用
|
|
|
ドキュメント
キットコンポーネント
100回用
| RS発光基質(凍結乾燥品) | 1 本 |
|---|---|
| RS発光基質溶解液(10 mL) | 1 本 |
| C Protein試薬(200 µL) | 1 本 |
| N Protein試薬(100 µL) | 1 本 |
| N Protein試薬 希釈液(900 µL) | 1 本 |
| C Protein Control Vector(0.5 µg/µL, 20 µL) | 1 本 |
| C Protein Test Vector(0.5 µg/µL, 20 µL) | 1 本 |
概要

ルシフェラーゼはホタルの発光反応を触媒する酵素として広く知られており、これまでに多くの発光生物のルシフェラーゼ遺伝子がクローニングされ、遺伝子発現マーカーなどとして研究現場で用いられています。しかしながら、ルシフェラーゼ分子はその大きさゆえ細胞膜を透過できないというデメリットもありました。
ReStart LUC™ は細胞膜と透過できるルシフェラーゼ断片をターゲットタンパク質に融合させることにより膜透過可能な検出タグです。
※本製品には東洋ビーネットが保有する複数の特許技術が採用されています。ご購入いただく際には事前に「購入同意書」のご提出をお願いします。
詳細は当社営業担当者または販売代理店担当者までお問い合わせください。
-
特長
- 信頼性
使用実績が最も高い北米産ホタル・ルシフェラーゼを採用 - 迅速
発光測定まで約 10 分
(検出操作はルシフェラーゼを再構築させて発光反応測定を行なうだけ) - 高感度
高 SN 比により、微量な分泌量の差異も判別可能
- 信頼性
-
主な用途
- 分泌タンパク質の局在/分泌量のモニタリング
- 細胞膜表面における膜タンパク質の発現解析
- チャネル異常の研究
測定原理
特定の位置で切断して生物発光能を失活させた北米産ホタルルシフェラーゼを再構成することにより、発光能を回復させます。その際、ルシフェラーゼの C 末端側を検出タグとすることで、以下のような解析を行なうことができます。
- 分泌シグナルの解析(解析例Ⅰ・Ⅱ)
- タンパク質の細胞内小器官移行解析(解析例Ⅲ)
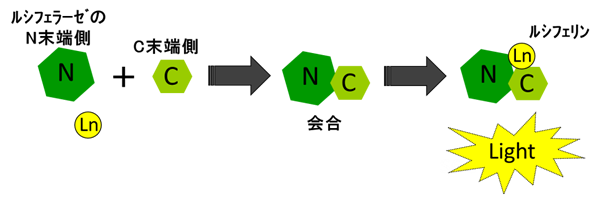
ホタル・ルシフェラーゼはその大きさから細胞膜を透過できませんが、 ReStart LUC™は、細胞膜を透過できるルシフェラーゼ断片をターゲットタンパク質に融合発現させることで膜透過可能な検出 Tag として使用できます。
解析例
分泌タンパク質のモニタリング解析
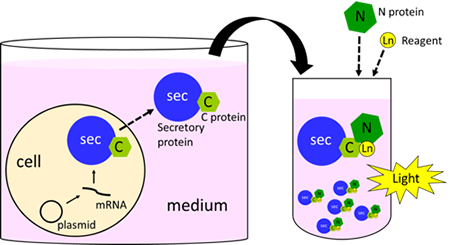
図 1. 分泌シグナルペプチドの解析方法
ステップ1
北米産ホタルルシフェラーゼの C 末端側(C Protein)遺伝子とシグナルペプチド遺伝子を結合させ、細胞に導入して発現させる。
ステップ2
分泌されたシグナルペプチドを含む培地に、北米産ホタルルシフェラーゼのN末端側(N Protein)を含む N Protein 試薬を添加してルシフェラーゼを再構成し、発光量を測定する。
【解析例Ⅰ】分泌タンパク質の細胞外(培地中)への移行解析
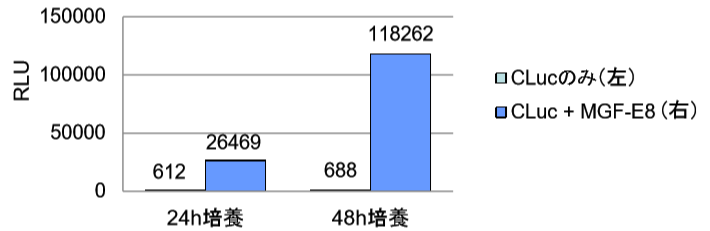
CHO細胞に、“C Protein のみを発現するように開始コドンのみを挿入した C Protein Test Vector + ATG(CLucのみ)”または“分泌タンパク質(Milk Growth Factor-E8)と C Protein の融合タンパク質を発現する C Protein Control Vector(CLuc + MGF-E8)”をトランスフェクションした。24 時間または 48 時間培養後、培地を回収し、N Protein 試薬を添加してルシフェラーゼを再構成させ、RS 発光試薬を加えて発光量を測定した。
コントロールベクターを導入した細胞の培養上清中には、MGF-E8 と C Protein の融合タンパク質が分泌されたため、発光を確認できた(グラフ:MGF-E8)。
【解析例Ⅱ】分泌タンパク質の細胞外(培地中)への移行解析 ~阻害剤による影響~
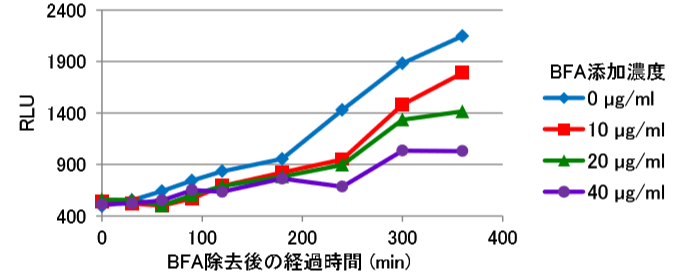
CHO細胞に、“分泌タンパク質(Milk Growth Factor-E8)と C Protein の融合タンパク質を発現する C Protein Control Vector”をトランスフェクションした。24 時間培養後、Brefeldin A (BFA)を添加した培地に培地交換した。1 時間後に BFA 入りの培地を除去し、PBS で洗浄後、BFA を含まない新しい培地に再交換した。培地交換から一定時間後に培地を回収し、N Protein 試薬を添加してルシフェラーゼを再構成させ、RS 発光試薬を加えて発光量を測定した。
BFA処理による細胞外への分泌阻害を確認できた。また、阻害からの回復時間は、BFA濃度に比例していた。
膜タンパク質の細胞膜表面への移行解析
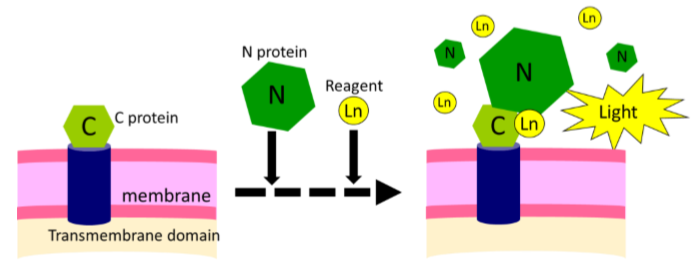
図 2. タンパク質の細胞内移行解析方法
ステップ1
細胞膜上に発現するよう設計されたベクターに北米産ホタルルシフェラーゼの C 末端側(C Protein)遺伝子を導入し、細胞で発現させる。
ステップ2
北米産ホタルルシフェラーゼの N 末端側(N Protein)を含む N Protein 試薬を添加し、細胞膜上でルシフェラーゼを再構成して発光量を測定する。
【解析例Ⅲ】タンパク質の細胞膜表面への移行解析 ~阻害剤による影響~
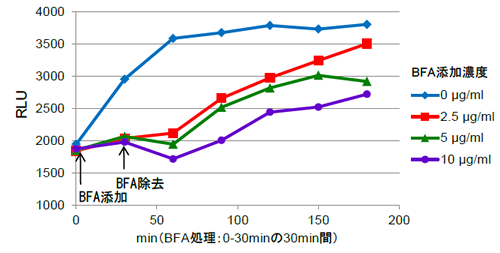
CHO 細胞に、pDisplay Vector(Sigma社)に C Protein を導入したプラスミド(pDisplay-C Protein)をトランスフェクションした。24 時間培養後、トリプシン-EDTA で細胞をはがして回収した。回収した細胞を各濃度の Brefeldin A (BFA)で 30 分間処理し、BFA を含まない新しい培地に再交換した。一定時間毎に細胞を回収し、N Protein 試薬を添加してルシフェラーゼを再構成させた後、RS 発光試薬を加えて発光量を測定した。
BFA処理による細胞表面への移行阻害が確認できた。また、阻害からの回復時間は、BFA濃度に比例していることが分かる。
※本解析では、細胞を剥がす際にトリプシン-EDTA を使用しているため、回収直後の細胞では細胞膜表面上の C Protein は分解されている。BFA処理後の経過時間中に発現した C Protein 量を発光量として確認している。
概要・使用例
| 概要 | 「タンパク質の局在&移行」を高感度に解析 ReStart LUCキット ルシフェラーゼはホタルの発光反応を触媒する酵素として広く知られており、これまでに多くの発光生物のルシフェラーゼ遺伝子がクローニングされ、遺伝子発現マーカーなどとして研究現場で用いられています。しかしながら、ルシフェラーゼ分子はその大きさゆえ細胞膜を透過できないというデメリットもありました。ReStart LUCは、細胞膜を透過できるルシフェラーゼ断片をターゲットタンパク質に融合させることにより膜透過可能な検出タグです。 特 長 ■信頼性 : 使用実績が最も高い北米産ホタル・ルシフェラーゼを採用 ■迅 速 : 発光測定まで約10分 (検出操作はルシフェラーゼを再構築させて発光反応測定を行うだけ) ■高感度 : 高SN比により、微量な分泌量の差異も判別可能 主な用途 ●分泌タンパク質の局在/分泌量のモニタリング ●細胞膜表面における膜タンパク質の発現解析 ●チャネル異常の研究 測定原理 特定の位置で切断して生物発光能を失活させた北米産ホタルルシフェラーゼを再構成することにより、発光能を回復させます。その際、ルシフェラーゼのC末端側を検出タグとすることで、以下のような解析を行うことができます。 ①分泌シグナルの解析 ②タンパク質の細胞内小器官移行解析 ホタル・ルシフェラーゼはその大きさから細胞膜を透過できませんが、 ReStart LUCは、細胞膜を透過できるルシフェラーゼ断片をターゲットタンパク質に融合発現させることで膜透過可能な検出Tagとして使用できます。 (Wako BioWindow JAN. 2019 / No.158, p6) |
|---|
物性情報
「物性情報」は参考情報でございます。規格値を除き、この製品の性能を保証するものではございません。
本製品の品質及び性能については、本品の製品規格書をご確認ください。
なお目的のご研究に対しましては、予備検討を行う事をお勧めします。
製造元情報
別名一覧
- 掲載内容は本記事掲載時点の情報です。仕様変更などにより製品内容と実際のイメージが異なる場合があります。
- 製品規格・包装規格の改訂が行われた場合、画像と実際の製品の仕様が異なる場合があります。
- 掲載されている製品について
- 【試薬】
- 試験・研究の目的のみに使用されるものであり、「医薬品」、「食品」、「家庭用品」などとしては使用できません。
- 試験研究用以外にご使用された場合、いかなる保証も致しかねます。試験研究用以外の用途や原料にご使用希望の場合、弊社営業部門にお問合せください。
- 【医薬品原料】
- 製造専用医薬品及び医薬品添加物などを医薬品等の製造原料として製造業者向けに販売しています。製造専用医薬品(製品名に製造専用の表示があるもの)のご購入には、確認書が必要です。
- 表示している希望納入価格は「本体価格のみ」で消費税等は含まれておりません。
- 表示している希望納入価格は本記事掲載時点の価格です。



